9. 化石燃料的开发、利用和燃烧尾气处理成为研究的热点。
(1)利用焦炉煤气制取甲醇,发生的主要反应为CO(g)+2H
2(g)

CH
3OH(g)。下表所列为常见化学键的键能数据:(提示CO和N
2是等电子体,其电子式相似)
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能(kJ/mol) | 348 | 414 | 436 | 327 | 1032 | 464 |
则CO(g)+2H
2(g)

CH
3OH(g)的△
H=__________ kJ·mol
-1,若想提高CH
3COH的产率,可以采取的措施有
__________、
__________(任写2条)。
(2)可以用H
2等清洁能源代替天然气(主要成分CH
4),两者的热化学方程式如下:H
2(g) +

O
2(g) = H
2O(1) △
H= -286 kJ·mol
-1;CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(l)
△
H=-890 kJ/mol。现有H
2与CH
4的混合气体112L(标准状况),使其完全燃烧生成CO
2和H
2O(l),若实验测得反应放热2034 kJ,则原混合气体中H
2与CH
4的物质的量之比是
_______。反应过程中消耗的氧气在标注状况下的体积为
_________ 。
(3)化石燃料会排放含SO
2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO
2体。1molCH
4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:
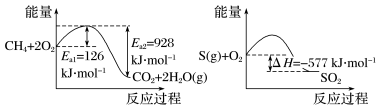
在催化剂作用下,CH
4可以还原SO
2生成单质S(g)、H
2O(g)和CO
2,写出该反应的热化学方程式:
__________;也可以用NaOH吸收化石燃料燃烧产生的SO
2,然后通入足量的O
2,这样做的目的是
__________;
(4)第(3)题中得到的S在O
2中燃烧生成SO
2,在催化剂的作用下与O
2发生反应产生SO
3,所发生的的化学方程式为2SO
2(g) +O
2(g)

2SO
3(g),在温度不变的情况下,同时加快该反应的化学反应速率和提高SO
2的转化率的措施有
__________(任写1条)。