10. 2-溴戊二酸二甲酯是某抗癌药物的重要中间体,其制备的反应原理如下:
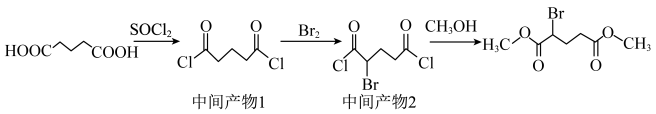
装置示意图如下图所示(夹持装置已略去),实验步骤为:
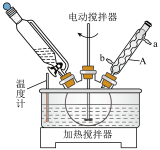
Ⅰ.制备
将10.0g戊二酸加入三颈烧瓶中,再向其中加入三氯甲烷 ,搅拌均匀。保持
,搅拌均匀。保持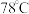 条件下,依次缓慢滴加氯化亚砜
条件下,依次缓慢滴加氯化亚砜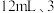 滴催化剂、液溴,随后回流。回流完毕后,将三颈烧瓶置于冰盐浴中,待溶液温度降到
滴催化剂、液溴,随后回流。回流完毕后,将三颈烧瓶置于冰盐浴中,待溶液温度降到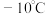 后,缓慢滴加
后,缓慢滴加 甲醇(沸点
甲醇(沸点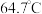 ),保持滴加过程中温度不超过
),保持滴加过程中温度不超过 。
。
Ⅱ.除杂
向三颈烧瓶中加入 饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用
饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用 饱和氯化钠溶液洗涤3次。洗涤完毕,用无水硫酸镁干燥,过滤。
饱和氯化钠溶液洗涤3次。洗涤完毕,用无水硫酸镁干燥,过滤。
Ⅲ.提纯过滤后的液体置于热浴容器中(外温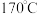 ,接上精馏装置,进行减压蒸馏。
,接上精馏装置,进行减压蒸馏。
Ⅳ.收集产品收集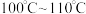 的馏分,得到
的馏分,得到 无色透明油状液体。
无色透明油状液体。
回答下列问题:
(1)仪器

的名称是
___________;冷却水应从
___________(填“a”或“b”)口通入。
(2)步骤Ⅰ中采取“温度降到
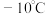
”、“缓慢滴加”这些措施的可能原因是
___________。
(3)步骤Ⅱ中加入饱和氯化钠溶液的目的是
___________。
(4)步骤Ⅲ中,热浴容器中应加入
___________(填“水”或“油”)作为热传导介质。
(5)中间产物1(戊二酰氯)比戊二酸的沸点低很多,原因是
___________;反应中生成戊二酰氯的同时得到两种有刺激性气味的气体,该反应的化学方程式为
___________。
(6)从绿色化学角度分析,该实验装置存在明显不足之处,解决的办法是
___________。
(7)本实验的产率是
___________(填标号,已知相对分子质量:戊二酸132,2-溴戊二酸二甲酯239)。
a. b.
b. c.
c. d.
d.