2024届河南省豫南名校高三下学期第二次质量检测理科综合试卷-高中化学
河南
高三
二模
2024-05-19
117次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础
2024届河南省豫南名校高三下学期第二次质量检测理科综合试卷-高中化学
河南
高三
二模
2024-05-19
117次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
1. 化学在人类卫生保健中有着极为重要的作用。下列说法错误的是
| A.用于给环境消毒的84消毒液的有效成分是NaClO |
B.用于生产医用口罩的聚丙烯可使酸性 溶液褪色 溶液褪色 |
| C.用于配制免洗洗手液的过氧乙酸能使蛋白质变性 |
| D.用酒精溶液消毒时,75%的酒精溶液消毒效果最好 |
【知识点】 漂白粉和漂粉精 蛋白质的变性 化学科学对人类文明发展的意义解读
您最近一年使用:0次
2024-05-19更新
|
192次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
单选题
|
适中(0.65)
名校
2. 我国西沙群岛软珊瑚中存在多种朵蕾烷二萜类天然产物,结构如图所示,它们具有较强抗菌、抗肿瘤等生物活性。下列关于该二萜类化合物说法错误的是
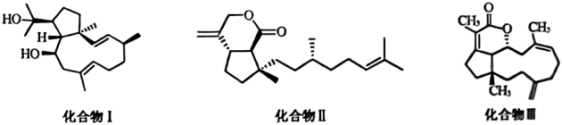
| A.化合物I不属于芳香族化合物 |
B.化合物II能使 的 的 溶液褪色 溶液褪色 |
| C.化合物III不能发生水解反应 |
D.等物质的量的化合物I、II、III最多消耗 的物质的量之比为2:2:3 的物质的量之比为2:2:3 |
【知识点】 有机反应类型 有机官能团的性质及结构
您最近一年使用:0次
2024-05-19更新
|
83次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
单选题
|
适中(0.65)
3. 硫化亚砷(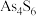 )常用作颜料、还原剂和药物等,易溶于NaOH溶液,反应原理为
)常用作颜料、还原剂和药物等,易溶于NaOH溶液,反应原理为
 。下列说法正确的是
。下列说法正确的是
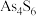 )常用作颜料、还原剂和药物等,易溶于NaOH溶液,反应原理为
)常用作颜料、还原剂和药物等,易溶于NaOH溶液,反应原理为
 。下列说法正确的是
。下列说法正确的是A.键角: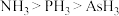 |
| B.第一电离能:O>N>S |
C. 的空间结构是平面三角形 的空间结构是平面三角形 |
| D.基态As原子有33种能量不同的电子 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
4.  同时作为燃料和氧化剂的直接过氧化氢燃料电池(DPPFC)的工作原理如图所示(电解过程中
同时作为燃料和氧化剂的直接过氧化氢燃料电池(DPPFC)的工作原理如图所示(电解过程中 溶液中溶质的种类不变且其质量减轻)。下列有关说法错误的是
溶液中溶质的种类不变且其质量减轻)。下列有关说法错误的是
 同时作为燃料和氧化剂的直接过氧化氢燃料电池(DPPFC)的工作原理如图所示(电解过程中
同时作为燃料和氧化剂的直接过氧化氢燃料电池(DPPFC)的工作原理如图所示(电解过程中 溶液中溶质的种类不变且其质量减轻)。下列有关说法错误的是
溶液中溶质的种类不变且其质量减轻)。下列有关说法错误的是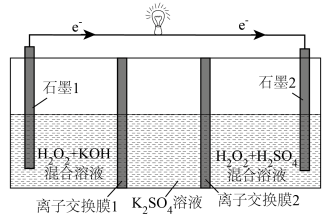
| A.石墨1为负极,发生氧化反应 |
B.石墨2的电极反应式为 |
| C.离子交换膜1、2分别为阴、阳离子交换膜 |
D.当外电路中转移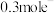 时, 时, 溶液的质量减轻52.2g 溶液的质量减轻52.2g |
您最近一年使用:0次
2024-05-20更新
|
116次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
单选题
|
适中(0.65)
名校
5. 下列实验操作、现象及得出的结论均正确的是
| 选项 | 实验操作、现象 | 实验结论 |
| A |  的 的 溶液与 溶液与 的 的 溶液等体积混合,产生白色沉淀 溶液等体积混合,产生白色沉淀 | 结合 能力: 能力: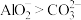 |
| B | 将补铁口服液(含维生素C)滴入酸性 溶液,紫红色褪去 溶液,紫红色褪去 | 补铁口服液中含有 |
| C | 将久置的 加入稀盐酸中,产生气泡 加入稀盐酸中,产生气泡 |  已经变质 已经变质 |
| D | 取两份新制氯水,分别滴加 溶液和淀粉-KI溶液,前者有白色沉淀,后者溶液变蓝 溶液和淀粉-KI溶液,前者有白色沉淀,后者溶液变蓝 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
【知识点】 过氧化钠与水的反应解读 弱电解质的电离平衡 化学实验方案的设计与评价
您最近一年使用:0次
2024-05-19更新
|
138次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
单选题
|
适中(0.65)
名校
6. 一种捕获 并将其转化为
并将其转化为 的反应历程如图所示。
的反应历程如图所示。
 并将其转化为
并将其转化为 的反应历程如图所示。
的反应历程如图所示。
| A.所有中间产物中均存在配位键 | B.反应过程中N元素的化合价没变 |
C. 为催化剂 为催化剂 | D.反应过程中存在非极性键的断裂和形成 |
您最近一年使用:0次
2024-05-19更新
|
41次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
单选题
|
较难(0.4)
名校
7. 25℃条件下,改变亚碲酸[开始时, ]溶液的pH,溶液中
]溶液的pH,溶液中 、
、 、
、 、
、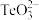 的物质的量分数
的物质的量分数 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ]。下列说法错误的是
]。下列说法错误的是
 ]溶液的pH,溶液中
]溶液的pH,溶液中 、
、 、
、 、
、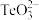 的物质的量分数
的物质的量分数 随pH的变化如图所示[已知
随pH的变化如图所示[已知 ]。下列说法错误的是
]。下列说法错误的是
A. |
B. 的平衡常数 的平衡常数 |
C. 时, 时, |
D. 溶液中: 溶液中: |
您最近一年使用:0次
2024-05-19更新
|
47次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
8. 某工厂废渣的主要成分为ZnO、PbO、 、CuO、
、CuO、 等(
等( 与
与 性质相似),以该工厂废渣为主要原料回收其中金属元素的工艺流程如图所示:
性质相似),以该工厂废渣为主要原料回收其中金属元素的工艺流程如图所示:
(1)“焙烧”产生的气体是___________ (填分子式),该气体的用途是___________ (填一条)。
(2)“氨浸”所得滤液1中的阳离子主要成分为 、
、 ,该步骤温度不宜过高,其原因是
,该步骤温度不宜过高,其原因是___________ ,“沉铜”时发生反应的离子方程式为___________ 。
(3)“滤渣4”的主要成分为___________ (填化学式)。
(4)“滤液3”的主要溶质为 ,以惰性电极电解该滤液可以回收单质Ga,电解时阴极主要电极反应式为
,以惰性电极电解该滤液可以回收单质Ga,电解时阴极主要电极反应式为___________ 。
(5)“转化”时生成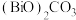 的同时放出能使澄清石灰水变浑浊的气体,该步骤的化学方程式为
的同时放出能使澄清石灰水变浑浊的气体,该步骤的化学方程式为___________ 。
(6)铁酸铋具有铁电性和反铁磁性,其晶胞结构如图所示,晶胞参数为a pm。___________ 。
②该晶体的密度=___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 、CuO、
、CuO、 等(
等( 与
与 性质相似),以该工厂废渣为主要原料回收其中金属元素的工艺流程如图所示:
性质相似),以该工厂废渣为主要原料回收其中金属元素的工艺流程如图所示:
(1)“焙烧”产生的气体是
(2)“氨浸”所得滤液1中的阳离子主要成分为
 、
、 ,该步骤温度不宜过高,其原因是
,该步骤温度不宜过高,其原因是(3)“滤渣4”的主要成分为
(4)“滤液3”的主要溶质为
 ,以惰性电极电解该滤液可以回收单质Ga,电解时阴极主要电极反应式为
,以惰性电极电解该滤液可以回收单质Ga,电解时阴极主要电极反应式为(5)“转化”时生成
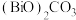 的同时放出能使澄清石灰水变浑浊的气体,该步骤的化学方程式为
的同时放出能使澄清石灰水变浑浊的气体,该步骤的化学方程式为(6)铁酸铋具有铁电性和反铁磁性,其晶胞结构如图所示,晶胞参数为a pm。
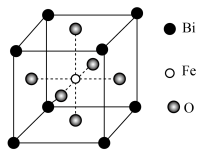
②该晶体的密度=
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
名校
解题方法
9. 氨基钠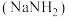 可用作有机合成的还原剂、脱水剂等。已知,i.
可用作有机合成的还原剂、脱水剂等。已知,i. 几乎不溶于液氨,易与水、氧气等反应;ii.
几乎不溶于液氨,易与水、氧气等反应;ii.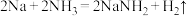 、
、 、
、 。回答下列问题:
。回答下列问题:
I.制备氨基钠___________ (填仪器接口字母,必要时个别装置可重复使用)。
(2)仪器x的名称为___________ ,装置A的作用为___________ 。
(3)装置B中制备 的化学方程式为
的化学方程式为___________ 。
(4) 的作用是
的作用是___________ ,若装置D中生成1.12L(标准状况下) ,则消耗
,则消耗___________ gNa。
(5)反应前装置D中需通入氨气排尽体系中空气,设计方案判断密闭体系中空气是否排尽:___________ 。
II.氨基钠产品质量分数测定
称量2.0g氨基钠产品,溶于水配成500mL溶液;量取25mL溶液,加热除去 ,冷却至室温后,滴入2滴酚酞试液,用
,冷却至室温后,滴入2滴酚酞试液,用 的HCl标准溶液进行滴定,记下达到滴定终点所消耗HCl标准溶液的体积,重复上述实验4次,滴定结果如下表。
的HCl标准溶液进行滴定,记下达到滴定终点所消耗HCl标准溶液的体积,重复上述实验4次,滴定结果如下表。
(6)氨基钠的质量分数为___________ %(保留三位有效数字)。
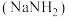 可用作有机合成的还原剂、脱水剂等。已知,i.
可用作有机合成的还原剂、脱水剂等。已知,i. 几乎不溶于液氨,易与水、氧气等反应;ii.
几乎不溶于液氨,易与水、氧气等反应;ii.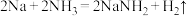 、
、 、
、 。回答下列问题:
。回答下列问题:I.制备氨基钠

(2)仪器x的名称为
(3)装置B中制备
 的化学方程式为
的化学方程式为(4)
 的作用是
的作用是 ,则消耗
,则消耗(5)反应前装置D中需通入氨气排尽体系中空气,设计方案判断密闭体系中空气是否排尽:
II.氨基钠产品质量分数测定
称量2.0g氨基钠产品,溶于水配成500mL溶液;量取25mL溶液,加热除去
 ,冷却至室温后,滴入2滴酚酞试液,用
,冷却至室温后,滴入2滴酚酞试液,用 的HCl标准溶液进行滴定,记下达到滴定终点所消耗HCl标准溶液的体积,重复上述实验4次,滴定结果如下表。
的HCl标准溶液进行滴定,记下达到滴定终点所消耗HCl标准溶液的体积,重复上述实验4次,滴定结果如下表。| 实验数据 | 滴定次数 | |||
| 1 | 2 | 3 | 4 | |
| V(产品)/mL | 25.00 | 25.00 | 25.00 | 25.00 |
| V[HCl(标准溶液)]/mL | 25.75 | 25.00 | 25.05 | 24.95 |
(6)氨基钠的质量分数为
您最近一年使用:0次
2024-05-19更新
|
100次组卷
|
2卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
解答题-原理综合题
|
较难(0.4)
名校
10. 二甲醚(DME)作为一种新兴的基本有机化工原料,在制药、燃料、农药等化学工业中有许多独特的用途,其制备方法有CO氢化法、 氢化法、
氢化法、 电化法等。回答下列问题:
电化法等。回答下列问题:
(1)CO氢化法所涉及的反应如下:
反应i.
 ;
;
反应ii.
 ;
;
反应iii.
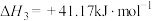 。
。
①反应iv。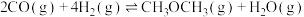

___________  ,利于该反应正向进行的条件是
,利于该反应正向进行的条件是___________ (填“高温”“低温”或“任意温度”)。
②将 和
和 充入密闭容器中仅发生反应iv,平衡体系中
充入密闭容器中仅发生反应iv,平衡体系中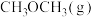 的物质的量分数与压强和温度的关系如图所示,关于温度和压强的关系判断正确的是
的物质的量分数与压强和温度的关系如图所示,关于温度和压强的关系判断正确的是___________ (填字母)。 ,
,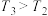 B.
B. ,
,
C. ,
, D.
D. ,
,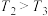
(2)在某温度及压强为pMPa条件下,在密闭容器中按物质的量之比1:2充入 、
、 ,发生反应
,发生反应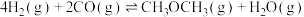 ,平衡时
,平衡时 的转化率为50%。
的转化率为50%。
①达平衡时,
___________ MPa。
②该温度下,平衡常数
___________ MPa-4(以平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
(3) 氢化法反应原理为反应v。
氢化法反应原理为反应v。
 。在一定压强、
。在一定压强、 和
和 的起始投料一定的条件下,发生反应iii、反应v,实验测得
的起始投料一定的条件下,发生反应iii、反应v,实验测得 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。 的选择性
的选择性 ,其中表示平衡时
,其中表示平衡时 的选择性的是曲线
的选择性的是曲线___________ (填“x”或“y”)。
②温度高于300℃时,曲线y随温度升高而升高的原因是___________ 。
③为同时提高 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为___________ (填字母)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
(4) 电化法工作原理如图所示:阴极电极反应式为
电化法工作原理如图所示:阴极电极反应式为___________ ,电解过程中右池溶液的质量___________ (填“增大”“减少”或“不变”)。
 氢化法、
氢化法、 电化法等。回答下列问题:
电化法等。回答下列问题:(1)CO氢化法所涉及的反应如下:
反应i.

 ;
;反应ii.

 ;
;反应iii.

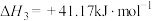 。
。①反应iv。
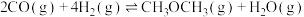

 ,利于该反应正向进行的条件是
,利于该反应正向进行的条件是②将
 和
和 充入密闭容器中仅发生反应iv,平衡体系中
充入密闭容器中仅发生反应iv,平衡体系中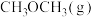 的物质的量分数与压强和温度的关系如图所示,关于温度和压强的关系判断正确的是
的物质的量分数与压强和温度的关系如图所示,关于温度和压强的关系判断正确的是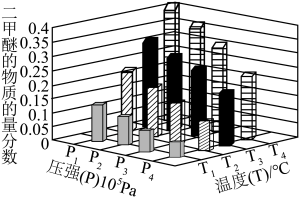
 ,
,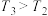 B.
B. ,
,
C.
 ,
, D.
D. ,
,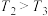
(2)在某温度及压强为pMPa条件下,在密闭容器中按物质的量之比1:2充入
 、
、 ,发生反应
,发生反应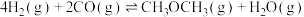 ,平衡时
,平衡时 的转化率为50%。
的转化率为50%。①达平衡时,

②该温度下,平衡常数

 物质的量分数)。
物质的量分数)。(3)
 氢化法反应原理为反应v。
氢化法反应原理为反应v。
 。在一定压强、
。在一定压强、 和
和 的起始投料一定的条件下,发生反应iii、反应v,实验测得
的起始投料一定的条件下,发生反应iii、反应v,实验测得 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。
的选择性随温度的变化如图所示。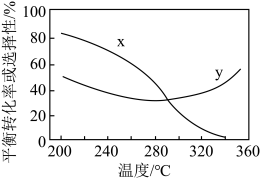
 的选择性
的选择性 ,其中表示平衡时
,其中表示平衡时 的选择性的是曲线
的选择性的是曲线②温度高于300℃时,曲线y随温度升高而升高的原因是
③为同时提高
 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
(4)
 电化法工作原理如图所示:阴极电极反应式为
电化法工作原理如图所示:阴极电极反应式为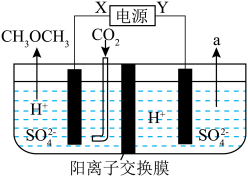
【知识点】 化学反应原理综合考查解读
您最近一年使用:0次
2024-05-19更新
|
141次组卷
|
3卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
解答题-有机推断题
|
较难(0.4)
11. 阿立哌唑对精神分裂症的阳性和阴性症状均有明显疗效,G是合成阿立哌唑的中间体,其合成路线如下:
(1)B的分子式为___________ ,C→D的反应类型为___________ 。
(2)E的结构简式为___________ ;D→E反应的另一种产物为___________ 。
(3)F→G反应中,有机副产物的结构简式是___________ 。
(4)写出F与过量NaOH水溶液反应的化学方程式:___________ 。
(5)F的同分异构体中同时满足下列条件的有___________ 种(不考虑立体异构),其中核磁共振氢谱有5组吸收峰,且峰面积比为1∶2∶2∶2∶2的化合物的结构简式为___________ 。
ⅰ.除苯环外无其他环状结构,只有1种含氧官能团,可以与银氨溶液反应,生成单质银;
ⅱ.苯环上有两个取代基,且氨基直接与苯环相连。

ⅰ. ;
;
ⅱ.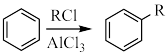 。
。
(1)B的分子式为
(2)E的结构简式为
(3)F→G反应中,有机副产物的结构简式是
(4)写出F与过量NaOH水溶液反应的化学方程式:
(5)F的同分异构体中同时满足下列条件的有
ⅰ.除苯环外无其他环状结构,只有1种含氧官能团,可以与银氨溶液反应,生成单质银;
ⅱ.苯环上有两个取代基,且氨基直接与苯环相连。
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、物质结构与性质、化学反应原理、化学实验基础
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 漂白粉和漂粉精 蛋白质的变性 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 有机反应类型 有机官能团的性质及结构 | |
| 3 | 0.65 | 电离能变化规律 键能、键长、键角及应用 利用杂化轨道理论判断分子的空间构型 | |
| 4 | 0.65 | 原电池原理理解 原电池有关计算 | |
| 5 | 0.65 | 过氧化钠与水的反应 弱电解质的电离平衡 化学实验方案的设计与评价 | |
| 6 | 0.65 | 催化剂对化学反应速率的影响 化学键与化学反应本质联系 简单配合物的成键 | |
| 7 | 0.4 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 盐的水解常数 弱电解质的电离平衡常数 | |
| 二、解答题 | |||
| 8 | 0.4 | 电子排布式 晶胞的有关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 9 | 0.4 | 氨气 氨的碱性 酸碱中和滴定原理的应用 常见无机物的制备 | 实验探究题 |
| 10 | 0.4 | 化学反应原理综合考查 | 原理综合题 |
| 11 | 0.4 | 常见官能团名称、组成及结构 根据要求书写同分异构体 有机物的推断 有机推断综合考查 | 有机推断题 |



