河南省天一大联考2021届高三上学期期末考试化学试题
河南
高三
期末
2021-02-08
587次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、化学反应原理、物质结构与性质
河南省天一大联考2021届高三上学期期末考试化学试题
河南
高三
期末
2021-02-08
587次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 化学和生活、生产息息相关。下列说法正确的是
| A.陈薇院士团队开发的腺病毒载体疫苗(Ad5-nCoV疫苗)性质稳定,该疫苗需在高温下保存 |
| B.海水稻制成的大米中含有淀粉、蛋白质、脂肪等,上述物质都是高分子 |
| C.我国“硅-石墨烯-锗晶体管”技术获得重大突破,上述涉及的三种元素都是短周期元素 |
| D.芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下发生分子间聚合而成像,该过程是化学变化 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
2. 实验室进行浓硫酸和铜反应的相关实验时,下列装置或操作错误的是
| A | B | C | D |
 | 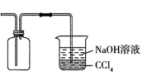 |  | 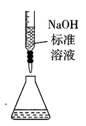 |
| 铜和浓硫酸反应 | 收集SO2并吸收尾气 | 加热CuSO4溶液以得到蓝色晶体 | 测定剩余硫酸的浓度 |
| A.A | B.B | C.C | D.D |
【知识点】 浓硫酸的强氧化性解读 物质性质实验方案的设计解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
3. 复杂天然产物MV合成过程的某片段如图(已知Me表示甲基),下列有关叙述错误的是


| A.X的分子式为C10H14O3 | B.X、Y都能使酸性重铬酸钾溶液变色 |
| C.X、Y中均最多有7个碳原子在同一平面 | D.能用Na来鉴别X、Y |
您最近一年使用:0次
2021-02-08更新
|
3222次组卷
|
5卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
河南省天一大联考2021届高三上学期期末考试化学试题山东省济南市莱芜第一中学2021届高三下学期2月校内检测化学试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)【奋进985】06-备战2022年高考化学名校进阶模拟卷(通用版)湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题
单选题
|
适中(0.65)
名校
4. 碳酸二甲酯(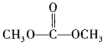 )是一种低毒、环保、性能优异、具有优良发展前景的“绿色”化工产品。纳米CeO2催化CO2和CH3OH合成碳酸二甲酯的示意图如图所示,下列说法正确的是
)是一种低毒、环保、性能优异、具有优良发展前景的“绿色”化工产品。纳米CeO2催化CO2和CH3OH合成碳酸二甲酯的示意图如图所示,下列说法正确的是
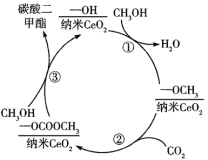
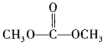 )是一种低毒、环保、性能优异、具有优良发展前景的“绿色”化工产品。纳米CeO2催化CO2和CH3OH合成碳酸二甲酯的示意图如图所示,下列说法正确的是
)是一种低毒、环保、性能优异、具有优良发展前景的“绿色”化工产品。纳米CeO2催化CO2和CH3OH合成碳酸二甲酯的示意图如图所示,下列说法正确的是
| A.CeO2可有效提高CH3OH的平衡转化率 | B.反应①中有O-H键的断裂 |
| C.反应②可以看作是取代反应 | D.上述转化过程中,中间产物有4种 |
您最近一年使用:0次
2021-02-08更新
|
601次组卷
|
5卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
5. LiY2ZXW2能够在锂离子电池负极形成稳定、低阻抗的SEI膜,帮助锂离子电池在高温环境中获得良好性能。[Y2Z4XW2]-的结构如图,图中原子最外层都达到8电子稳定结构,X、Y、Z、W位于同一短周期,元素X的最外层电子数是其内层电子数的1.5倍,W是同周期中原子半径最小的元素。下列说法正确的是
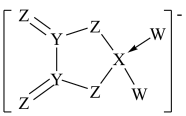
| A.该结构中,X、Y、Z之间形成的化学键均为共价键 |
| B.Y和Z形成的化合物都能和碱发生反应 |
| C.X、Y的最高价氧化物对应的水化物均是强酸 |
| D.Z和W分别与氢元素形成的10电子化合物的沸点:后者高于前者 |
您最近一年使用:0次
2021-02-08更新
|
888次组卷
|
5卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
河南省天一大联考2021届高三上学期期末考试化学试题(已下线)仿真卷01-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型10 物质结构与性质的综合分析与推断-高考必备50个题型湖北省荆州市沙市中学2023届高三模拟预测化学试题黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(三)试题
6. 羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为CO2、H2O的原电池-电解池组合装置(如图),该装置能实现发电、环保二位一体。下列说法错误的是
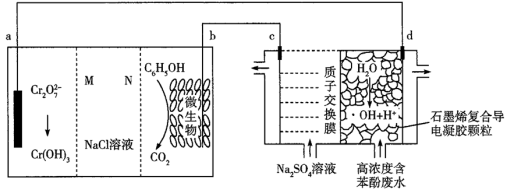

| A.a极为正极,c极为阴极 |
| B.b极的电极反应式为C6H5OH-28e-+11H2O=6CO2↑+28H+ |
| C.d极区苯酚被氧化的化学方程式为C6H5OH+28·OH=6CO2↑+17H2O |
| D.右侧装置中,每转移0.7mole-,c、d两极共产生气体3.36L(标准状况) |
您最近一年使用:0次
2021-02-08更新
|
2002次组卷
|
5卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
单选题
|
较难(0.4)
解题方法
7. ROH是一种一元碱,25℃时,在20.0mL0.1mol·L-1ROH溶液中滴加0.1mol·L-1盐酸VmL,混合溶液的pH与lg[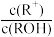 ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是
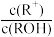 ]的关系如图所示。下列说法正确的是
]的关系如图所示。下列说法正确的是
| A.b点时,向溶液中加入一定量的水,b点向e点的方向移动 | B.a点时,V=10.0 |
| C.x=3.75 | D.c点溶液中,c(R+)>c(Cl-)>c(H+)>c(OH-) |
【知识点】 酸碱中和滴定的综合考查解读 盐的水解常数解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
解题方法
8. 利用某工业废料(主要成分为Co2O3,含有少量PbO、NiO、FeO)制备Co2O3和Ni(OH)2的流程如下。
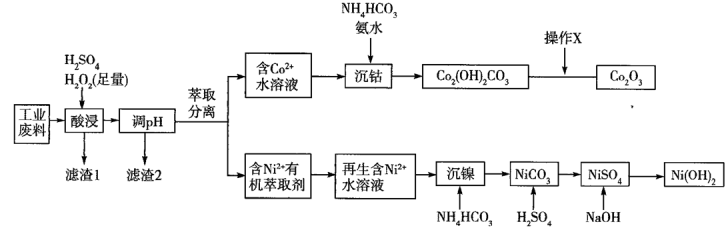
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
回答下列问题:
(1)“酸浸”时为加快反应速率,可采取的措施是___________ (答两条)。
(2)“酸浸”时Co2O3和H2O2能发生氧化还原反应,该反应的离子方程式为___________ ;滤渣1的主要成分是___________ (填化学式)。
(3)“调pH”时,pH调节的最小值是___________ ;操作X是高温煅烧,如果在实验室中进行操作X,装Co2(OH)2CO3的仪器的名称是___________ 。
(4)“沉钴”时发生反应的离子方程式为___________ 。
(5)Ni(OH)2可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH(M为储氢合金),电解液为KOH溶液,则放电时正极的电极反应式为___________ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
| 完全沉淀时的pH | 9.7 | 3.7 | 9.0 | 9.2 |
(1)“酸浸”时为加快反应速率,可采取的措施是
(2)“酸浸”时Co2O3和H2O2能发生氧化还原反应,该反应的离子方程式为
(3)“调pH”时,pH调节的最小值是
(4)“沉钴”时发生反应的离子方程式为
(5)Ni(OH)2可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH(M为储氢合金),电解液为KOH溶液,则放电时正极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
名校
解题方法
9. 某同学为探究NaHSO3溶液与Cu2+的反应,查阅资料设计如下实验:
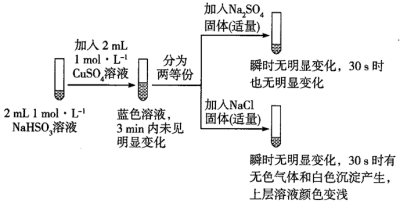
已知:①氯化亚铜(CuCl)为白色立方结晶或白色粉末,难溶于水;
②Cu2O [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)。
[Cu(NH3)4]2+(深蓝色溶液)。
回答下列问题:
(1)加入NaCl固体后产生的无色气体能使湿润的品红试纸褪色,且加热后能恢复原来的颜色,则该气体是___________ (填化学式);工业上将Na2S和Na2CO3以2:1的物质的量比配成溶液,然后通入该无色气体,Na2S、Na2CO3完全反应,得到硫代硫酸钠(Na2S2O3)和另一种无色无味的气体,该过程中发生反应的化学方程式是___________ 。
(2)该同学对实验中加入NaCl产生无色气体的原因进行分析,提出两种假设:
①假设1不成立的原因是___________ 。
②若假设2合理,请将假设2补充完整:___________ ,其中生成的白色沉淀是___________ (填化学式)。
(3)通过分析实验可知,Cl-增强了Cu2+的氧化性。某同学设计原电池实验(如图)证明上述实验结果,请将实验现象补充完整:___________ (写两点即可)。
(4)将实验后的溶液静置24小时或加热后,得到红色沉淀,洗涤干燥后利用已知信息设计实验,证明红色沉淀中含有Cu+:___________ 。

已知:①氯化亚铜(CuCl)为白色立方结晶或白色粉末,难溶于水;
②Cu2O
 [Cu(NH3)2]+(无色溶液)
[Cu(NH3)2]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)。
[Cu(NH3)4]2+(深蓝色溶液)。回答下列问题:
(1)加入NaCl固体后产生的无色气体能使湿润的品红试纸褪色,且加热后能恢复原来的颜色,则该气体是
(2)该同学对实验中加入NaCl产生无色气体的原因进行分析,提出两种假设:
| 假设1 | Cu2+水解使溶液中c(H+)增大 |
| 假设2 | Cl-存在时, 将Cu2+还原为Cu+,___________ 将Cu2+还原为Cu+,___________ |
②若假设2合理,请将假设2补充完整:
(3)通过分析实验可知,Cl-增强了Cu2+的氧化性。某同学设计原电池实验(如图)证明上述实验结果,请将实验现象补充完整:
| 编号 | 实验1 | 实验2 |
| 实验 | 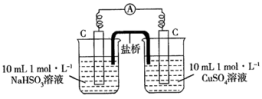 |  |
| 现象 | 电流表指针发生微小偏转 | 电流表指针发生明显偏转,_________ |
您最近一年使用:0次
2021-02-08更新
|
499次组卷
|
2卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
解答题-原理综合题
|
较难(0.4)
解题方法
10. 氮的化合物种类繁多,性质也各不相同。请回答下列问题:
(1)已知:①SO3(g)+NO(g)=NO2(g)+SO2(g)△H=+41.8kJ·mol-1,②2SO2(g)+O2(g)=2SO3(g)△H2=-196.6kJ·mol-1,则NO2(g)分解生成NO(g)和O2(g)的热化学方程式是___________ 。
(2)在恒容密闭容器中,对NO2和SO2的反应[NO2(g)+SO2(g) SO3(g)+NO(g)△H<0]进行探究,改变投料比[n(SO2):n(NO2)]进行多组实验(每组实验的温度可能相同,也可能不同),测得SO2的平衡转化率[α(SO2)]如表所示。
SO3(g)+NO(g)△H<0]进行探究,改变投料比[n(SO2):n(NO2)]进行多组实验(每组实验的温度可能相同,也可能不同),测得SO2的平衡转化率[α(SO2)]如表所示。
如果要将II组的平衡状态改变为I组的平衡状态,应采取的措施是___________ ;通过计算确定表中四组实验中温度相等的是___________ (填序号)。
(3)NOx作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g) N2(g)+CO2(g)△H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
N2(g)+CO2(g)△H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是___________ ;温度为1100K时,CO2的平衡体积分数为___________ 。
(4)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g) 3H2O(g)+2N2(g)△H<0。
3H2O(g)+2N2(g)△H<0。
①低压有利于尾气转化的原因是___________ 。
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,10min时反应达到平衡,此时NH3的转化率为40%,体系压强为p1MPa,则0~10min内用N2表示的平均反应速率v(N2)=___________ mol·L-1·min-1,500℃时该反应的平衡常数Kp=___________ MPa(用含p1的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)已知:①SO3(g)+NO(g)=NO2(g)+SO2(g)△H=+41.8kJ·mol-1,②2SO2(g)+O2(g)=2SO3(g)△H2=-196.6kJ·mol-1,则NO2(g)分解生成NO(g)和O2(g)的热化学方程式是
(2)在恒容密闭容器中,对NO2和SO2的反应[NO2(g)+SO2(g)
 SO3(g)+NO(g)△H<0]进行探究,改变投料比[n(SO2):n(NO2)]进行多组实验(每组实验的温度可能相同,也可能不同),测得SO2的平衡转化率[α(SO2)]如表所示。
SO3(g)+NO(g)△H<0]进行探究,改变投料比[n(SO2):n(NO2)]进行多组实验(每组实验的温度可能相同,也可能不同),测得SO2的平衡转化率[α(SO2)]如表所示。| 组别 | 投料比[n(SO2):n(NO2)] | SO2的平衡转化率 | 平衡常数K |
| Ⅰ | 1.0 | 0.8 | |
| Ⅱ | 1.0 | 0.5 | 1 |
| Ⅲ | 2.0 | 0.25 |  |
| Ⅳ | 3.0 | 0.25 |
(3)NOx作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:C(s)+2NO(g)
 N2(g)+CO2(g)△H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
N2(g)+CO2(g)△H<0.在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率α(NO)随温度的变化如图所示:
图中a、b、c三点中,达到平衡的点是
(4)现代技术用氨气将汽车尾气中的NOx还原为N2和H2O,反应原理是NO(g)+NO2(g)+2NH3(g)
 3H2O(g)+2N2(g)△H<0。
3H2O(g)+2N2(g)△H<0。①低压有利于尾气转化的原因是
②500℃时,在2L恒容密闭容器中充入1molNO、1molNO2和2molNH3,10min时反应达到平衡,此时NH3的转化率为40%,体系压强为p1MPa,则0~10min内用N2表示的平均反应速率v(N2)=
您最近一年使用:0次
11. 铜是人类最早使用的金属之一,铜的使用对早期人类文明的进步影响深远。按要求回答下列问题。
(1)基态Cu与Cu2+中未成对电子数之比为___________ 。
(2)白铜是铜镍合金,呈银白色,有金属光泽,白铜中存在的化学键是___________ ;元素铜与镍的第二电离能分别为I(Cu)=1958kJ·mol-1、I(Ni)=1753kJ·mol-1,I(Cu)>I(Ni)的原因是铜的核电荷数较大,且___________ 。
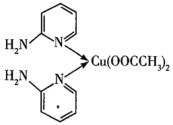
(3)某含铜配合物的结构简式如图所示,其中Cu2+的配位数是___________ ,C原子的杂化类型为___________ ;C、N、O三种元素的简单氢化物中能形成氢键的是___________ (填化学式)。
(4)两种或两种以上的金属元素在一定条件下以它们原子数的整数比相结合而成的化合物,通常叫金属互化物。
①金属互化物ZnCu中所有金属原子均按面心立方最密堆积,若所有Cu原子均位于晶胞的面心,则Zn原子位于晶胞的___________ 。
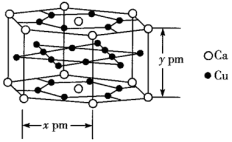
②一种Ca、Cu形成的金属互化物的晶体结构如图所示,设阿伏加德罗常数的值为NA,则该金属互化物的密度是___________ g·cm-3(列出表达式即可)。
(1)基态Cu与Cu2+中未成对电子数之比为
(2)白铜是铜镍合金,呈银白色,有金属光泽,白铜中存在的化学键是
(3)某含铜配合物的结构简式如图所示,其中Cu2+的配位数是

(4)两种或两种以上的金属元素在一定条件下以它们原子数的整数比相结合而成的化合物,通常叫金属互化物。
①金属互化物ZnCu中所有金属原子均按面心立方最密堆积,若所有Cu原子均位于晶胞的面心,则Zn原子位于晶胞的
②一种Ca、Cu形成的金属互化物的晶体结构如图所示,设阿伏加德罗常数的值为NA,则该金属互化物的密度是

您最近一年使用:0次
2021-02-08更新
|
449次组卷
|
4卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
河南省天一大联考2021届高三上学期期末考试化学试题山东省济南市莱芜第一中学2021届高三下学期2月校内检测化学试题(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)河南省南阳市第一中学校2022届高三上学期第一次月考化学试题
解答题-有机推断题
|
较难(0.4)
名校
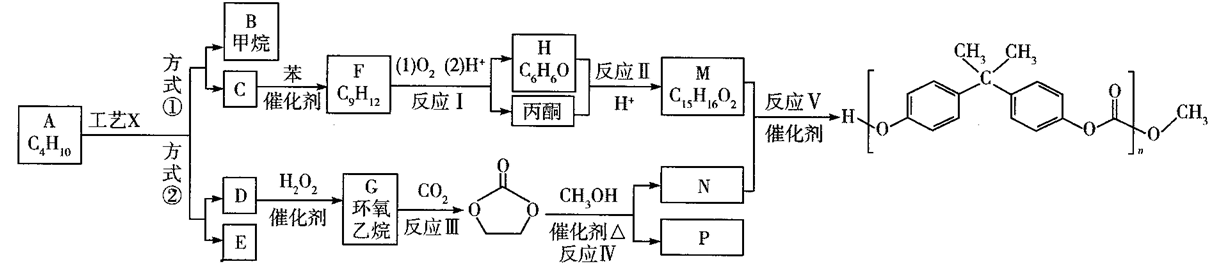
12. 由于聚碳酸酯结构的特殊性,芳香族聚碳酸酯已成为五大工程塑料中增长速度最快的通用工程塑料。某芳香族聚碳酸酯的合成路线如下:
已知:①RCOOR1+R2OH RCOOR2+R1OH
RCOOR2+R1OH
②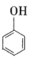 +
+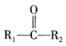

 +H2O
+H2O
(1)工艺X的名称为___________ ,有机物E的名称是___________ 。
(2)C到F的反应类型为___________ ;有机物P的结构简式是___________ 。
(3)反应V的化学方程式为___________ 。
(4)有机物W的相对分子质量是D的三倍,且二者的最简式相同,满足下列条件的W的同分异构体的结构简式是___________ 。
①分子中含有甲基
②核磁共振氢谱显示有2组峰
(5)已知:①2-COOH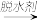
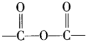 +H2O;
+H2O;
②内酯型酚酞(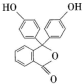 )在pH<0时可转变为
)在pH<0时可转变为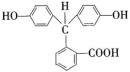 。写出以邻二甲苯和苯酚为原料合成
。写出以邻二甲苯和苯酚为原料合成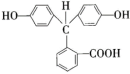 的合成路线:
的合成路线:___________ (无机试剂任选)。

已知:①RCOOR1+R2OH
 RCOOR2+R1OH
RCOOR2+R1OH②
 +
+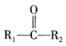

 +H2O
+H2O(1)工艺X的名称为
(2)C到F的反应类型为
(3)反应V的化学方程式为
(4)有机物W的相对分子质量是D的三倍,且二者的最简式相同,满足下列条件的W的同分异构体的结构简式是
①分子中含有甲基
②核磁共振氢谱显示有2组峰
(5)已知:①2-COOH
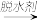
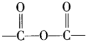 +H2O;
+H2O;②内酯型酚酞(
 )在pH<0时可转变为
)在pH<0时可转变为 。写出以邻二甲苯和苯酚为原料合成
。写出以邻二甲苯和苯酚为原料合成 的合成路线:
的合成路线:【知识点】 根据要求书写同分异构体解读 有机推断综合考查解读 信息给予的有机合成
您最近一年使用:0次
2021-02-08更新
|
489次组卷
|
4卷引用:河南省天一大联考2021届高三上学期期末考试化学试题
河南省天一大联考2021届高三上学期期末考试化学试题(已下线)培优05 有机合成基础训练-2021年高考化学大题培优练(新高考地区专用)河南省南阳市第一中学校2022届高三上学期第一次月考化学试题(已下线)大题10 有机化学基础(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、化学实验基础、化学反应原理、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 硅的物理性质与用途 蛋白质 化学科学对人类文明发展的意义 化学对材料制造和应用的作用 | |
| 2 | 0.65 | 浓硫酸的强氧化性 物质性质实验方案的设计 | |
| 3 | 0.65 | 乙烯分子构型的理解及延伸 醇类与金属单质的反应 有机化学基础知识综合考查 | |
| 4 | 0.65 | 影响化学反应速率的因素 催化剂对化学反应速率的影响 化学反应条件的控制及优化 信息给予的有机合成 | |
| 5 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 共价键概念及判断 | |
| 6 | 0.4 | 原电池电极反应式书写 燃料电池 新型电池 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.4 | 酸碱中和滴定的综合考查 盐的水解常数 | |
| 二、解答题 | |||
| 8 | 0.4 | 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 9 | 0.4 | 氧化亚铜 化学实验探究 亚硫酸及其盐 | 实验探究题 |
| 10 | 0.4 | 化学反应原理综合考查 盖斯定律与热化学方程式 化学平衡的有关计算 化学平衡常数的有关计算 | 原理综合题 |
| 11 | 0.4 | 原子核外电子的排布 利用杂化轨道理论判断化学键杂化类型 配合物的应用 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 根据要求书写同分异构体 有机推断综合考查 信息给予的有机合成 | 有机推断题 |



