22. Ⅰ.已知反应:①101 kPa时,2C(s)+O
2(g)=2CO(g) Δ
H=-221kJ·mol
-1②稀溶液中,H
+(aq)+OH
-(aq)=H
2O(l) Δ
H=-57.3kJ·mol
-1下列结论中正确的是
_________。
A.碳的燃烧热等于110.5kJ·mol
-1B.①的反应热为221kJ·mol
-1C.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ·mol
-1D.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量
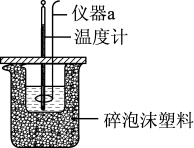
Ⅱ.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50mL 0.50mol·L
-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL 0.55mol·L
-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)仪器a的名称是
_____________________。
(2)反应过程中NaOH溶液的浓度为0.55mol·L
-1,不能使用0.50mol·L
-1 NaOH的原因是
_________________。
(3)倒入NaOH和盐酸溶液的正确操作是
___________(填字母)。
A.沿玻璃棒缓慢倒入
B.分三次倒入
C.一次迅速倒入
D.一边搅拌一边一次滴入
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol·L
-1的稀盐酸恰好完全反应,其反应热分别为Δ
H1、Δ
H2、Δ
H3,则Δ
H1、Δ
H2、Δ
H3的大小关系为
____________。
(5)用Ba(OH)
2溶液和硫酸代替氢氧化钠溶液和盐酸所测中和热的数值并不相等,从它们的离子方程式分析,所测中和热的数值并不相等的理由是
____________________。