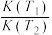甲醛(HCHO)俗称蚁醛,在化工、医药、农药等方面有广泛的应用。
I·甲醛的制备
工业上利用甲醇脱氢法制备甲醛,已知:CH3OH(g) HCHO(g)+H2(g) △H
HCHO(g)+H2(g) △H
(1)该反应的能量变化如图甲所示,△H=___ kJ•mol-1。

(2)为提高CH3OH转化率,采取的措施有___ 、___ ;在温恒容条件下,该反应达到平衡状态的标志有___ (填标号)。
a.混合气体的密度保持不变
b.混合气体的总压强保持不变
c.v(CH3OH)消耗=v(H2)生成
d.甲醛的浓度保持不变
(3)选用Ag/SiO2—ZnO作催化剂,在400~750℃区间进行活性评价,图乙给出了甲醇转化率与甲醛选择性(选择性越大,表示生成该物质越多)随反应温度的变化曲线。制备甲醛的最佳反应温度为___ (填标号),理由是___ 。
a.400℃b.650℃c.700℃d.750℃

(4)T℃时,在2L恒容密闭容器中充入1mol甲醇,发生反应:
①CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
②CH3OH(g) CO(g)+2H2(g)
CO(g)+2H2(g)
平衡时甲醇为0.2mol,甲醛为0.7mol。则反应i的平衡常数K=___ 。
II.甲醛的用途
(5)将甲醛水溶液与硫酸镍(NiSO4)溶液混合,可用于化学镀镍。反应过程中有CO2产生,则该反应的离子方程式为___ :若收集到112mLCO2(标准状况),理论上转移电子___ mol。
I·甲醛的制备
工业上利用甲醇脱氢法制备甲醛,已知:CH3OH(g)
 HCHO(g)+H2(g) △H
HCHO(g)+H2(g) △H(1)该反应的能量变化如图甲所示,△H=

(2)为提高CH3OH转化率,采取的措施有
a.混合气体的密度保持不变
b.混合气体的总压强保持不变
c.v(CH3OH)消耗=v(H2)生成
d.甲醛的浓度保持不变
(3)选用Ag/SiO2—ZnO作催化剂,在400~750℃区间进行活性评价,图乙给出了甲醇转化率与甲醛选择性(选择性越大,表示生成该物质越多)随反应温度的变化曲线。制备甲醛的最佳反应温度为
a.400℃b.650℃c.700℃d.750℃

(4)T℃时,在2L恒容密闭容器中充入1mol甲醇,发生反应:
①CH3OH(g)
 HCHO(g)+H2(g)
HCHO(g)+H2(g)②CH3OH(g)
 CO(g)+2H2(g)
CO(g)+2H2(g)平衡时甲醇为0.2mol,甲醛为0.7mol。则反应i的平衡常数K=
II.甲醛的用途
(5)将甲醛水溶液与硫酸镍(NiSO4)溶液混合,可用于化学镀镍。反应过程中有CO2产生,则该反应的离子方程式为
更新时间:2020-04-22 12:43:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________ H2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________ (填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
标注。
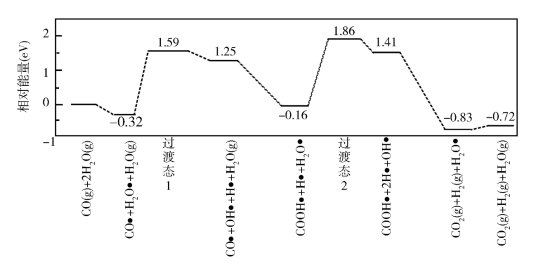
可知水煤气变换的ΔH________ 0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________ eV,写出该步骤的化学方程式_______________________ 。
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。
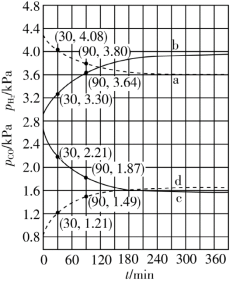
计算曲线a的反应在30~90 min内的平均速率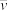 (a)=
(a)=___________ kPa·min−1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________ 、___________ 。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________ 、___________ 。
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用
 标注。
标注。
可知水煤气变换的ΔH
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。

计算曲线a的反应在30~90 min内的平均速率
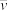 (a)=
(a)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】五种短周期主族元素的部分信息如下表所示:

(1)E在元素周期表中的位置是____________________ 。
(2)在BDC溶液中滴加酚酞溶液,溶液先变红后褪色,原因是__________________ (用离子方程式表示)。
(3)25℃时,pH均为10的BCA溶液和B2E溶液中,水电离出的c(OH-)之比为____________ 。
(4)下列事实中,能说明D的非金属性比E强的是________ (填字母)。
a.D的简单氢化物比E的稳定 b.AD的酸性比A2E的强
c.D的单质的沸点低于E的单质 d.D2与A2E能发生置换反应
(5)500℃时,向容积为1L的恒容密闭容器中充入2mol EC3气体,在催化剂作用下发生反应,经过10min恰好达到平衡,测得平衡浓度c(C2)=0.75mol·L-1。
①反应从开始到平衡时的平均反应速率v(EC2)=____________ 。
②EC3的平衡转化率为____________ 。
③其他条件不变,再向容器中充入少量EC3气体,则EC3的平衡转化率会________ (填“增大”“减小”或“不变”)。
(6)在B2E2C3溶液中滴加BAEC4溶液,会析出黄色沉淀并逸出刺激性气体,反应的离子方程式为____________________________________ 。

(1)E在元素周期表中的位置是
(2)在BDC溶液中滴加酚酞溶液,溶液先变红后褪色,原因是
(3)25℃时,pH均为10的BCA溶液和B2E溶液中,水电离出的c(OH-)之比为
(4)下列事实中,能说明D的非金属性比E强的是
a.D的简单氢化物比E的稳定 b.AD的酸性比A2E的强
c.D的单质的沸点低于E的单质 d.D2与A2E能发生置换反应
(5)500℃时,向容积为1L的恒容密闭容器中充入2mol EC3气体,在催化剂作用下发生反应,经过10min恰好达到平衡,测得平衡浓度c(C2)=0.75mol·L-1。
①反应从开始到平衡时的平均反应速率v(EC2)=
②EC3的平衡转化率为
③其他条件不变,再向容器中充入少量EC3气体,则EC3的平衡转化率会
(6)在B2E2C3溶液中滴加BAEC4溶液,会析出黄色沉淀并逸出刺激性气体,反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=___ 。
(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
①已知上述反应中相关的化学键键能数据如下:
则该反应的ΔH=___ 。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___ (填“A”或“B”)。
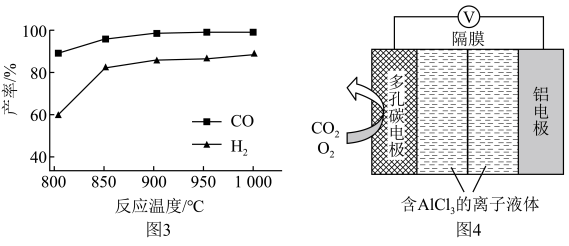
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是___ 。
(3)O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
电池的正极反应式:6O2+6e−=6O2− 6CO2+6O2−=3C2O42−+6O2
反应过程中O2的作用是___ 。该电池的总反应式:___ 。
(1)CO2可以被NaOH溶液捕获。若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=
(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)①已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图3所示。此反应优选温度为900℃的原因是

(3)O2辅助的Al~CO2电池工作原理如图4所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
电池的正极反应式:6O2+6e−=6O2− 6CO2+6O2−=3C2O42−+6O2
反应过程中O2的作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氨是一种重要的化工原料和极具前景的能源载体,实现在温和条件下氨的高效合成是催化领域的重要研究课题,工业合成氨原理:N2(g)+3H2(g) 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。
(1)合成氨实际生产中,常用催化剂为铁触媒,反应温度773K、压强20~50MPa,升高温度对N2、H2的平衡转化率的影响是_______ (填“增大”“减小”或“不变”)。选择较高反应温度773K的主要依据是下列中的_______ (填标号,双选)。
A.温度对平衡转化率的影响 B.温度对反应速率的影响
C.温度对催化剂活性的影响 D.能耗对生产成本的影响
(2)氨的催化合成在LaCoSi催化作用的化学吸附及初步表面反应历程如下:

注:方框内包含微粒种类及微粒的相对总能量,TS表示过渡态,*表示吸附态。
①请表示出N2变为吸附态的过程:_______ →_______ ;
②以上历程须克服的最大能垒为_______ eV。
(3)新型催化剂Ba2RuH6在温和条件下可以合成NH3,向密闭容器中充入5 mol N2和15 mol H2,在该温和条件下合成NH3,相同时间内测得体系中N2的物质的量(mol)与温度、压强的关系如图所示。

①P_______ (填“>”、“<”或“=”)1.6MPa。
②投料比一定时,随着温度升高,在相同温度不同压强下N2的物质的量趋向相等,其主要原因是_______ 。
③平衡时,NH3净速率方程式为:
k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数):α为常数,工业上以Ba2RuH6为催化剂时,α=0.5。由Q点数据计算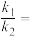
_______ MPa−2(保留两位小数)。
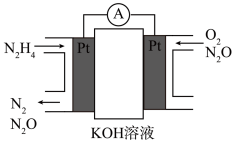
(4)纳米金表面电催化合成NH3的过程中,有副产物N2H4(l)生成,N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为_______ 。
 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。(1)合成氨实际生产中,常用催化剂为铁触媒,反应温度773K、压强20~50MPa,升高温度对N2、H2的平衡转化率的影响是
A.温度对平衡转化率的影响 B.温度对反应速率的影响
C.温度对催化剂活性的影响 D.能耗对生产成本的影响
(2)氨的催化合成在LaCoSi催化作用的化学吸附及初步表面反应历程如下:

注:方框内包含微粒种类及微粒的相对总能量,TS表示过渡态,*表示吸附态。
①请表示出N2变为吸附态的过程:
②以上历程须克服的最大能垒为
(3)新型催化剂Ba2RuH6在温和条件下可以合成NH3,向密闭容器中充入5 mol N2和15 mol H2,在该温和条件下合成NH3,相同时间内测得体系中N2的物质的量(mol)与温度、压强的关系如图所示。

①P
②投料比一定时,随着温度升高,在相同温度不同压强下N2的物质的量趋向相等,其主要原因是
③平衡时,NH3净速率方程式为:

k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数):α为常数,工业上以Ba2RuH6为催化剂时,α=0.5。由Q点数据计算
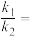
(4)纳米金表面电催化合成NH3的过程中,有副产物N2H4(l)生成,N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)研究 之间的转化具有重要意义,下图能表示
之间的转化具有重要意义,下图能表示 之间转化历程。
之间转化历程。

①写出图中所表示的总反应的热化学方程式_______ 。
②上述总反应的决速步骤的活化能是_______ (填写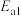 或
或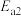 )。
)。
(2) 与
与 在高温下发生反应:
在高温下发生反应: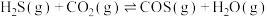
 。在610K时,将0.1mol
。在610K时,将0.1mol  与0.3mol
与0.3mol  充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
①能判断该反应达到化学平衡状态的依据是_______ 。
A.容器中压强不变 B.容器中 的物质的量分数不变
的物质的量分数不变
C. D.容器中混合气体的密度不变
D.容器中混合气体的密度不变
②反应平衡常数K的表达式为_______ , 的平衡转化率α=
的平衡转化率α=_______ 。
③要增大该反应的平衡常数K,可采取的措施是_______ 。
(1)研究
 之间的转化具有重要意义,下图能表示
之间的转化具有重要意义,下图能表示 之间转化历程。
之间转化历程。
①写出图中所表示的总反应的热化学方程式
②上述总反应的决速步骤的活化能是
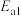 或
或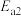 )。
)。(2)
 与
与 在高温下发生反应:
在高温下发生反应: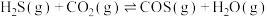
 。在610K时,将0.1mol
。在610K时,将0.1mol  与0.3mol
与0.3mol  充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。
充入2.5L的空钢瓶中(体积不变),经过10min,反应达到平衡,反应平衡时水蒸气的物质的量分数为0.125。①能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.容器中
 的物质的量分数不变
的物质的量分数不变C.
 D.容器中混合气体的密度不变
D.容器中混合气体的密度不变②反应平衡常数K的表达式为
 的平衡转化率α=
的平衡转化率α=③要增大该反应的平衡常数K,可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】工业合成氨反应具有非常重要的意义。
(1)已知: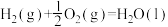


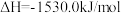
则合成氨反应的热化学方程式为___________ 。
(2)在某容积为2L的恒容容器中发生合成氨反应,体系中各物质浓度随时间变化的曲线如图所示:
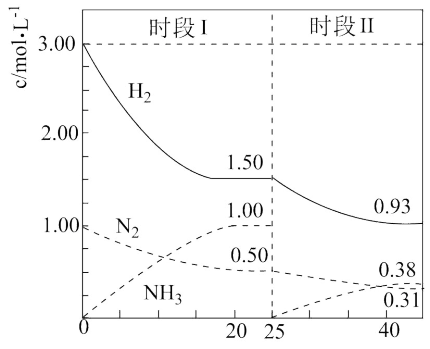
前20min内
___________  ,放出的热量为
,放出的热量为___________ ,25min时采取的措施是___________ 。
(3)对可逆反应 ,若起始投料
,若起始投料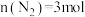 、
、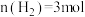 ,达到平衡后,增大压强,
,达到平衡后,增大压强, 的体积分数
的体积分数___________ (填“增大”“减小”或“不变”)
(4)T℃,以 和
和 为原料可合成化肥尿素:
为原料可合成化肥尿素: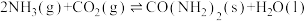 ;在2L的密闭容器中,通入1.2mol
;在2L的密闭容器中,通入1.2mol 和0.6mol
和0.6mol ,2min时反应刚好达到平衡。此时,
,2min时反应刚好达到平衡。此时, ,
, 。
。
①该反应的平衡常数是___________ 。
②若2min时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入0.6mol ,则此时平衡
,则此时平衡___________ (填“正向移动”“逆向移动”或“不移动”)
(1)已知:
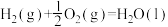


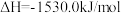
则合成氨反应的热化学方程式为
(2)在某容积为2L的恒容容器中发生合成氨反应,体系中各物质浓度随时间变化的曲线如图所示:

前20min内

 ,放出的热量为
,放出的热量为(3)对可逆反应
 ,若起始投料
,若起始投料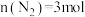 、
、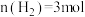 ,达到平衡后,增大压强,
,达到平衡后,增大压强, 的体积分数
的体积分数(4)T℃,以
 和
和 为原料可合成化肥尿素:
为原料可合成化肥尿素: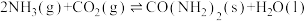 ;在2L的密闭容器中,通入1.2mol
;在2L的密闭容器中,通入1.2mol 和0.6mol
和0.6mol ,2min时反应刚好达到平衡。此时,
,2min时反应刚好达到平衡。此时, ,
, 。
。①该反应的平衡常数是
②若2min时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入0.6mol
 ,则此时平衡
,则此时平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业制硫酸中的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和O2,在催化剂、500℃的条件下发生反应。SO2与SO3的物质的量随时间变化的曲线如图所示,请回答下列问题。

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是_______ ;表示SO3的物质的量随时间变化的曲线是_______ (填相应的字母编号)。
(2)由图象可知SO2与O2的反应是可逆反应,证据是_______ 。
(3)下列说法不正确的是_______ 。
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是_______ 。
a.单位时间内消耗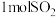 ,同时生成
,同时生成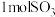
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是
(2)由图象可知SO2与O2的反应是可逆反应,证据是
(3)下列说法不正确的是
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是
a.单位时间内消耗
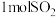 ,同时生成
,同时生成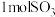
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮气分子在催化剂作用下发生的一系列转化如下:

反应①属于工业固氮,为可逆反应。反应②可用于工业制硝酸。完成下列填空:
(1)氮原子的核外电子排布式是___________ ,氧原子最外层有_____ 种运动状态不同的电子。反应②的化学反应方程式是_____ 。
(2)为模拟反应①,T℃时,在2L恒容密闭容器中加入2molN2和2molH2,其中n(NH3)随时间的变化见图。

氮气在前2分钟内的平均反应速率v(N2)=______ mol/(L·min),达平衡时N2和H2的浓度之比为____ 。
(3)能说明上题所述反应在T℃下已达平衡状态的是_________ (选填序号)。
A.混合气体的密度不再变化
B.3v正(H2)=2v逆(NH3)
C.容器内的总压强不再变化
D.各物质的浓度相等
E.氮气物质的量不再变化
请提出一条既能提高氢气的转化率,又能加快反应速率的措施______________ 。
(4)一氧化二氮俗名笑气,250℃时硝酸铵固体在密闭容器中加热分解可得N2O和H2O,该可逆反应的平衡常数表达式为________ 。

反应①属于工业固氮,为可逆反应。反应②可用于工业制硝酸。完成下列填空:
(1)氮原子的核外电子排布式是
(2)为模拟反应①,T℃时,在2L恒容密闭容器中加入2molN2和2molH2,其中n(NH3)随时间的变化见图。

氮气在前2分钟内的平均反应速率v(N2)=
(3)能说明上题所述反应在T℃下已达平衡状态的是
A.混合气体的密度不再变化
B.3v正(H2)=2v逆(NH3)
C.容器内的总压强不再变化
D.各物质的浓度相等
E.氮气物质的量不再变化
请提出一条既能提高氢气的转化率,又能加快反应速率的措施
(4)一氧化二氮俗名笑气,250℃时硝酸铵固体在密闭容器中加热分解可得N2O和H2O,该可逆反应的平衡常数表达式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为探讨化学平衡移动原理与氧化还原反应规律的联系,重庆八中某化学兴趣小组成员通过改变浓度研究反应“2Fe3++2I- 2Fe2++I2” 中Fe3+和Fe2+的相互转化,实验设计如图:
2Fe2++I2” 中Fe3+和Fe2+的相互转化,实验设计如图:
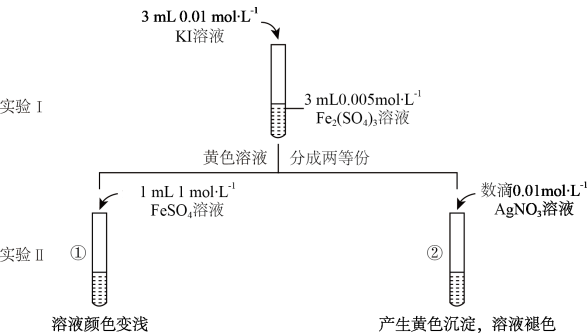
回答下列问题:
(1)待实验I溶液颜色不再改变时,再进行实验II,其目的是确保实验I的反应达到_______ 。
(2)甲同学认为实验II—①中现象产生的原因是c(Fe2+)增大,平衡逆向移动。但乙同学认为此实验不能排除溶液稀释对颜色造成的影响,应增加一个对照实验,即另取等量的黄色溶液,加入_______ ,若______ (填实验现象),则能排除溶液稀释对颜色造成的影响。
(3)实验II—②中产生黄色沉淀的离子方程式为_______ ,用平衡移动原理解释实验II—②中溶液褪色的原因:_______ 。
(4)丙同学推测实验II-②中Fe2+向Fe3+转化的 原因是外加Ag+使c(I-)下降,导致I-的还原性弱于Fe2+,于是设计了如图所示的装置,验证了这一结论。
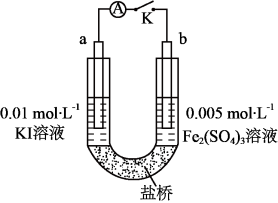
①当K闭合时,电流计指针右偏,此时b极发生的电极反应方程式为_______ 。
②电流计指针归零后,向U形管左侧滴加0.01 mol·L-1AgNO3溶液,产生黄色沉淀,同时_______ (填实验现象)后证实了丙同学的推测。
(5)按照(4)的原理,丙同学又用同样的装置证实了实验II-①中Fe2+向Fe3+转化的原因是外加Fe2+使c(Fe3+)增大,导致Fe2+的还原性强于I-。结合实验I、II,对比(2)—(4)和(5),你能得出的结论是_______ 。
 2Fe2++I2” 中Fe3+和Fe2+的相互转化,实验设计如图:
2Fe2++I2” 中Fe3+和Fe2+的相互转化,实验设计如图: 
回答下列问题:
(1)待实验I溶液颜色不再改变时,再进行实验II,其目的是确保实验I的反应达到
(2)甲同学认为实验II—①中现象产生的原因是c(Fe2+)增大,平衡逆向移动。但乙同学认为此实验不能排除溶液稀释对颜色造成的影响,应增加一个对照实验,即另取等量的黄色溶液,加入
(3)实验II—②中产生黄色沉淀的离子方程式为
(4)丙同学推测实验II-②中Fe2+向Fe3+转化的 原因是外加Ag+使c(I-)下降,导致I-的还原性弱于Fe2+,于是设计了如图所示的装置,验证了这一结论。

①当K闭合时,电流计指针右偏,此时b极发生的电极反应方程式为
②电流计指针归零后,向U形管左侧滴加0.01 mol·L-1AgNO3溶液,产生黄色沉淀,同时
(5)按照(4)的原理,丙同学又用同样的装置证实了实验II-①中Fe2+向Fe3+转化的原因是外加Fe2+使c(Fe3+)增大,导致Fe2+的还原性强于I-。结合实验I、II,对比(2)—(4)和(5),你能得出的结论是
您最近一年使用:0次
【推荐1】溴是一种重要的化工原料,回答下列问题:
I. 地球上99%的溴元素存在于海水中,海水提溴是最有效的制备方法。
(1)溴元素在元素周期表中的位置为___________ 。
(2)在获得低浓度的溴水后,可用空气吹出溴单质并用亚硫酸溶液吸收,所得浓溶液用于后续步骤,则吸收过程中发生反应的离子方程式为___________ 。
II.一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加成反应(1,2-加成和1,4-加成),体系中同时存在如下反应:
①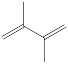 +Br2 →
+Br2 → 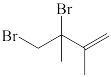 ΔH1
ΔH1
②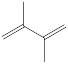 +Br2 →
+Br2 → 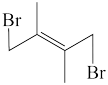 ΔH2
ΔH2
③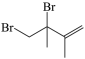

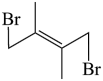 ΔH3
ΔH3
已知体系中两种产物可通过中间产物 互相转化,反应历程及能量变化如图所示:
互相转化,反应历程及能量变化如图所示:
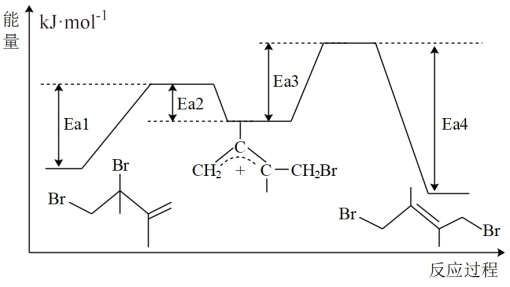
(3)由反应历程及能量变化图示判断,ΔH1___________ ΔH2(填“>”、“=”或“<”)。
(4)由反应历程及能量变化图示判断,产物中_____ 含量更大。
III. 溴化氢可以与苯乙烯发生加成反应,其产物有两种,其反应的化学方程式如下:
i.C6H5-CH=CH2(g)+HBr(g) C6H5-CH2CH2Br(g)
C6H5-CH2CH2Br(g)
ii.C6H5-CH=CH2(g)+HBr(g) C6H5-CHBrCH3(g)
C6H5-CHBrCH3(g)
在600℃条件下,向容积为3L的恒容密闭容器中充入1.2molC6H5-CH=CH2(g)和1.2molHBr(g)发生反应,达到平衡时C6H5-CH2CH2Br(g)和C6H5-CHBrCH3(g)的物质的量 随时间
随时间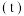 变化的曲线如图所示。
变化的曲线如图所示。
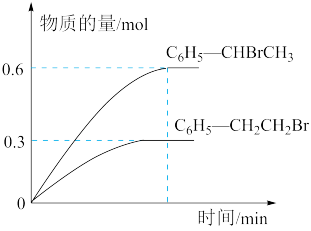
(5)600℃时,反应ii的化学平衡常数
_____ 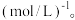
(6)反应平衡后,若保持其他条件不变,向该容器中再充入1molC6H5-CH2CH2Br(g),则反应ii将___________ (填“正向”“逆向”或“不”)移动。
(7)在恒温恒容的密闭容器中,苯乙烯与溴化氢发生i、ii两个加成反应,可以判断反应已达到平衡状态的是___________ (填编号)。
I. 地球上99%的溴元素存在于海水中,海水提溴是最有效的制备方法。
(1)溴元素在元素周期表中的位置为
(2)在获得低浓度的溴水后,可用空气吹出溴单质并用亚硫酸溶液吸收,所得浓溶液用于后续步骤,则吸收过程中发生反应的离子方程式为
II.一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加成反应(1,2-加成和1,4-加成),体系中同时存在如下反应:
①
 +Br2 →
+Br2 →  ΔH1
ΔH1②
 +Br2 →
+Br2 →  ΔH2
ΔH2③


 ΔH3
ΔH3已知体系中两种产物可通过中间产物
 互相转化,反应历程及能量变化如图所示:
互相转化,反应历程及能量变化如图所示:
(3)由反应历程及能量变化图示判断,ΔH1
(4)由反应历程及能量变化图示判断,产物中
III. 溴化氢可以与苯乙烯发生加成反应,其产物有两种,其反应的化学方程式如下:
i.C6H5-CH=CH2(g)+HBr(g)
 C6H5-CH2CH2Br(g)
C6H5-CH2CH2Br(g)ii.C6H5-CH=CH2(g)+HBr(g)
 C6H5-CHBrCH3(g)
C6H5-CHBrCH3(g)在600℃条件下,向容积为3L的恒容密闭容器中充入1.2molC6H5-CH=CH2(g)和1.2molHBr(g)发生反应,达到平衡时C6H5-CH2CH2Br(g)和C6H5-CHBrCH3(g)的物质的量
 随时间
随时间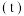 变化的曲线如图所示。
变化的曲线如图所示。
(5)600℃时,反应ii的化学平衡常数

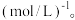
(6)反应平衡后,若保持其他条件不变,向该容器中再充入1molC6H5-CH2CH2Br(g),则反应ii将
(7)在恒温恒容的密闭容器中,苯乙烯与溴化氢发生i、ii两个加成反应,可以判断反应已达到平衡状态的是___________ (填编号)。
| A.容器内混合气体的密度不再改变 |
| B.C6H5-CH2CH2Br(g)的生成速率与C6H5-CHBrCH3(g)的分解速率相等 |
| C.反应器中压强不再随时间变化而变化 |
| D.混合气体的平均相对分子质量保持不变 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】CO、 加氢可合成甲醇
加氢可合成甲醇 和乙醇
和乙醇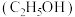 ,实现“碳中和”。该体系主要涉及以下反应:
,实现“碳中和”。该体系主要涉及以下反应:
反应Ⅰ: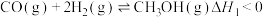
反应Ⅱ: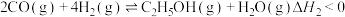
反应Ⅲ:
反应Ⅳ: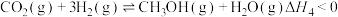
反应Ⅴ: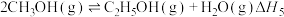
(1)上述反应中,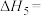
______ (写出一个代数式即可)。
(2)密闭容器中,上述反应体系达平衡状态后,下列描述正确的有______ (填标号)。
a.加入催化剂,可提高 的平衡转化率
的平衡转化率
b.降低温度,反应V的正反应速率增大,逆反应速率减小
c.恒温恒容充入 ,反应Ⅰ、Ⅱ的平衡均向左移动
,反应Ⅰ、Ⅱ的平衡均向左移动
d.恒温恒容充入氩气,反应Ⅰ、Ⅱ的平衡不移动
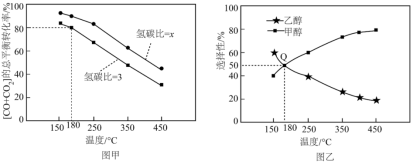
(3)恒容下,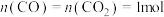 ,并按照不同氢碳比
,并按照不同氢碳比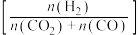 投料,发生上述反应。图甲表示不同氢碳比时,
投料,发生上述反应。图甲表示不同氢碳比时,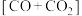 的总平衡转化率随温度变化的关系;图乙表示氢碳比
的总平衡转化率随温度变化的关系;图乙表示氢碳比 时,平衡后体系中
时,平衡后体系中 、
、 的选择性随温度变化的关系。
的选择性随温度变化的关系。
已知: 的选择性
的选择性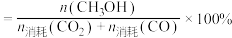 ;
;
 的选择性
的选择性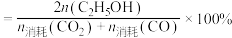
______ 3(填“>、<或=”),其原因是______ 。
②Q点对应的体系中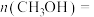
______ mol;此时, 转化了4mol,则反应
转化了4mol,则反应 的平衡常数
的平衡常数
______ 。( 为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)
为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)
(4)已知: ,其中R、C均为大于0的常数。反应Ⅰ和反应Ⅱ在不同温度(
,其中R、C均为大于0的常数。反应Ⅰ和反应Ⅱ在不同温度( 、
、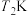 )下的平衡常数之比如下表:
)下的平衡常数之比如下表:
则
______  (填“>、<或=”,下同),
(填“>、<或=”,下同),
______  。
。
 加氢可合成甲醇
加氢可合成甲醇 和乙醇
和乙醇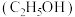 ,实现“碳中和”。该体系主要涉及以下反应:
,实现“碳中和”。该体系主要涉及以下反应:反应Ⅰ:
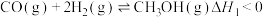
反应Ⅱ:
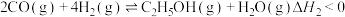
反应Ⅲ:

反应Ⅳ:
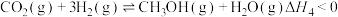
反应Ⅴ:
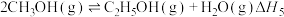
(1)上述反应中,
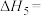
(2)密闭容器中,上述反应体系达平衡状态后,下列描述正确的有
a.加入催化剂,可提高
 的平衡转化率
的平衡转化率b.降低温度,反应V的正反应速率增大,逆反应速率减小
c.恒温恒容充入
 ,反应Ⅰ、Ⅱ的平衡均向左移动
,反应Ⅰ、Ⅱ的平衡均向左移动d.恒温恒容充入氩气,反应Ⅰ、Ⅱ的平衡不移动
(3)恒容下,
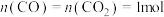 ,并按照不同氢碳比
,并按照不同氢碳比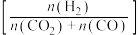 投料,发生上述反应。图甲表示不同氢碳比时,
投料,发生上述反应。图甲表示不同氢碳比时,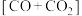 的总平衡转化率随温度变化的关系;图乙表示氢碳比
的总平衡转化率随温度变化的关系;图乙表示氢碳比 时,平衡后体系中
时,平衡后体系中 、
、 的选择性随温度变化的关系。
的选择性随温度变化的关系。已知:
 的选择性
的选择性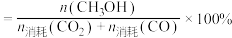 ;
; 的选择性
的选择性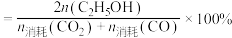
②Q点对应的体系中
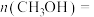
 转化了4mol,则反应
转化了4mol,则反应 的平衡常数
的平衡常数
 为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)
为以分压表示的平衡常数,分压=总压×物质的量分数,结果保留两位有效数字)(4)已知:
 ,其中R、C均为大于0的常数。反应Ⅰ和反应Ⅱ在不同温度(
,其中R、C均为大于0的常数。反应Ⅰ和反应Ⅱ在不同温度( 、
、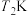 )下的平衡常数之比如下表:
)下的平衡常数之比如下表:
| |
反应Ⅰ | 0.8 |
反应Ⅱ | 0.75 |

 (填“>、<或=”,下同),
(填“>、<或=”,下同),
 。
。
您最近一年使用:0次
【推荐3】做好碳达峰、碳中和工作,是中央经济工作会议确定的2021年八项重点任务之一、CO2的资源化可以推动经济高质量发展和生态环境质量的持续改善。
(1)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1: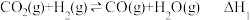
反应2:
反应3: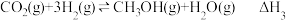
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。则△H2___________ △H3 (填“大于”、“小于”或“等于”)。
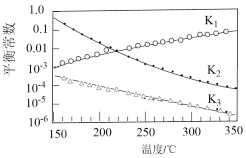
(2)①对于上述CO2加氢合成CH3OH的体系,下列说法错误的是___________ (填标号)。
A.增大H2浓度有利于提高CO2的转化率
B.当气体的平均相对分子质量保持不变时,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应1平衡不移动,反应3平衡正向移动
D.选用合适的催化剂可以提高CH3OH在单位时间内的产量
②已知对于反应: ,其标准平衡常数:
,其标准平衡常数: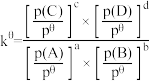 ,某温度为T,压强为
,某温度为T,压强为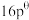 的恒压密闭容器中,通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol(b>a),此时H2O(g)的分压p(H2O)=
的恒压密闭容器中,通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol(b>a),此时H2O(g)的分压p(H2O)=___________ (用含a、b的代数式表示,下同),反应1的标准平衡常数为___________ 。
(3)电催化还原能将CO2转化为多种碳产物。在铜电极上将CO2还原为CO的机理如图所示:
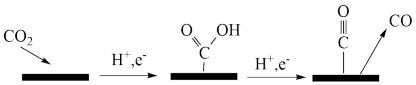
写出该机理过程总的电极方程式:___________ 。
(4)利用CO2为原料可以合成苯乙烯,涉及以下反应:
I.
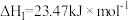
II.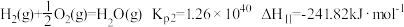
结合数据说明乙苯制苯乙烯过程中加氧气的理由___________ 。
(1)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:
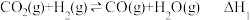
反应2:

反应3:
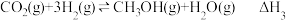
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。则△H2

(2)①对于上述CO2加氢合成CH3OH的体系,下列说法错误的是
A.增大H2浓度有利于提高CO2的转化率
B.当气体的平均相对分子质量保持不变时,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应1平衡不移动,反应3平衡正向移动
D.选用合适的催化剂可以提高CH3OH在单位时间内的产量
②已知对于反应:
 ,其标准平衡常数:
,其标准平衡常数: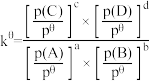 ,某温度为T,压强为
,某温度为T,压强为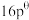 的恒压密闭容器中,通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol(b>a),此时H2O(g)的分压p(H2O)=
的恒压密闭容器中,通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为a mol,CO为b mol(b>a),此时H2O(g)的分压p(H2O)=(3)电催化还原能将CO2转化为多种碳产物。在铜电极上将CO2还原为CO的机理如图所示:

写出该机理过程总的电极方程式:
(4)利用CO2为原料可以合成苯乙烯,涉及以下反应:
I.

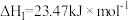
II.
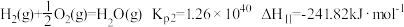
结合数据说明乙苯制苯乙烯过程中加氧气的理由
您最近一年使用:0次