已知反应式:mX(g)+nY(?) pQ (g)+2mZ(g),达到平衡时c( X) =0.3 mol• L-1。其他条件不变,将容器体积缩小到原来的
pQ (g)+2mZ(g),达到平衡时c( X) =0.3 mol• L-1。其他条件不变,将容器体积缩小到原来的 ,重新平衡后c(X) =0.5 mol• L-1。下列说法正确的是
,重新平衡后c(X) =0.5 mol• L-1。下列说法正确的是
 pQ (g)+2mZ(g),达到平衡时c( X) =0.3 mol• L-1。其他条件不变,将容器体积缩小到原来的
pQ (g)+2mZ(g),达到平衡时c( X) =0.3 mol• L-1。其他条件不变,将容器体积缩小到原来的 ,重新平衡后c(X) =0.5 mol• L-1。下列说法正确的是
,重新平衡后c(X) =0.5 mol• L-1。下列说法正确的是| A.平衡逆方向移动 | B.Y 可能是固体 |
| C.系数n>m | D.Z 的体积分数减小 |
2020·浙江金华·模拟预测 查看更多[3]
浙江省金华十校2020届高三4月模拟考试化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古自治区呼伦贝尔市鄂温克族自治旗第三中学2021-2022学年高二上学期第一次月考化学试题
更新时间:2020/05/16 19:11:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】向一恒容密闭容器中加入 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比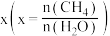 温度的变化曲线如图所示。下列说法不正确的是
温度的变化曲线如图所示。下列说法不正确的是
 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
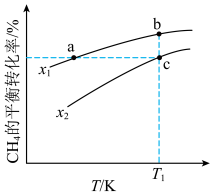
的平衡转化率按不同投料比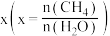 温度的变化曲线如图所示。下列说法不正确的是
温度的变化曲线如图所示。下列说法不正确的是
A.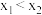 |
B. 两点的正反应速率: 两点的正反应速率: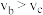 |
| C.此反应在任意温度下都可自发进行 |
| D.当容器内气体的平均相对分子质量不变时,反应达平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】实验室为了保存液溴常加水形成水封。仔细观察储存液溴的试剂瓶中分成了上、中、下三相,如图所示。下列说法错误的是


| A.不用橡胶塞的原因之一是防止橡胶被溴单质氧化 |
| B.瓶中气体压强较初始时增大 |
C.饱和溴水相中存在平衡: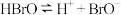 |
| D.深红棕色液溴相中存在大量的共价键和离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
下列说法中错误的是
 4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:
4NO2(g)+O2(g) △H>0。一定温度时,向密闭容器中通入N2O5,部分实验数据见表:| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
| A.500s时O2的浓度为0.075mol/L |
| B.平衡后,升高温度,逆反应速率增大 |
| C.平衡后,要使平衡常数减小,改变的条件是降低温度 |
| D.1000s时将容器的体积缩小一半,重新达到平衡时0.25mol/L<c(N2O5)<0.50mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】人体内的血红蛋白(Hb)可与O2结合形成HbO2,Hb(aq)也可以与CO结合,人体发生CO中毒的原理为:HbO2(aq)+CO(g) HbCO(aq)+O2(g) ΔH<0.下列说法
HbCO(aq)+O2(g) ΔH<0.下列说法不正确 的是
 HbCO(aq)+O2(g) ΔH<0.下列说法
HbCO(aq)+O2(g) ΔH<0.下列说法| A.海拔较高的地区由于气压较低,所以血红蛋白较难与O2结合,容易产生缺氧现象 |
| B.已知CO中毒为熵减过程,则理论上冬天比夏天可能更容易发生CO中毒现象 |
| C.把CO中毒的人转到高压氧仓中有助于缓解症状 |
D.此反应的平衡常数K=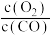 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】100 ℃时,向容积为2 L的密闭容器中充入一定量的X气体,发生如下反应:X(g)+2Y(g) Z(g),反应过程中测定的部分数据见下表:下列说法正确的是
Z(g),反应过程中测定的部分数据见下表:下列说法正确的是
 Z(g),反应过程中测定的部分数据见下表:下列说法正确的是
Z(g),反应过程中测定的部分数据见下表:下列说法正确的是| 反应时间/min | n(X)/mol | n(Y)/mol |
| 0 | 2.00 | 2.40 |
| 10 | 1.00 | |
| 30 | 0.40 |
| A.温度为200 ℃时,上述反应平衡常数为20,则正反应为吸热反应 |
| B.若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)>1 mol/L |
| C.保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大 |
| D.保持其他条件不变,若再向容器中通入0.10 mol X气体,0.10 mol Y和0.10 mol Z,则v(正)<v(逆) |
您最近一年使用:0次

 2NH3(g)的 ΔH < 0,ΔS >0
2NH3(g)的 ΔH < 0,ΔS >0 N2O4(g)体系,压缩体积,再达平衡时气体颜色比原平衡的深
N2O4(g)体系,压缩体积,再达平衡时气体颜色比原平衡的深

