过碳酸钠(2Na2CO3·3H2O2)晶体性质具有Na2CO3和H2O2 的双重性,被广泛用于氧气发生、漂白杀菌、污水处理、金属表面处理以及高分子聚合控制等。
(1)Na 原子的核外电子排布式为_____ ,O 原子核外 L 层上有_______ 种能量不同的电子,H2O2 的电子式是_____________________________________________
(2)设计一个简单实验,比较O 元素与其同主族短周期元素的非金属性强弱(简要写出实验方法、实验现象和结论)_____ ;并用原子结构知识对作出的结论进行解释_____ 。
(3)用一个离子方程式表示过碳酸钠溶液显碱性的原因________________________ 。
(4)高锰酸根离子( )水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:
)水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:
_____ +_______CO
+_______CO +___H2O2→___MnCO3+___□+____OH-+____H2O
+___H2O2→___MnCO3+___□+____OH-+____H2O
补全并配平上述化学反应过程式_____ ;反应中,过碳酸钠起沉淀剂和_________ 剂作用;若将 1L 含Mn 2000mg·L-1 的含高锰酸根离子的废水处理至含Mn 1.2mg·L-1,则转移电子数为_____ mol(保留 2 位小数)
(1)Na 原子的核外电子排布式为
(2)设计一个简单实验,比较O 元素与其同主族短周期元素的非金属性强弱(简要写出实验方法、实验现象和结论)
(3)用一个离子方程式表示过碳酸钠溶液显碱性的原因
(4)高锰酸根离子(
 )水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:
)水对人体危害极大,可用过碳酸钠改性赤泥进行处理,反应如下:_____
 +_______CO
+_______CO +___H2O2→___MnCO3+___□+____OH-+____H2O
+___H2O2→___MnCO3+___□+____OH-+____H2O补全并配平上述化学反应过程式
更新时间:2020-06-11 22:30:31
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】焦亚硫酸钠 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 .在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
.在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
(1)利用烟道气中的 生产
生产 的工艺流程如图:
的工艺流程如图:
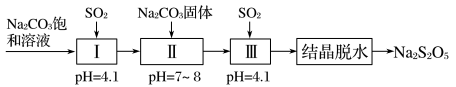
资料:当 溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
①焦亚硫酸钠中硫元素的化合价为_______ ,常温下焦亚硫酸钠溶于水形成的溶液显_______ 性(填“酸”、“中”或“碱”)。
②控制Ⅰ中反应结束的方法是测定溶液的pH,当 时停止通入
时停止通入 ,此时溶液的溶质主要是
,此时溶液的溶质主要是_______ (填物质名称)。
③Ⅲ中发生反应的化学方程式有_______ 。
(2)研究表明,焦亚硫酸钠处理含铬(VI)废水较其他方法效果好,处理费用低。其工艺流程如图:
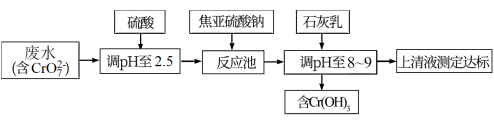
①加硫酸调废水pH至2.5,可增强 的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因
的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因_______ 。
②石灰乳的作用为_______ 。
 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 .在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
.在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。(1)利用烟道气中的
 生产
生产 的工艺流程如图:
的工艺流程如图:
资料:当
 溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。①焦亚硫酸钠中硫元素的化合价为
②控制Ⅰ中反应结束的方法是测定溶液的pH,当
 时停止通入
时停止通入 ,此时溶液的溶质主要是
,此时溶液的溶质主要是③Ⅲ中发生反应的化学方程式有
(2)研究表明,焦亚硫酸钠处理含铬(VI)废水较其他方法效果好,处理费用低。其工艺流程如图:

①加硫酸调废水pH至2.5,可增强
 的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因
的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因②石灰乳的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Cl2常用作自来水消毒剂,Cl2作消毒剂时生成的有机氯化物可能对人体有害。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。某小组探究“地康法制氯气”的原理并验证Cl2的性质,设计实验如下(夹持装置略去)。请回答下列问题:

(1)A装置中反应利用了浓硫酸的难挥发性,则该反应的化学方程式为______________ 。
(2)当B装置中反应转移0.08 mol电子时,则消耗的Na2O2固体的质量为______________ 。
(3)反应开始后,硫酸铜变蓝,则装置D中发生反应的化学方程式为______________ 。
(4)ClO2的制备方法比较实用的有数十种,下列方法是常见方法之一。
方法一:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。当有0.4 mol电子发生转移时,得到的还原产物为______________ mol。
方法二:实验室常用氯酸钾(KClO3)、草酸(H2C2O4)和硫酸溶液共热制备。
有同学设计如下装置制备ClO2并用其处理含锰离子的工业废水。

①C装置的作用为______________ 。
②B中反应产物有ClO2、CO2等, 发生氧化反应的过程为:______________ → ______________ (用化学式表示)。______________
③写出装置D中除去Mn2+ (已知Mn2+转化为MnO2)的离子方程式:______________ 。

(1)A装置中反应利用了浓硫酸的难挥发性,则该反应的化学方程式为
(2)当B装置中反应转移0.08 mol电子时,则消耗的Na2O2固体的质量为
(3)反应开始后,硫酸铜变蓝,则装置D中发生反应的化学方程式为
(4)ClO2的制备方法比较实用的有数十种,下列方法是常见方法之一。
方法一:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。当有0.4 mol电子发生转移时,得到的还原产物为
方法二:实验室常用氯酸钾(KClO3)、草酸(H2C2O4)和硫酸溶液共热制备。
有同学设计如下装置制备ClO2并用其处理含锰离子的工业废水。

①C装置的作用为
②B中反应产物有ClO2、CO2等, 发生氧化反应的过程为:______________ → ______________ (用化学式表示)。
③写出装置D中除去Mn2+ (已知Mn2+转化为MnO2)的离子方程式:
您最近一年使用:0次
【推荐3】马日夫盐[Mn(H2PO4)2·H2O]主要用作磷化剂。以软锰矿(主要成分为MnO2及少量的FeO、Al2O3和SiO2)为原料制备马日夫盐的主要工艺流程如图:

(1)按照无机物命名规律,马日夫盐[Mn(H2PO4)2·2H2O]的化学名称为______ 。在反应中,Mn2+若再失去一个电子比Fe2+再失去一个电子难,从原子结构解释其原因_______ 。
(2)“浸锰”过程中主要反应的离子方程式为_______ 。滤渣X主要成分为_________ 。检验“沉锰”已完成的实验操作及现象是_________ 。步骤五产生马日夫盐晶体的化学方程式为_________ 。
(3)Fe3+的萃取率与溶液的pH和接触时间之间的关系如图,据此分析,萃取的最佳条件为__________ 。

(4)马日夫盐作防锈磷化剂的原因是利用其较强的酸性以及在防锈处理过程中生成了具有保护作用的FeHPO4,马日夫盐显酸性的主要原因是__________ (用相关化学用语回答)。

(1)按照无机物命名规律,马日夫盐[Mn(H2PO4)2·2H2O]的化学名称为
(2)“浸锰”过程中主要反应的离子方程式为
(3)Fe3+的萃取率与溶液的pH和接触时间之间的关系如图,据此分析,萃取的最佳条件为

(4)马日夫盐作防锈磷化剂的原因是利用其较强的酸性以及在防锈处理过程中生成了具有保护作用的FeHPO4,马日夫盐显酸性的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用;NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。回答下列问题:
(1)NH4Al(SO4)2可用作做净水剂的原因是________ (用离子方程式表示)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH )
)________ 0.1 mol·L-1NH4HSO4中c(NH )。(填“>”“<”或“=”)
)。(填“>”“<”或“=”)
(3)图所示是0.1 mol·L-1电解质溶液的pH随温度变化的图象。图中符合0.1 mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是________ (填序号);20 ℃时,0.1 mol·L-1 NH4Al(SO4)2溶液中2 c(SO )-c(NH
)-c(NH )-3 c(Al3+)=
)-3 c(Al3+)=_____ mol·L-1。

(4)若液氨中也存在类似水的电离(H2O+H2O⇌H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
①液氨的电离方程式为________ 。
②碳酸钠的液氨溶液中各离子浓度的大小关系为_____ 。
(1)NH4Al(SO4)2可用作做净水剂的原因是
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH
 )
) )。(填“>”“<”或“=”)
)。(填“>”“<”或“=”)(3)图所示是0.1 mol·L-1电解质溶液的pH随温度变化的图象。图中符合0.1 mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是
 )-c(NH
)-c(NH )-3 c(Al3+)=
)-3 c(Al3+)=
(4)若液氨中也存在类似水的电离(H2O+H2O⇌H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
①液氨的电离方程式为
②碳酸钠的液氨溶液中各离子浓度的大小关系为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化亚铜(CuCl)是用途广泛的化工产品,其露置于空气中易被氧化。某兴趣小组高温加热分解氯化铜晶体(CuCl2·xH2O)制备CuCl,其装置如图(加热仪器、夹持仪器省略):
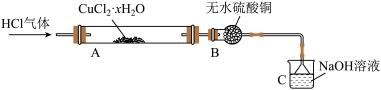
回答下列问题:
(1)通入HCl气体的作用是_______ 。
(2)硬质玻璃管A中主要发生反应的化学方程式为_______ 。

回答下列问题:
(1)通入HCl气体的作用是
(2)硬质玻璃管A中主要发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某萃铜余液主要含有 、
、 、
、 、
、 ,
, 等离子,从萃铜余液中回收金属和制备
等离子,从萃铜余液中回收金属和制备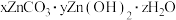 的工艺流程如甲图所示。
的工艺流程如甲图所示。

回答下列问题:
(1)过硫酸钠( )中S的化合价为+6,
)中S的化合价为+6,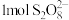 中过氧键的数目为
中过氧键的数目为_______ 。
(2)向 的萃铜余液中加入
的萃铜余液中加入 。进行“氧化除锰”,其反应的离子方程式为
。进行“氧化除锰”,其反应的离子方程式为_______ 。“氧化除锰”过程中,
_______ (填“能”或“不能”)用绿色氧化剂 来代替。
来代替。
(3)向“氧化除锰”后的余液中加入试剂X调节 使铁元素完全沉淀,试剂X的化学式为
使铁元素完全沉淀,试剂X的化学式为_______ 。
(4)“沉锌”时,应保持溶液 在6.8~7.0之间,
在6.8~7.0之间, 不能过低的原因是
不能过低的原因是_______ 。
(5)“过滤”时,经常采用抽滤的方式加快过滤的速度。实验室用如图乙所示的装置,经过一系列操作完成抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→c→_______→_______→_______→c→关抽气泵。_______

a.转移固液混合物 b.关活塞A c.开活塞A d.确认抽干 e.加洗涤剂洗涤
(6)用 溶液浸泡法将
溶液浸泡法将 转化为
转化为 ,若不考虑
,若不考虑 水解,要使4.66g
水解,要使4.66g 恰好完全转化为
恰好完全转化为 ,至少需要浓度为
,至少需要浓度为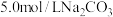 溶液
溶液_______  。(已知
。(已知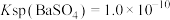 ,
,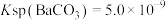 )
)
 、
、 、
、 、
、 ,
, 等离子,从萃铜余液中回收金属和制备
等离子,从萃铜余液中回收金属和制备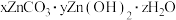 的工艺流程如甲图所示。
的工艺流程如甲图所示。
回答下列问题:
(1)过硫酸钠(
 )中S的化合价为+6,
)中S的化合价为+6,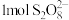 中过氧键的数目为
中过氧键的数目为(2)向
 的萃铜余液中加入
的萃铜余液中加入 。进行“氧化除锰”,其反应的离子方程式为
。进行“氧化除锰”,其反应的离子方程式为
 来代替。
来代替。(3)向“氧化除锰”后的余液中加入试剂X调节
 使铁元素完全沉淀,试剂X的化学式为
使铁元素完全沉淀,试剂X的化学式为(4)“沉锌”时,应保持溶液
 在6.8~7.0之间,
在6.8~7.0之间, 不能过低的原因是
不能过低的原因是(5)“过滤”时,经常采用抽滤的方式加快过滤的速度。实验室用如图乙所示的装置,经过一系列操作完成抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→c→_______→_______→_______→c→关抽气泵。

a.转移固液混合物 b.关活塞A c.开活塞A d.确认抽干 e.加洗涤剂洗涤
(6)用
 溶液浸泡法将
溶液浸泡法将 转化为
转化为 ,若不考虑
,若不考虑 水解,要使4.66g
水解,要使4.66g 恰好完全转化为
恰好完全转化为 ,至少需要浓度为
,至少需要浓度为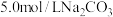 溶液
溶液 。(已知
。(已知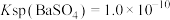 ,
,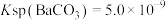 )
)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1869年,俄国化学家门捷列夫制作了第一张元素周期表。下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

(1)c元素的符号是_______ ,短周期元素中,元素_______ 原子半径最大。
(2)请写出元素g,h,i中氢化物稳定性最强的元素在元素周期表中所在的位置_______ 。
(3)请画出元素f的简单离子结构示意图_______ 。请写出单质f与d的最高价氧化物对应水化物反应的化学方程式_______ 。
(4)元素i的单质制备漂白粉的离子方程式_______ 。
(5)元素d和c构成的化合物中,有一种淡黄色物质具有强氧化性,其结构中含有的化学键类型为_______ ,电子式_______ ,该化合物和 反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ 。

(1)c元素的符号是
(2)请写出元素g,h,i中氢化物稳定性最强的元素在元素周期表中所在的位置
(3)请画出元素f的简单离子结构示意图
(4)元素i的单质制备漂白粉的离子方程式
(5)元素d和c构成的化合物中,有一种淡黄色物质具有强氧化性,其结构中含有的化学键类型为
 反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求答题。
①X、Y、Z、W、Q是四种短周期元素,X元素某原子中含中子数和质子数相等,均为8;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的简单氢化物水溶液呈碱性;W元素最高正价与最低负价之和为6;Q是地壳中含量最高的金属元素。回答下列问题:
(1)X元素在元素周期表中的位置_______ 。能够作为示踪原子的核素符号为______ 。
(2)由Y和W形成的化合物的电子式_______ 。
(3)Y、Z、W的最高价氧化物的水化物的酸性由强到弱的顺序_______ 。(用化学式表达顺序)
(4)写出Q的工业制备方法(以化学方程式表示)_______ 。
②二甲醚是一种清洁能源,用水煤气制取二甲醚的原理如下:
I、CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
II、2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
(5)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3),则反应I的平衡常数K=_______ 。
①X、Y、Z、W、Q是四种短周期元素,X元素某原子中含中子数和质子数相等,均为8;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的简单氢化物水溶液呈碱性;W元素最高正价与最低负价之和为6;Q是地壳中含量最高的金属元素。回答下列问题:
(1)X元素在元素周期表中的位置
(2)由Y和W形成的化合物的电子式
(3)Y、Z、W的最高价氧化物的水化物的酸性由强到弱的顺序
(4)写出Q的工业制备方法(以化学方程式表示)
②二甲醚是一种清洁能源,用水煤气制取二甲醚的原理如下:
I、CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)II、2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)(5)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3),则反应I的平衡常数K=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】氮的价类二维图如下。回答下列问题:

(1)从氮元素的价态角度分析,物质B具有___________ 性。
(2) 是生产黑火药的原料之一,其爆炸反应为:
是生产黑火药的原料之一,其爆炸反应为: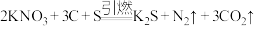 。该反应中非金属元素的原子半径从小到大的顺序是
。该反应中非金属元素的原子半径从小到大的顺序是___________ ,标准状况下,生成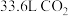 时,转移电子的数目为
时,转移电子的数目为___________ 。
(3)在催化剂和加热的条件下,物质A与 反应生成NO是工业制物质C的重要反应,其化学方程式为
反应生成NO是工业制物质C的重要反应,其化学方程式为___________ 。
(4)下列事实能证明碳元素与氮元素非金属性相对强弱的有___________(填标号)。
(5)对工业尾气中NO和 脱除后产生的含
脱除后产生的含 溶液可用下图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用下图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为___________ ,若甲室处理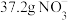 ,则乙室可生成
,则乙室可生成___________ 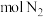 。
。


(1)从氮元素的价态角度分析,物质B具有
(2)
 是生产黑火药的原料之一,其爆炸反应为:
是生产黑火药的原料之一,其爆炸反应为: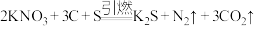 。该反应中非金属元素的原子半径从小到大的顺序是
。该反应中非金属元素的原子半径从小到大的顺序是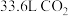 时,转移电子的数目为
时,转移电子的数目为(3)在催化剂和加热的条件下,物质A与
 反应生成NO是工业制物质C的重要反应,其化学方程式为
反应生成NO是工业制物质C的重要反应,其化学方程式为(4)下列事实能证明碳元素与氮元素非金属性相对强弱的有___________(填标号)。
A.单质熔点: | B.酸性: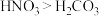 |
C.沸点: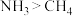 | D.分解温度: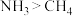 |
 脱除后产生的含
脱除后产生的含 溶液可用下图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用下图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为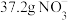 ,则乙室可生成
,则乙室可生成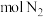 。
。
您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D的阳离子与B中阴离子具有相同的电子层结构,D的化合价为+1,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1,请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为_______ 。
(2)用电子排布图表示F元素原子的价电子构型_______ 。
(3)F、G元素的最高价含氧酸中酸性较强的分子式为_______ 。
(4)离子半径:D+_______ B3-,第一电离能:B_______ C,电负性:C_______ F(填“<”“>”或“=”)
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为_______ ,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式_______ 。
(6)写出E与D的最高价氧化物对应的水化物反应的化学方程式_______ 。
(1)E元素基态原子电子排布式为
(2)用电子排布图表示F元素原子的价电子构型
(3)F、G元素的最高价含氧酸中酸性较强的分子式为
(4)离子半径:D+
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(6)写出E与D的最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
【推荐2】2022年珠海航展成功举办,歼20战机和C919国产大飞机等大国重器悉数亮相,世界瞩目。金属材料和复合材料在航空航天工业中具有重要的应用。回答下列问题:
(1)金属铼(Re)是生产航空发动机叶片必不可少的材料。NH4ReO4在高温下用H2还原可制得金属铼,反应的化学方程式为_____ 。
(2)硬铝中含Mg、Si等合金元素,因其密度小、强度高且耐腐蚀,常用于制造飞机的外壳。
①基态Al原子核外电子的空间运动状态有____ 种。
②Mg、Al、Si的第一电离能由大到小的顺序为____ 。
③AlCl3易与Cl-形成配离子AlCl ,AlCl
,AlCl 的空间构型为
的空间构型为____ ,其中Al的杂化轨道类型为____ 。写出与AlCl 原子总数和价电子总数均相等的一种等电子体的分子式
原子总数和价电子总数均相等的一种等电子体的分子式____ 。
(3)以SiC为连续基体的碳陶瓷是一种复合材料,可用于制造歼20的刹车片。
①SiC的熔点比晶体Si____ (填“高”或“低”),原因是____ 。
②某碳族元素参与形成的三元化合物晶胞示意图如图,该化合物的化学式为____ 。

(1)金属铼(Re)是生产航空发动机叶片必不可少的材料。NH4ReO4在高温下用H2还原可制得金属铼,反应的化学方程式为
(2)硬铝中含Mg、Si等合金元素,因其密度小、强度高且耐腐蚀,常用于制造飞机的外壳。
①基态Al原子核外电子的空间运动状态有
②Mg、Al、Si的第一电离能由大到小的顺序为
③AlCl3易与Cl-形成配离子AlCl
 ,AlCl
,AlCl 的空间构型为
的空间构型为 原子总数和价电子总数均相等的一种等电子体的分子式
原子总数和价电子总数均相等的一种等电子体的分子式(3)以SiC为连续基体的碳陶瓷是一种复合材料,可用于制造歼20的刹车片。
①SiC的熔点比晶体Si
②某碳族元素参与形成的三元化合物晶胞示意图如图,该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Na2PO3F作牙膏的添加剂可预防龋齿,其制备原料为NaF和H3PO4。
(1)基态F原子的价层电子排布式为___________ 。
(2)基态O原子中,电子占据的最高能层的符号是___________ ,处于最高能级的电子的运动状态共有___________ 个。
(3)两个H3PO4分子间可以通过脱水缩合生成焦磷酸:___________ (写结构简式)。
(4)Na2PO3F溶于水时与水反应,P-F键断裂,生成F-。
①PO3F2-中磷元素的化合价是___________ 价。
②该反应会形成___________ (填“P-O”或“P-H”)键。
③反应后,溶液中粒子浓度的关系:2c(F-)___________ c(Na+)(填“>”“<”或“=”)。
(5)SrF2也可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为anm。___________ 。
A.含SrF2添加剂的牙膏可以在酸性条件下保持很好的效果
B.图中黑色的球●代表Sr2+
C.每个Sr2+周围紧邻且等距离的Sr2+个数为4
D.Sr2+配位数为8
E.F-位于距其最近且等距的Sr2+构成的八面体空隙中
②该晶胞的密度为___________ g·cm-3。
(1)基态F原子的价层电子排布式为
(2)基态O原子中,电子占据的最高能层的符号是
(3)两个H3PO4分子间可以通过脱水缩合生成焦磷酸:

(4)Na2PO3F溶于水时与水反应,P-F键断裂,生成F-。
①PO3F2-中磷元素的化合价是
②该反应会形成
③反应后,溶液中粒子浓度的关系:2c(F-)
(5)SrF2也可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为anm。

A.含SrF2添加剂的牙膏可以在酸性条件下保持很好的效果
B.图中黑色的球●代表Sr2+
C.每个Sr2+周围紧邻且等距离的Sr2+个数为4
D.Sr2+配位数为8
E.F-位于距其最近且等距的Sr2+构成的八面体空隙中
②该晶胞的密度为
您最近一年使用:0次



