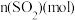在2L密闭容器内,800℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)上述反应______________ (“是”或“不是”)可逆反应。
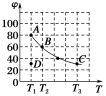
(2)如图所示表示NO2变化的曲线是___________________ ,用O2表示从0~2s内该反应的平均反应速率v(O2)=__________________ 。

(3)不能说明该反应已达到平衡状态的是________________________ 。
a.v(NO2)=2v(O2) b.容器内气体压强保持不变
c.v逆(NO)=2v正(O2) d.容器内气体的密度保持不变
 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应
(2)如图所示表示NO2变化的曲线是

(3)不能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内气体压强保持不变
c.v逆(NO)=2v正(O2) d.容器内气体的密度保持不变
更新时间:2020-09-06 15:01:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L‒1·min‒1,则以物质B表示此反应的化学反应速率为___________ 。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为___________ 。
(3)①将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有___________ mol A,此时C的物质的量浓度为___________ 。
②能说明该反应已达到平衡状态的是_______ (填字母)。
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
③在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
(4)在2 L的恒温恒容密闭容器内,某一反应中A、B气体的物质的量随时间变化的曲线如图所示,从反应开始至4 min时,B的平均反应速率为___________ ,该反应的化学方程式为___________ 。
(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L‒1·min‒1,则以物质B表示此反应的化学反应速率为
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为
(3)①将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有②能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
③在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积
(4)在2 L的恒温恒容密闭容器内,某一反应中A、B气体的物质的量随时间变化的曲线如图所示,从反应开始至4 min时,B的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】牙齿上的牙釉质主要由矿物羟基磷灰石([Ca10(PO4)6(OH)2]组成,是人体最坚硬的物质,但口腔内残留食物会发酵使口腔呈酸性,羟基磷灰石溶解导致牙齿受损,从而形成蛀牙,Ca10(PO4)6(OH)2(s)+8H+(aq) 10Ca2+(aq)+6HPO
10Ca2+(aq)+6HPO (aq)+2H2O(1)。回答下列问题:
(aq)+2H2O(1)。回答下列问题:
(1)当喝下碳酸饮料时,平衡向_____ (填“正”或“逆”)反应方向移动。
(2)牙釉质的质量(m)与反应温度(T)、pH的关系如图所示,则该反应为____ (填“放热”或“吸热”)反应,pH1_____ pH2(填“>”、“<”或“=”)。

(3)下列能说明反应达到平衡状态的是____ (填字母)。
a.各离子浓度相等
b.pH维持稳定
c.5v正(Ca2+)=3v逆(HPO )
)
d.羟基磷灰石的质量不再发生变化
(4)为模拟酸对牙釉质的影响,在一密闭容器中加入牙釉质和盐酸,经过5h后,发现溶液的pH由3变化为4,则用Ca2+的浓度变化表示的平均反应速率为____ mol/(L•h)。
(5)已知:P(s,红磷)=P(s,黑磷)ΔH=-21.7kJ•mol-1
P(s,白磷)=P(s,红磷)ΔH=-17.6kJ•mol-1
由此推知,其中最稳定的磷单质是____ 。
 10Ca2+(aq)+6HPO
10Ca2+(aq)+6HPO (aq)+2H2O(1)。回答下列问题:
(aq)+2H2O(1)。回答下列问题:(1)当喝下碳酸饮料时,平衡向
(2)牙釉质的质量(m)与反应温度(T)、pH的关系如图所示,则该反应为

(3)下列能说明反应达到平衡状态的是
a.各离子浓度相等
b.pH维持稳定
c.5v正(Ca2+)=3v逆(HPO
 )
)d.羟基磷灰石的质量不再发生变化
(4)为模拟酸对牙釉质的影响,在一密闭容器中加入牙釉质和盐酸,经过5h后,发现溶液的pH由3变化为4,则用Ca2+的浓度变化表示的平均反应速率为
(5)已知:P(s,红磷)=P(s,黑磷)ΔH=-21.7kJ•mol-1
P(s,白磷)=P(s,红磷)ΔH=-17.6kJ•mol-1
由此推知,其中最稳定的磷单质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)=2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,则
(1)用物质A表示的反应的平均速率为_________ ;
(2)2 s时物质B的转化率为_______ ;
(3)用物质B表示的反应的平均速率为_________ ;
(4)2 s时物质A的浓度为__________ 。
Ⅱ、某温度时,在一个0.5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.

根据图中数据回答下列问题:
(1)该反应的化学方程式为___________ .
(2)反应开始至2min,以气体Z表示的平均反应速率为_________ .
(3)用物质X表示的化学反应速率为0.2mol•L﹣1•s﹣1与用物质Y表示的化学反应速率为0.1mol•L﹣1•s﹣1,哪个快?___________ 。
a.前者 b.后者 c.一样快 d.无法比较
(1)用物质A表示的反应的平均速率为
(2)2 s时物质B的转化率为
(3)用物质B表示的反应的平均速率为
(4)2 s时物质A的浓度为
Ⅱ、某温度时,在一个0.5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.

根据图中数据回答下列问题:
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)用物质X表示的化学反应速率为0.2mol•L﹣1•s﹣1与用物质Y表示的化学反应速率为0.1mol•L﹣1•s﹣1,哪个快?
a.前者 b.后者 c.一样快 d.无法比较
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】肼(N2H4)与N2O4是火箭发射中最常用的燃料与助燃剂。
(1)800 ℃时,某密闭容器中存在如下反应:2NO2(g) 2NO(g)+O2(g) ΔH>0,若开始向容器中加入1 mol·L-1的NO2,反应过程中NO的产率随时间的变化如图中曲线I所示。
2NO(g)+O2(g) ΔH>0,若开始向容器中加入1 mol·L-1的NO2,反应过程中NO的产率随时间的变化如图中曲线I所示。
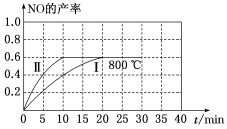
①反应II相对于反应I而言,改变的条件可能是_____ 。
②请在图中绘制出在其他条件与反应I相同,反应在820 ℃时进行,NO的产率随时间的变化曲线_____ 。
(2)已知N2O4(g) 2NO2(g) ΔH=+57.20 kJ·mol-1,开始时,将一定量的NO2、N2O4充入一个容器为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g) ΔH=+57.20 kJ·mol-1,开始时,将一定量的NO2、N2O4充入一个容器为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:
①c(X)代表___________ (填化学式)的浓度。
②前10 min内用NO2表示的反应速率为___________ ;20 min时改变的条件是___________ ;重新达到平衡时,NO2的百分含量___________ (填字母)。
a.增大 b.减小 c.不变 d.无法判断
(1)800 ℃时,某密闭容器中存在如下反应:2NO2(g)
 2NO(g)+O2(g) ΔH>0,若开始向容器中加入1 mol·L-1的NO2,反应过程中NO的产率随时间的变化如图中曲线I所示。
2NO(g)+O2(g) ΔH>0,若开始向容器中加入1 mol·L-1的NO2,反应过程中NO的产率随时间的变化如图中曲线I所示。
①反应II相对于反应I而言,改变的条件可能是
②请在图中绘制出在其他条件与反应I相同,反应在820 ℃时进行,NO的产率随时间的变化曲线
(2)已知N2O4(g)
 2NO2(g) ΔH=+57.20 kJ·mol-1,开始时,将一定量的NO2、N2O4充入一个容器为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g) ΔH=+57.20 kJ·mol-1,开始时,将一定量的NO2、N2O4充入一个容器为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol·L-1) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol·L-1) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10 min内用NO2表示的反应速率为
a.增大 b.减小 c.不变 d.无法判断
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题。
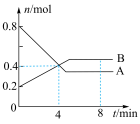
(1)某温度时,在2L容器中A、B 两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:___________ 。
②反应开始至 4 min 时,B 的平均反应速率为___________ ,A 的转化率为 ___________ 。
③平衡时,A 的物质的量为 0.2mol,B 的物质的量为 0.5mol,计算该反应的化学平衡常数___________ 。
④4 min 时,反应是否达到平衡状态?___________ (填“是”或“否”),8 min 时,v (正) ___________ v (逆) (填“>”、“<”或“=”)。
(2)下图表示在密闭容器中反应: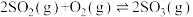
 达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时改变的条件可能是
达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时改变的条件可能是___________ 。
(1)某温度时,在2L容器中A、B 两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:
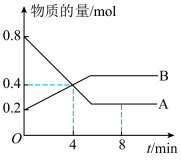
②反应开始至 4 min 时,B 的平均反应速率为
③平衡时,A 的物质的量为 0.2mol,B 的物质的量为 0.5mol,计算该反应的化学平衡常数
④4 min 时,反应是否达到平衡状态?
(2)下图表示在密闭容器中反应:
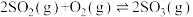
 达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时改变的条件可能是
达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a 时改变的条件可能是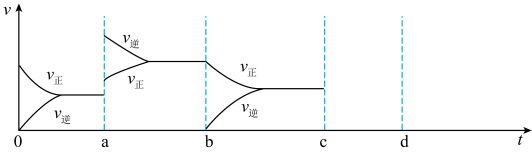
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】500℃时,在2L的密闭容器中,SO2和足量的O2在催化剂的条件下发生反应:2SO2+O2 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
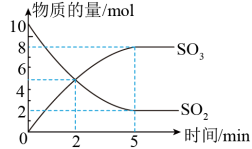
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是____ mol/(L·min)。加快反应速率的措施有____ (至少提出两条)。
(2)该反应在____ (填2或5)min达到限度。
(3)反应达到平衡状态的依据是____ 。
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:____ 。

 2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
2SO3。SO2和SO3的物质的量随时间变化的关系曲线如图所示。回答下列问题。
(1)在前5min内,以SO2的浓度变化表示的化学反应速率是
(2)该反应在
(3)反应达到平衡状态的依据是
A.单位时间内消耗1molSO2,同时生成1molSO3
B.SO2的浓度与SO3浓度相等
C.SO2的浓度与SO3浓度均不再变化
(4)用微观示意图的形式表示上述反应:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以下是反应:2SO2+O2 2SO3在不同条件下达到平衡状态时SO2的转化率。
2SO3在不同条件下达到平衡状态时SO2的转化率。
试回答下列问题。
(1)关于可逆反应的限度,你能得出什么启示?
________________________________________ 。
(2)提高该化学反应限度的途径有:_____________________ 。
(3)要实现SO2的转化率为93.5%,需控制的反应条件是____________________ 。
 2SO3在不同条件下达到平衡状态时SO2的转化率。
2SO3在不同条件下达到平衡状态时SO2的转化率。| 压强 转化率 温度 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
试回答下列问题。
(1)关于可逆反应的限度,你能得出什么启示?
(2)提高该化学反应限度的途径有:
(3)要实现SO2的转化率为93.5%,需控制的反应条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨是最重要的氮肥,是产量最大的化工产品之一。其合成原理为: N2(g)+3H2(g) 2NH3(g) ΔH= - 92.4 kJ·mol-1。
2NH3(g) ΔH= - 92.4 kJ·mol-1。
I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应。
(1)测得反应放出的热量_________ 92.4kJ(填“小于”,“大于”或“等于”)。
(2)当反应达到平衡时,N2和H2的浓度比是_________ ;N2和H2的转化率比是___________ 。
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量____ 。(填“变大”、“变小”或“不变”)
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将____ (填“正向”、“逆向”或“不”)移动。
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。
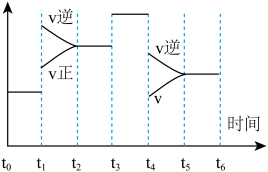
(5)t1时刻,体系中发生变化的条件是_______ 。
A.增大压强B.升高温度C.减小压强D.降低温度 E.加入正催化剂
(6)下列时间段中,氨的百分含量最高的是_______ 。
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
 2NH3(g) ΔH= - 92.4 kJ·mol-1。
2NH3(g) ΔH= - 92.4 kJ·mol-1。I.在密闭容器中,投入1mol N2和3 mol H2在催化剂作用下发生反应。
(1)测得反应放出的热量
(2)当反应达到平衡时,N2和H2的浓度比是
(3)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将
II.该反应在一密闭容器中发生,下图是某一时间段反应速率与反应进程的关系曲线图。

(5)t1时刻,体系中发生变化的条件是
A.增大压强B.升高温度C.减小压强D.降低温度 E.加入正催化剂
(6)下列时间段中,氨的百分含量最高的是
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一固定容积的密闭容器中进行着如下反应: CO2(g) + H2(g)  CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
(1)K的表达式为:____ ;
(2)该反应的正反应为___ 反应(“吸热”或“放热”);
(3)下列选项中可作为该反应在850℃时已经达到化学平衡状态的标志的是:_________
A.容器中压强不再变化 B.混合气体中CO浓度不再变化
C.混合气体的密度不再变化 D.c(CO2) = c(CO)= c(H2) = c(H2O)
(4)当温度为850℃,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时上述的反应中正、逆反应速率的关系式是___________ (填代号)。
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
(5)在700℃通过压缩体积增大气体压强,则该反应中H2(g)的转化率___ (“增大”、“减小”或“不变”);工业生产中,通过此方法使容器内气体压强增大以加快反应,却意外发现H2(g)的转化率也显著提高,请你从平衡原理解释其原因________ 。
 CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1)K的表达式为:
(2)该反应的正反应为
(3)下列选项中可作为该反应在850℃时已经达到化学平衡状态的标志的是:
A.容器中压强不再变化 B.混合气体中CO浓度不再变化
C.混合气体的密度不再变化 D.c(CO2) = c(CO)= c(H2) = c(H2O)
(4)当温度为850℃,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO | H2O | CO2 | H2 |
0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时上述的反应中正、逆反应速率的关系式是
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
(5)在700℃通过压缩体积增大气体压强,则该反应中H2(g)的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】500℃时,在2L密闭容器内发生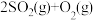 ⇌
⇌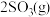 的反应,其中
的反应,其中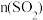 随时间的变化如下表:
随时间的变化如下表:
(1)用O2表示从0~2s内该反应的平均速率: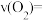
__________ 。
(2)在第5s时,SO2的转化率为__________ 。
(3)如图所示,表示SO3变化曲线的是_______ 。

(4)能说明该反应已达到平衡状态的是_____ 。
a.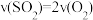
b. 混合气体中 的体积分数保持不变
的体积分数保持不变
c.v逆( )=2v正(
)=2v正( )
)
d. 容器内密度保持不变
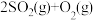 ⇌
⇌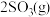 的反应,其中
的反应,其中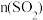 随时间的变化如下表:
随时间的变化如下表:时间( | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)用O2表示从0~2s内该反应的平均速率:
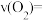
(2)在第5s时,SO2的转化率为
(3)如图所示,表示SO3变化曲线的是

(4)能说明该反应已达到平衡状态的是
a.
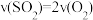
b. 混合气体中
 的体积分数保持不变
的体积分数保持不变c.v逆(
 )=2v正(
)=2v正( )
)d. 容器内密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应中的能量和速率变化对生产生活有着重要意义。某研究小组同学进行下列探究活动。
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为___________ (填“放热”或“吸热”)反应。
②下列措施中,能加快氢气生成速率的是___________ (填字母标号)。
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g) pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
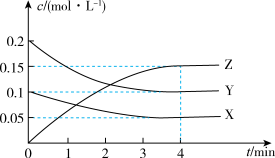
①0~4 min内的反应速率v(Z)=___________ 。
②m:n:p=___________ 。
③该反应达最大限度时Y的转化率___________ 。
④下列描述能表示该反应达平衡状态的是___________ (填字母标号)。
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
(1)甲同学探究反应2Al+3H2SO4(稀)=Al2(SO4)3+3H2↑中的能量变化。向装有铝片的试管中加入1 mol·L-1的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为
②下列措施中,能加快氢气生成速率的是
a.加CuSO4溶液 b.将稀H2SO4改成浓硫酸
c.加Na2SO4溶液 d.将铝片换成铝粉
(2)乙同学对可逆反应m X(g) +nY(g)
 pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
pZ(g)进行探究。回答下列问题: T℃时,起始向10L恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度(c)与时间(t)的关系如图所示。
①0~4 min内的反应速率v(Z)=
②m:n:p=
③该反应达最大限度时Y的转化率
④下列描述能表示该反应达平衡状态的是
A.容器中Y与Z的物质的量相等
B.容器内气体的密度不再发生改变
C.单位时间内生成n molY的同时生成pmolZ
D. X的体积分数不再改变
E.容器内气体的平均相对分子质量不随时间的变化而变化
您最近一年使用:0次

 )
)