硝酸铵是一种重要的化工原料,通常用合成氨及合成硝酸的产物进行生产
(1)已知合成氨的热化学方程式为:N2(g)+ 3H2(g) 2NH3(g) △H=-92kJ/mol,按照氮气和氢气的物质的量之比1:3的比例,分别在200℃、400℃、600℃的条件下进行反应,生成物NH3的物质的量分数随压强的变化曲线如图所示
2NH3(g) △H=-92kJ/mol,按照氮气和氢气的物质的量之比1:3的比例,分别在200℃、400℃、600℃的条件下进行反应,生成物NH3的物质的量分数随压强的变化曲线如图所示
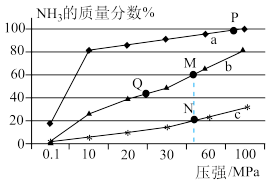
①曲线c对应的温度为___________ ℃。
②下列说法中正确的是___________ 。
A.增大氢气浓度,可促进平衡正向移动并能提高氮气的转化率
B.Q点对应的反应条件下,若加入适当的催化剂,可提高NH3在混合物中的物质的量分数
C.M、N两点的平衡常数大小关系为:M>N
D.M、N、Q三点反应速率的大小关系为:N>M>Q
(2)尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)=H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_____________________________ 。
(3)柴油汽车尾气净化器通常用尿素作为氮氧化物尾气的吸收剂,生成物均为无毒无污染的常见物质,请写出尿素与NO反应的化学方程式_______________________________________ ,当有1mol尿素完全反应时,转移电子的数目为___________ 。
(1)已知合成氨的热化学方程式为:N2(g)+ 3H2(g)
 2NH3(g) △H=-92kJ/mol,按照氮气和氢气的物质的量之比1:3的比例,分别在200℃、400℃、600℃的条件下进行反应,生成物NH3的物质的量分数随压强的变化曲线如图所示
2NH3(g) △H=-92kJ/mol,按照氮气和氢气的物质的量之比1:3的比例,分别在200℃、400℃、600℃的条件下进行反应,生成物NH3的物质的量分数随压强的变化曲线如图所示
①曲线c对应的温度为
②下列说法中正确的是
A.增大氢气浓度,可促进平衡正向移动并能提高氮气的转化率
B.Q点对应的反应条件下,若加入适当的催化剂,可提高NH3在混合物中的物质的量分数
C.M、N两点的平衡常数大小关系为:M>N
D.M、N、Q三点反应速率的大小关系为:N>M>Q
(2)尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)=H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:
(3)柴油汽车尾气净化器通常用尿素作为氮氧化物尾气的吸收剂,生成物均为无毒无污染的常见物质,请写出尿素与NO反应的化学方程式
更新时间:2020-09-15 13:47:28
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】氢能是一种极具发展潜力的清洁能源。可通过下列反应大规模制取氢气。
Ⅰ.水煤气变换反应(WGSR)
反应a:
(1)一定压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为 、
、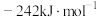 。则
。则 的摩尔生成焓的热化学方程式为
的摩尔生成焓的热化学方程式为_______ 。
(2)实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H₂的体积分数。对比实验的结果如下图所示。投入CaO时, 的体积分数增大的原因为
的体积分数增大的原因为_______ 。投入纳米CaO装置的氢气产率更高,其原因为_______ 。 可用于生产
可用于生产 ,实现
,实现 的资源化,其电极反应式为
的资源化,其电极反应式为_______ 。生成 的电极应连接电源的
的电极应连接电源的_______ 极(选填“正”或“负”)。
Ⅱ.甲烷干重整(DRM)
DRM的主要反应为:
反应b:
反应c:
该过程中会逐渐生成积碳覆盖在催化剂 表面,使催化剂中毒。
表面,使催化剂中毒。
(4)甲烷和二氧化碳的起始物质的量均为1mol,实验测得在0.1MPa下,平衡时各组分的量随温度变化如下图所示。已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 。625°C时反应c的压强平衡常数
。625°C时反应c的压强平衡常数 为
为_______ 。 改性,使其形成氧空位,可减少积碳。
改性,使其形成氧空位,可减少积碳。 晶胞如下图所示。取干燥
晶胞如下图所示。取干燥 在Ar气条件下加热,热重分析显示样品一直处于质量损失状态;X射线衍射分析结果表明随着温度升高,该晶胞边长变长,但铈离子空间排列没有发生变化。加热后,当失重率(损失的质量/总质量)为2.32%时,每个晶胞拥有的
在Ar气条件下加热,热重分析显示样品一直处于质量损失状态;X射线衍射分析结果表明随着温度升高,该晶胞边长变长,但铈离子空间排列没有发生变化。加热后,当失重率(损失的质量/总质量)为2.32%时,每个晶胞拥有的 的个数为
的个数为_______ 。
Ⅰ.水煤气变换反应(WGSR)
反应a:

(1)一定压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓。已知
 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为 、
、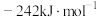 。则
。则 的摩尔生成焓的热化学方程式为
的摩尔生成焓的热化学方程式为(2)实验发现,其他条件不变,在相同时间内,向上述体系中投入一定量的CaO可以增大H₂的体积分数。对比实验的结果如下图所示。投入CaO时,
 的体积分数增大的原因为
的体积分数增大的原因为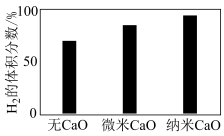
 可用于生产
可用于生产 ,实现
,实现 的资源化,其电极反应式为
的资源化,其电极反应式为 的电极应连接电源的
的电极应连接电源的Ⅱ.甲烷干重整(DRM)
DRM的主要反应为:
反应b:

反应c:

该过程中会逐渐生成积碳覆盖在催化剂
 表面,使催化剂中毒。
表面,使催化剂中毒。(4)甲烷和二氧化碳的起始物质的量均为1mol,实验测得在0.1MPa下,平衡时各组分的量随温度变化如下图所示。已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 。625°C时反应c的压强平衡常数
。625°C时反应c的压强平衡常数 为
为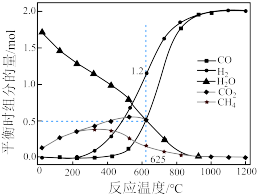
 改性,使其形成氧空位,可减少积碳。
改性,使其形成氧空位,可减少积碳。 晶胞如下图所示。取干燥
晶胞如下图所示。取干燥 在Ar气条件下加热,热重分析显示样品一直处于质量损失状态;X射线衍射分析结果表明随着温度升高,该晶胞边长变长,但铈离子空间排列没有发生变化。加热后,当失重率(损失的质量/总质量)为2.32%时,每个晶胞拥有的
在Ar气条件下加热,热重分析显示样品一直处于质量损失状态;X射线衍射分析结果表明随着温度升高,该晶胞边长变长,但铈离子空间排列没有发生变化。加热后,当失重率(损失的质量/总质量)为2.32%时,每个晶胞拥有的 的个数为
的个数为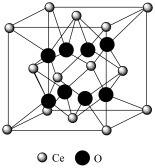
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】能源是国民经济发展的重要基础,如何合理利用现有能源以及开发新能源一直是研究的重点课题。
(1)在25 ℃、101 kPa时,8g CH4完全燃烧生成液态水时放出的热量是445.0 kJ。在直接以甲烷为燃料电池时,电解质溶液为酸性,负极的反应式为____________________ 。理想状态下,该燃料电池消耗1 mol甲烷所能产生的最大电能为756.5 kJ,则该燃料电池的理论效率(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)为________ 。
(2)将煤转化为水煤气的方法是通过化学高温方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要反应为 。有关物质的燃烧热数据如下表所示:
。有关物质的燃烧热数据如下表所示:
已知: 转化为
转化为 放出44.0 kJ的热量。
放出44.0 kJ的热量。
①写出C完全燃烧的热化学方程式:___________________________________ 。
②相同条件下,相同体积的氢气与一氧化碳完全燃烧,放出热量较多的是________ 。
③写出煤转化为水煤气的主要反应的热化学方程式:______________________ 。
(1)在25 ℃、101 kPa时,8g CH4完全燃烧生成液态水时放出的热量是445.0 kJ。在直接以甲烷为燃料电池时,电解质溶液为酸性,负极的反应式为
(2)将煤转化为水煤气的方法是通过化学高温方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要反应为
 。有关物质的燃烧热数据如下表所示:
。有关物质的燃烧热数据如下表所示:| 物质 | C | H2 | CO |
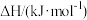 | -393.5 | -285.8 | -283.0 |
已知:
 转化为
转化为 放出44.0 kJ的热量。
放出44.0 kJ的热量。①写出C完全燃烧的热化学方程式:
②相同条件下,相同体积的氢气与一氧化碳完全燃烧,放出热量较多的是
③写出煤转化为水煤气的主要反应的热化学方程式:
您最近一年使用:0次
【推荐3】利用甲烷可以有效降低有害气体对大气的污染,成为当前科学研究的重点课题。
(1)利用CH4和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应:
反应Ⅰ.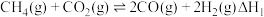
反应Ⅱ.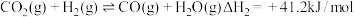
反应Ⅲ.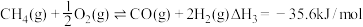
①已知: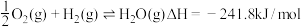 ,则△H1=
,则△H1=___________
②恒容密闭容器中CH4、CO2的分压分别为25 kPa、20 kPa,一定条件下发生反应Ⅰ。已知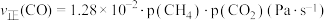 ,某时刻测得
,某时刻测得 ,则该时刻
,则该时刻
___________  。
。
(2)CH4(g)和H2S(g)反应可以生成化工原料CS2(g)和H2(g)。控制体系压强为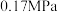 ,当原料初始组成n(CH4):n(H2S)=1:2,反应达到平衡时,四种组分的物质的量分数随温度的变化如图甲。
,当原料初始组成n(CH4):n(H2S)=1:2,反应达到平衡时,四种组分的物质的量分数随温度的变化如图甲。

①图中表示CS2、CH4变化的曲线分别是___________ 、___________ (填字母序号)。
②M点对应温度下,H2S的转化率是___________ ,反应的Kp=___________  (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
(3)在恒容密闭容器中,通入一定量CH4和NO2发生反应,相同时间内测得NO2的转化率与温度的关系如图乙。下列叙述正确的是___________。
(4)CH4燃料电池(NaOH溶液作电解质溶液)的正极反应式为___________ ,放电过程中溶液的pH___________ (填“增大”“减小”或“不变”)。
(1)利用CH4和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应:
反应Ⅰ.
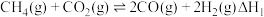
反应Ⅱ.
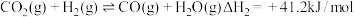
反应Ⅲ.
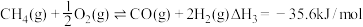
①已知:
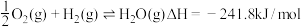 ,则△H1=
,则△H1=②恒容密闭容器中CH4、CO2的分压分别为25 kPa、20 kPa,一定条件下发生反应Ⅰ。已知
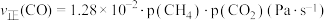 ,某时刻测得
,某时刻测得 ,则该时刻
,则该时刻
 。
。(2)CH4(g)和H2S(g)反应可以生成化工原料CS2(g)和H2(g)。控制体系压强为
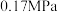 ,当原料初始组成n(CH4):n(H2S)=1:2,反应达到平衡时,四种组分的物质的量分数随温度的变化如图甲。
,当原料初始组成n(CH4):n(H2S)=1:2,反应达到平衡时,四种组分的物质的量分数随温度的变化如图甲。
①图中表示CS2、CH4变化的曲线分别是
②M点对应温度下,H2S的转化率是
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。(3)在恒容密闭容器中,通入一定量CH4和NO2发生反应,相同时间内测得NO2的转化率与温度的关系如图乙。下列叙述正确的是___________。
| A.200℃NO2的平衡转化率大于300℃NO2的平衡转化率 |
| B.b点的v(逆)大于e点的v(逆) |
| C.c点和d点均处于平衡状态 |
| D.适当升温或增大c(CH4)可提高C点时NO2的转化率和反应速率 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.运用电化学原理可生产硫酸;总反应为2SO2+O2+2H2O=2H2SO4,装置如图所示。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。

(1)①H+通过质子交换膜时的移动方向是_______ 。
A.从左向右 B.从右向左
②通入O2的电极反应式是_______ 。
II.光气(COCl2)是合成聚氨酯材料和制农药的原料。
(2)已知光气分子中每个原子最外层都达到8电子稳定结构,光气分子的电子式为_______ 。
(3)在活性炭催化下用氯气和一氧化碳合成光气:Cl2(g)+CO(g) COCl2(g) ΔH=-108 kJ·mol-1。已知:Cl-Cl、C≡O、C-Cl键的键能依次为243 kJ·mol-1、1076 kJ·mol-1、346 kJ·mol-1。根据上述反应估算光气中C=O键的键能为
COCl2(g) ΔH=-108 kJ·mol-1。已知:Cl-Cl、C≡O、C-Cl键的键能依次为243 kJ·mol-1、1076 kJ·mol-1、346 kJ·mol-1。根据上述反应估算光气中C=O键的键能为_______ kJ·mol-1
(4)一定温度下,该反应在密闭容器中进行,下列措施不改变化学反应速率的是_______

(1)①H+通过质子交换膜时的移动方向是
A.从左向右 B.从右向左
②通入O2的电极反应式是
II.光气(COCl2)是合成聚氨酯材料和制农药的原料。
(2)已知光气分子中每个原子最外层都达到8电子稳定结构,光气分子的电子式为
(3)在活性炭催化下用氯气和一氧化碳合成光气:Cl2(g)+CO(g)
 COCl2(g) ΔH=-108 kJ·mol-1。已知:Cl-Cl、C≡O、C-Cl键的键能依次为243 kJ·mol-1、1076 kJ·mol-1、346 kJ·mol-1。根据上述反应估算光气中C=O键的键能为
COCl2(g) ΔH=-108 kJ·mol-1。已知:Cl-Cl、C≡O、C-Cl键的键能依次为243 kJ·mol-1、1076 kJ·mol-1、346 kJ·mol-1。根据上述反应估算光气中C=O键的键能为(4)一定温度下,该反应在密闭容器中进行,下列措施不改变化学反应速率的是_______
| A.缩小体积使压强增大 | B.恒容,充入Cl2 |
| C.恒容,充入N2 | D.恒压,充入N2 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:I.
II.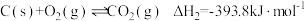
III.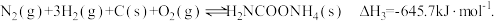
回答下列问题:
(1)写出 H2NCOONH4 分解生成 NH3 与 CO2 气体的热化学方程式:___________ 。
(2)在一定温度下,向 0.5L 密闭容器中,加入 0.1mol H2NCOONH4,实验测得 CO2 物质的量变化如下表所示:
从反应开始到 2min,用 NH3 的浓度变化表示的化学反应速率为___________ ;平衡后,H2NCOONH4 的转化率为___________ 。
(3)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
(4)对该反应,改变某一条件,对化学反应速率的影响及解释不正确的是___________。
已知:I.

II.
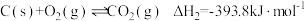
III.
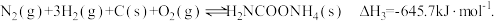
回答下列问题:
(1)写出 H2NCOONH4 分解生成 NH3 与 CO2 气体的热化学方程式:
(2)在一定温度下,向 0.5L 密闭容器中,加入 0.1mol H2NCOONH4,实验测得 CO2 物质的量变化如下表所示:
t/min | 0 | 1 | 2 | 3 | 4 |
n/mol | 0 | a | b | c | c |
(3)若在恒温恒压条件下进行反应,下列能够说明该反应已达到化学平衡状态的是___________。
| A.NH3 的浓度不再改变 | B.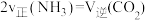 |
| C.容器体积不再改变 | D.容器内密度不再改变 |
| A.升高温度,使单位体积内活化分子百分数增加,反应速率加快 |
| B.增加反应物的量,使活化分子百分数增加,有效碰撞增多,反应速率加快 |
| C.使用催化剂能降低反应活化能,使单位体积内活化分子百分数增加,反应速率加快 |
| D.反应达平衡后,压缩体积增大压强,v 正 仍等于 v逆 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碲(Te)可用作半导体器件、合金、化工原料等。电解精炼铜所得的阳极泥中富含碲。工业上,常用铜阳极泥(主要成分是Cu2Te,含少量的Ag、Au)回收碲,其工艺流程如图:
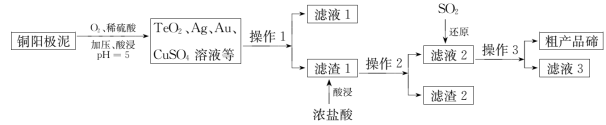
已知:①TeO2微溶于水,易与浓的强碱反应;
②TeO2与浓盐酸反应生成TeCl4。
回答下列问题:
(1)碲与硫是同主族元素,写出碲化氢的化学式:____ 。
(2)“加压、酸浸”时,Cu2Te转化为TeO2、CuSO4溶液的化学方程式为___ ;该步骤加压的目的是____ 。
(3)滤液2中通入SO2发生反应的化学方程式为___ 。
(4)滤液3中可以循环利用的物质有___ (填化学式)。
(5)工业上还可以将铜阳极泥煅烧(Cu2Te转化为TeO2、CuO)、碱浸后得到Na2TeO3溶液,再通过惰性电极电解的方法得到单质碲,则碱浸过程中生成Na2TeO3的化学方程式为___ 。

已知:①TeO2微溶于水,易与浓的强碱反应;
②TeO2与浓盐酸反应生成TeCl4。
回答下列问题:
(1)碲与硫是同主族元素,写出碲化氢的化学式:
(2)“加压、酸浸”时,Cu2Te转化为TeO2、CuSO4溶液的化学方程式为
(3)滤液2中通入SO2发生反应的化学方程式为
(4)滤液3中可以循环利用的物质有
(5)工业上还可以将铜阳极泥煅烧(Cu2Te转化为TeO2、CuO)、碱浸后得到Na2TeO3溶液,再通过惰性电极电解的方法得到单质碲,则碱浸过程中生成Na2TeO3的化学方程式为
您最近一年使用:0次
【推荐1】李克强总理在《2018年国务院政府工作报告》中强调“今年二氧化硫、氮氧化物排放量要下降3%。”研究烟气的脱硝(除NOx)、脱硫(除SO2)有着积极的环保意义。
Ⅰ.汽车排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g) 2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。

(1)图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是___ (填“a”或“b”)。
(2)在a曲线所示反应中,0~10min内,CO的平均反应速率v(CO)=____ ;T℃时,该反应的化学平衡常数K=___ ;平衡时若保持温度不变,再向容器中充入CO、CO2各0.2mol,则平衡将移动____ (填“向左”、“向右”或“不”)。
(3)15min时,n(NO)发生图中所示变化,则改变的条件可能是___ (填序号)
A.充入少量CO B.将N2液化移出体系 C.升高温度 D.加入催化剂
(4)Ⅱ.已知有下列反应:
①5O2(g)+4NH3(g) 6H2O(g)+4NO(g)△H1
6H2O(g)+4NO(g)△H1
②N2(g)+O2(g) 2NO(g)△H2
2NO(g)△H2
③2NO(g)+O2(g) 2NO2(g)△H3
2NO2(g)△H3
若在高效催化剂作用下可发生8NH3(g)+6NO2(g)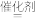 7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=
7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=___ (用△H1,△H2,△H3表示),△S___ 0。
(5)某温度下,向某恒容密闭容器中充入一定量的NH3和NO2,按照(4)的原理模拟污染物的处理。若容器中观察到___ (填序号),可判断该反应达到平衡状态。
A.混合气体颜色不再改变
B.混合气体的密度不再改变
C.混合气体平均相对分子质量不再改变
D.NH3和NO2的物质的量之比不再改变
Ⅰ.汽车排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g)
 2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
(1)图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是
(2)在a曲线所示反应中,0~10min内,CO的平均反应速率v(CO)=
(3)15min时,n(NO)发生图中所示变化,则改变的条件可能是
A.充入少量CO B.将N2液化移出体系 C.升高温度 D.加入催化剂
(4)Ⅱ.已知有下列反应:
①5O2(g)+4NH3(g)
 6H2O(g)+4NO(g)△H1
6H2O(g)+4NO(g)△H1②N2(g)+O2(g)
 2NO(g)△H2
2NO(g)△H2③2NO(g)+O2(g)
 2NO2(g)△H3
2NO2(g)△H3若在高效催化剂作用下可发生8NH3(g)+6NO2(g)
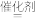 7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=
7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=(5)某温度下,向某恒容密闭容器中充入一定量的NH3和NO2,按照(4)的原理模拟污染物的处理。若容器中观察到
A.混合气体颜色不再改变
B.混合气体的密度不再改变
C.混合气体平均相对分子质量不再改变
D.NH3和NO2的物质的量之比不再改变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】对于反应N2O4(g) 2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)
2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)
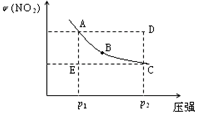
(1)B、C两点的反应速率的关系为B_________ C(填“>”“<”或“=”)。
(2)当反应处于A状态时,V正_____ V逆(填“>”“<”或“=”),A、B、C、D、E各状态中,V正<V逆的是_______________________ 。
(3)由D状态转变为C状态后,混合气体的总物质的量会______ (填“增大”、“减小”)。
(4)若在注射器中盛有一定量NO2,向内推活塞至原有体积的3/4,达到平衡时其中气体颜色较初始颜色如何变化_______ ,其原理为_________________________________ 。
 2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)
2NO2(g)在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)
(1)B、C两点的反应速率的关系为B
(2)当反应处于A状态时,V正
(3)由D状态转变为C状态后,混合气体的总物质的量会
(4)若在注射器中盛有一定量NO2,向内推活塞至原有体积的3/4,达到平衡时其中气体颜色较初始颜色如何变化
您最近一年使用:0次
【推荐3】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) ΔH=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=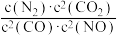 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:_______ ;下列措施能够增大此反应中NO的转化率的是(填字母代号)_______ 。
a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
①T1℃,0~5min内,以CO2表示的该反应速率v(CO2)=_______ ,该条件下的平衡常数K=_______ 。
②第15 min后,温度调整到T2,数据变化如上表所示,则T1_______ T2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应_______ 移动(填“正向”、“逆向”或“不”);最终达平衡时NO的转化率a=_______ 。
已知:2C(s)+O2(g)=2CO(g) ΔH=- 221 kJ/mol
C(s)+O2(g)=CO2(g) ΔH=- 393.5 kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181 kJ/mol
(1)若某反应的平衡常数表达式为K=
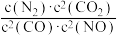 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:a.增大容器压强 b.升高温度 c.使用优质催化剂 d.增大CO的浓度
(2)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。| 物质的量/mol | T1/℃ | T2/℃ | |||||
| 0 | 5 min | 10 min | 15 min | 20 min | 15 min | 30 min | |
| NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
②第15 min后,温度调整到T2,数据变化如上表所示,则T1
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,则此时反应
您最近一年使用:0次
【推荐1】绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措,可以用以下方法制备氢气。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.2kJ•mol-1
CO(g)+3H2(g) △H=+206.2kJ•mol-1
ii.CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ•mol-1
CO2(g)+H2(g) △H=-41.2kJ•mol-1
(1)反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=______ kJ•mol-1。
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是______ (填标号)。
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。
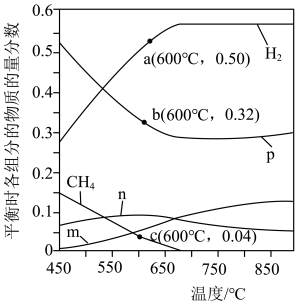
①图中表示CO2的物质的量分数与温度的变化曲线是______ (填字母)。
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是______ (填标号)。
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是______ 。
③600℃时,反应ii的平衡常数的计算式为Kp=______ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)。
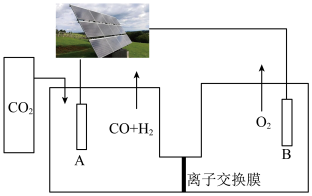
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO2和H2O在碱性电解液中制备水煤气(H2、CO),产物中H2和CO的物质的量之比为1∶1。
(4)电极B是______ 极,生成水煤气的电极反应式为______ 。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=+206.2kJ•mol-1
CO(g)+3H2(g) △H=+206.2kJ•mol-1ii.CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41.2kJ•mol-1
CO2(g)+H2(g) △H=-41.2kJ•mol-1(1)反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。

①图中表示CO2的物质的量分数与温度的变化曲线是
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是
③600℃时,反应ii的平衡常数的计算式为Kp=
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO2和H2O在碱性电解液中制备水煤气(H2、CO),产物中H2和CO的物质的量之比为1∶1。
(4)电极B是

您最近一年使用:0次
【推荐2】丙烯是重要的有机化工原料,丁烯催化裂解法是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。
反应如下:I主反应,3C4H8(g)=4C3H6(g) △H1
II副反应: C4H8(g)=2C2H4(g) △H2
(1) 已知丁烯的燃烧热△H3=-akJ/mol 丙烯的燃烧热△H4=-bkJ/mol。 计算: △H1=____ kJ/mol
(2) 以ZSM-5分子筛作为催化剂,测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T) 和压强(p)变化的趋势分别如图1和图2所示:
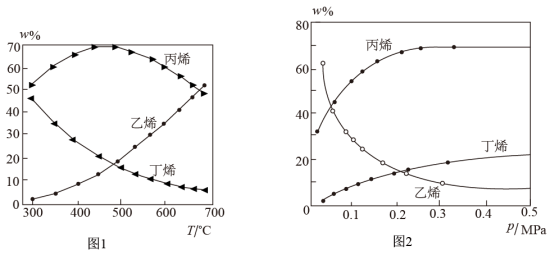
① 下列说法正确的是______ 。
A.随温度升高反应II的正反应速率增大,逆反应速率减小
B.温度可影响产物的选择性
C.根据350℃时各物质的质量分数可知,反应I的活化能低于反应II
D.制备丙烯适宜的温度和压强分别为600℃,0.5Mpa
②若某温度下反应达到平衡时C4H8、C3H6、C2H4的体积分数分别为20%、70%、10%,平衡时总压强为P,请计算该温度下反应的平衡常数Kp=_______ (Kp为用气体的分压表示的平衡常数,分压=气体的体积分数×体系总压)
③图2 中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是__________________ 。
(3) 在恒温恒容体系中,充入一定量的丁烯,转化率随时间的变化如图。在实际生产中,通常在恒压条件下以氮气作为反应体系的稀释剂,请在下图中画出恒压条件丁烯的转化率随时间变化由线_______ 。
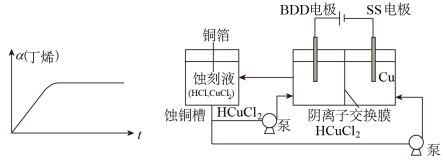
(4) 有研究者用HCl和CuCl2的混合液做蚀刻液,浸泡铜板可制备印刷电路板,蚀铜结束会产生大量含HCuC12废液。采用如图所示装置可直接从水中电解产生具有强氧化性的氢氧自由基(HO·),再进一步反应可实现阳极区蚀刻液再生的目的。
阳极区发生的反应为:_____________ ,H++CuCl2-+ HO·=Cu2++2Cl-+H2O
反应如下:I主反应,3C4H8(g)=4C3H6(g) △H1
II副反应: C4H8(g)=2C2H4(g) △H2
(1) 已知丁烯的燃烧热△H3=-akJ/mol 丙烯的燃烧热△H4=-bkJ/mol。 计算: △H1=
(2) 以ZSM-5分子筛作为催化剂,测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T) 和压强(p)变化的趋势分别如图1和图2所示:

① 下列说法正确的是
A.随温度升高反应II的正反应速率增大,逆反应速率减小
B.温度可影响产物的选择性
C.根据350℃时各物质的质量分数可知,反应I的活化能低于反应II
D.制备丙烯适宜的温度和压强分别为600℃,0.5Mpa
②若某温度下反应达到平衡时C4H8、C3H6、C2H4的体积分数分别为20%、70%、10%,平衡时总压强为P,请计算该温度下反应的平衡常数Kp=
③图2 中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是
(3) 在恒温恒容体系中,充入一定量的丁烯,转化率随时间的变化如图。在实际生产中,通常在恒压条件下以氮气作为反应体系的稀释剂,请在下图中画出恒压条件丁烯的转化率随时间变化由线

(4) 有研究者用HCl和CuCl2的混合液做蚀刻液,浸泡铜板可制备印刷电路板,蚀铜结束会产生大量含HCuC12废液。采用如图所示装置可直接从水中电解产生具有强氧化性的氢氧自由基(HO·),再进一步反应可实现阳极区蚀刻液再生的目的。
阳极区发生的反应为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】(1)在其他条件不变的情况下,起始氢气的物质的量[用n(H2)表示]对N2(g)+3H2(g)  2NH3(g)反应的影响可表示成如图所示的规律(图中
2NH3(g)反应的影响可表示成如图所示的规律(图中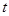 表示温度,
表示温度, 表示物质的量)。
表示物质的量)。

①比较在a、b、c三点处的平衡状态中,反应物N2的转化率最高的是__________ 。
②若容器容积为1L, =3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为
=3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为__________ mol,此条件下(t2)反应的平衡常数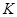 =
=________ 。
③图象中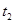 和
和 的关系是t2
的关系是t2 ______ t1(填“高于”“低于”“等于”或“无法确定”)。
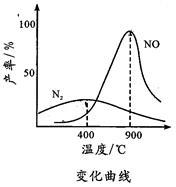
(2)氨气和氧气与145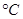 时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
4NH3+5O2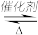 4NO+6H2O
4NO+6H2O
4NH3+3O2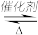 2N2+6H2O
2N2+6H2O
温度较低时以生成________ 为主,温度高于900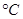 时,NO产率下降的原因是
时,NO产率下降的原因是______ 。
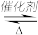 2NH3(g)反应的影响可表示成如图所示的规律(图中
2NH3(g)反应的影响可表示成如图所示的规律(图中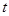 表示温度,
表示温度, 表示物质的量)。
表示物质的量)。
①比较在a、b、c三点处的平衡状态中,反应物N2的转化率最高的是
②若容器容积为1L,
 =3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为
=3mol,反应达到平衡时H2的转化率为60%,则在起始时体系中加入N2的物质的量为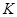 =
=③图象中
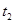 和
和 的关系是t2
的关系是t2 (2)氨气和氧气与145
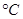 时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
时开始反应,在不同温度和催化剂条件下生成不同产物(如图所示)
4NH3+5O2
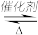 4NO+6H2O
4NO+6H2O4NH3+3O2
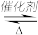 2N2+6H2O
2N2+6H2O温度较低时以生成
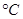 时,NO产率下降的原因是
时,NO产率下降的原因是
您最近一年使用:0次



