A、B、C、D是原子序数依次递增的四种短周期元素。基态A原子所含的电子只有一种运动状态;基态B原子中有三个未成对电子。A、B、C、D四种元素共同组成化合物M,M可发生如下反应:
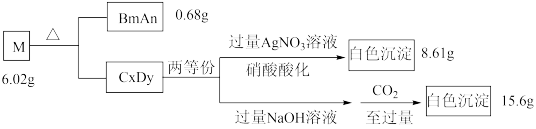
回答下列问题:
(1)B原子的价电子排布式为_______ 。实验室制备BmAn的化学方程式是_________ 。
(2)A、C、D三种元素的原子半径由大到小的顺序为_________ (用元素符号表示)。
(3)B元素的第一电离能比同周期相邻两种元素的都高;原因是____________ 。
(4) D元素的一种氧化物D2O为淡棕黄色气体,可由新制的HgO和D2发生歧化反应(氧化剂和还原剂为同一种物质的反应)制得。上述制备D2O的化学方程式为_________ 。
(5)D元素的另一种氧化物DO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaDO2、NaHSO4、NaHCO3的泡腾片,能快速溶于水,溢出大量气泡,得到DO2溶液。上述过程中,生成DO2的反应属于歧化反应,每生成1 mol DO2消耗NaDO2的量为_____ mol;若产生的“气泡”与DO2的物质的量相等,则反应过程中消耗NaDO2、NaHSO4、NaHCO3的物质的量之比为____________ 。
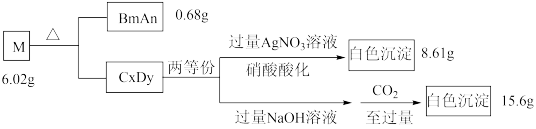
回答下列问题:
(1)B原子的价电子排布式为
(2)A、C、D三种元素的原子半径由大到小的顺序为
(3)B元素的第一电离能比同周期相邻两种元素的都高;原因是
(4) D元素的一种氧化物D2O为淡棕黄色气体,可由新制的HgO和D2发生歧化反应(氧化剂和还原剂为同一种物质的反应)制得。上述制备D2O的化学方程式为
(5)D元素的另一种氧化物DO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaDO2、NaHSO4、NaHCO3的泡腾片,能快速溶于水,溢出大量气泡,得到DO2溶液。上述过程中,生成DO2的反应属于歧化反应,每生成1 mol DO2消耗NaDO2的量为
19-20高三·山东潍坊·阶段练习 查看更多[2]
更新时间:2020-10-12 07:03:30
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】用粗铜精炼工业中产生的铜阳极泥(主要含Cu2Se、Ag2Se、金和铂等)为原料,回收并制备硝酸铜和硒的工艺流程如图:
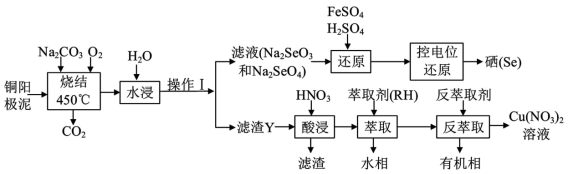
(1)工业上,高压氧气与铜阳极泥采用“逆流”的方式通入,其目的是_______ 。“烧结”时会发生多个反应,写出其中Cu2Se烧结时生成Cu2O、Na2SeO3反应方程式_______ 。
(2)在实验室,操作Ⅰ的名称为_______ 。
(3)滤渣Y的成分有Ag2O、_______ (填化学式,下同);已知萃取与反萃取原理为:2RH+Cu2+ R2Cu+2H+,则“反萃取”时反萃取剂最好选用
R2Cu+2H+,则“反萃取”时反萃取剂最好选用_______ 溶液。
(4)Na2SeO4中 的空间构型为
的空间构型为_______ ;常温下,H2SeO3的Ka1=1.0×10-3,Ka2=1.0×10-7;当常温下溶液的pH=4.5时,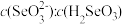 为
为_______ 。
(5)“控电位还原”是指在一定电压下,电位高的氧化剂优先被还原,电位低的氧化剂保留在溶液中,以达到硒与杂质金属的分离;酸性环境下,一些氧化剂的电位如下表(A/B:A代表氧化剂,B代表还原产物)。
则 、Fe3+和Cu2+氧化性由强到弱的顺序为
、Fe3+和Cu2+氧化性由强到弱的顺序为_______ ,在控电位还原时 还原反应(半反应)式为
还原反应(半反应)式为_______ 。

(1)工业上,高压氧气与铜阳极泥采用“逆流”的方式通入,其目的是
(2)在实验室,操作Ⅰ的名称为
(3)滤渣Y的成分有Ag2O、
 R2Cu+2H+,则“反萃取”时反萃取剂最好选用
R2Cu+2H+,则“反萃取”时反萃取剂最好选用(4)Na2SeO4中
 的空间构型为
的空间构型为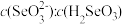 为
为(5)“控电位还原”是指在一定电压下,电位高的氧化剂优先被还原,电位低的氧化剂保留在溶液中,以达到硒与杂质金属的分离;酸性环境下,一些氧化剂的电位如下表(A/B:A代表氧化剂,B代表还原产物)。
| 名称 | Cu2+/Cu | Fe2+/Fe | Fe3+/Fe2+ | 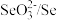 |
| 电位/V | 0.345 | -0.440 | 0.770 | 0.740 |
 、Fe3+和Cu2+氧化性由强到弱的顺序为
、Fe3+和Cu2+氧化性由强到弱的顺序为 还原反应(半反应)式为
还原反应(半反应)式为
您最近一年使用:0次
【推荐2】以软锰矿[主要成分为MnO2,还含有钙镁碳酸盐及少量的有机物(C12H22O11)]为原料制备硫酸锰,进而进一步制备Mn3O4。
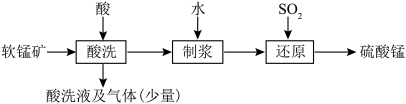
(1)制备硫酸锰的流程如下:
①写出用硝酸“酸洗”时,有机物与MnO2反应生成CO2的离子方程式___________ 。
②工业上常采用硝酸酸洗而不采用磷酸酸洗的主要原因是___________ 。
③控制反应温度和SO2流速一定,反应2小时,测得“还原”时锰元素的回收率与“制浆”时液固比的关系如图所示。液固比为20∶1浆料中锰元素回收率低于液固比为10∶1的浆料,原因是___________ 。___________ 。pH在4~6范围内,随溶液pH增大,MnS2O6的生成速率减小,其主要原因是___________ 。
(2)已知:pH在6.4~7.6范围内,MnSO4可被氧气直接氧化得到Mn3O4.实际工业生产时,先向MnSO4溶液中通入氨气生成 沉淀,再将
沉淀,再将 氧化得到Mn3O4,其他条件一定时,Mn2+的沉淀率随氨气通入量的变化如图所示。
氧化得到Mn3O4,其他条件一定时,Mn2+的沉淀率随氨气通入量的变化如图所示。___________ 。
②实际工业生产中,当氨气超过30mL时,Mn2+的沉淀率下降的主要原因是___________ 。
(1)制备硫酸锰的流程如下:
①写出用硝酸“酸洗”时,有机物与MnO2反应生成CO2的离子方程式
②工业上常采用硝酸酸洗而不采用磷酸酸洗的主要原因是
③控制反应温度和SO2流速一定,反应2小时,测得“还原”时锰元素的回收率与“制浆”时液固比的关系如图所示。液固比为20∶1浆料中锰元素回收率低于液固比为10∶1的浆料,原因是

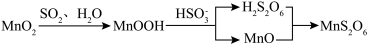
(2)已知:pH在6.4~7.6范围内,MnSO4可被氧气直接氧化得到Mn3O4.实际工业生产时,先向MnSO4溶液中通入氨气生成
 沉淀,再将
沉淀,再将 氧化得到Mn3O4,其他条件一定时,Mn2+的沉淀率随氨气通入量的变化如图所示。
氧化得到Mn3O4,其他条件一定时,Mn2+的沉淀率随氨气通入量的变化如图所示。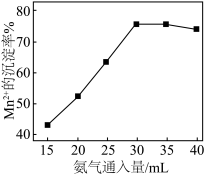
②实际工业生产中,当氨气超过30mL时,Mn2+的沉淀率下降的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氮氧化物是大气主要污染物,主要来自于工业废气及汽车尾气的排放,工业废气中NO是主要成分之一。
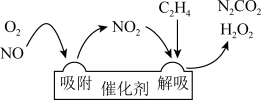
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式____________________ 。
(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4 Fe(NO)SO4
Fe(NO)SO4
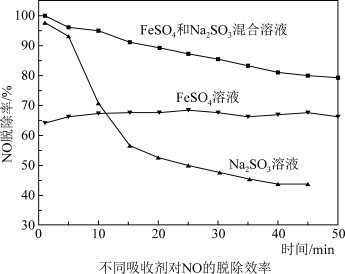
①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式_______________________________________ 。
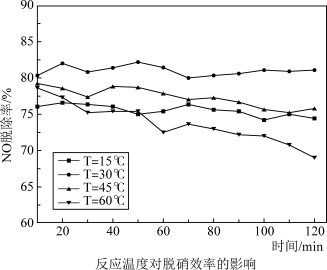
②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是_______________________________________ 。
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图
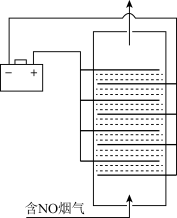
①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是____________________________ .
②写出NO发生反应的离子方程式____________________________ 。
③根据下图所示,脱NO过程中控制溶液pH在______________ 范围内更合理。
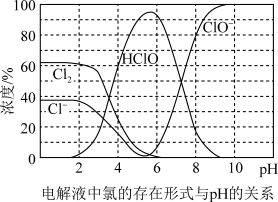
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式

(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4
 Fe(NO)SO4
Fe(NO)SO4①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式


②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图

①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是
②写出NO发生反应的离子方程式
③根据下图所示,脱NO过程中控制溶液pH在

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】A、B、D、E、F为短周期元素,非金属元素 A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。 B在 D中充分燃烧能生成其最高价化合物 BD2。 E+与D2-具有相同的电子数。 A 在 F中燃烧,产物溶于水得到一种强酸。
回答下列问题:
(1)A 在周期表中的位置是_____________ ,写出一种工业制备单质 F的离子方程式__________________ 。
(2)B、D、E 组成的一种盐中,E的质量分数为43%,其俗名为_______________ ,其水溶液与等物质的量的 F单质反应的化学方程式为_______________ ;在上述反应的产物中加入少量 KI,反应后加入 CC14并振荡,有机层显___________ 色。
(3)由这些元素组成的物质,其组成和结构信息如下表:

a 的化学式为____________ ;b 的化学式为____________ ;
c的电子式为____________ ;d的晶体类型是____________ 。
回答下列问题:
(1)A 在周期表中的位置是
(2)B、D、E 组成的一种盐中,E的质量分数为43%,其俗名为
(3)由这些元素组成的物质,其组成和结构信息如下表:

a 的化学式为
c的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】现有X、Y、Z、T四种短周期元素,原子序数依次增大。请根据下列相关信息,回答问题。
(1) Z2X4分子中Z原子采取________ 杂化,写出与之互为等电子体的有机物的结构简式_____________________
(2) Cl2T分子的空间构型___________ , Z2T的电子式_________________
(3) 请用价层电子对互斥理论解释ZX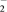 和ZX3的键角∠XZX的大小:
和ZX3的键角∠XZX的大小:_____________ 。
(4) Y晶体的晶胞如图所示,该晶胞含有______ 个Y原子,若晶胞的密度为d g·cm-3,阿伏加 德罗常数的值为NA(mol-1),则晶胞参数为a=_______ pm。(用含d 、NA的式子表示)
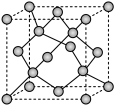
| 元素 | 相关信息 |
| X | 原子的1s轨道上只有1个电子 |
| Y | 原子的L层上s电子数等于p电子数 |
| Z | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的 |
| T | 负二价的元素T的氢化物在通常情况下是一种液体,且T的质量分数为88.9% |
(1) Z2X4分子中Z原子采取
(2) Cl2T分子的空间构型
(3) 请用价层电子对互斥理论解释ZX
 和ZX3的键角∠XZX的大小:
和ZX3的键角∠XZX的大小:(4) Y晶体的晶胞如图所示,该晶胞含有

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】W、X、Y、Z 是同一周期的四种短周期主族元素,原子序数依次增大。Z元素的最高正价与最低负价代数和为6,它们能够形成一种新型化合物 M,其结构如图。
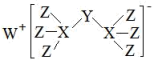
回答下列问题:
(1)元素W在周期表中的位置___________ ,写出元素Y基态原子核外电子排布式 ___________ 。
(2)X、Y、Z最高价含氧酸的酸性由强到弱的顺序为___________ (用化学式表示)。
(3)X—Z 共价键与 Y-Z 共价键的极性,前者___________ 后者(填“大于”、“小于”或“等于”), 原因___________ 。
(4)元素 M 是与 Y 同主族的短周期元素,两者最简单气态氢化物的稳定性关系为:___________ >___________ (填化学式),键角 H-M-H ___________ H-Y-H(填“大于”、“小于”或“等于”), 原因 ___________ 。
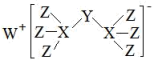
回答下列问题:
(1)元素W在周期表中的位置
(2)X、Y、Z最高价含氧酸的酸性由强到弱的顺序为
(3)X—Z 共价键与 Y-Z 共价键的极性,前者
(4)元素 M 是与 Y 同主族的短周期元素,两者最简单气态氢化物的稳定性关系为:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】下表为元素周期表的一部分。请回答下列问题:
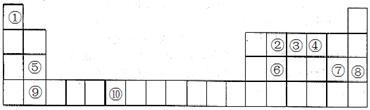
(1)上述元素中,属于s区的是___________ (填元素符号)。
(2)写出元素⑩的基态原子的电子排布式________________ 。
(3)元素第一电离能为⑤_______________ ⑨(填“大于”或“小于”)。
(4)元素③气态氢化物的中心原子有______________ 对弧对电子,其VSEPR模型为_____________ ;中心原子的杂化类型为_______________ ;该分子为_________________ 分子(填“极性”或“非极性”)。向AgNO3溶液中逐滴加入其水溶液,可观察到的现象为___________________ 。
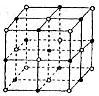
(5)元素⑦的钠盐晶胞结构如上图所示,每个Na+周围与之距离最近的Na+的个数为_____________ 。若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该钠盐的密度为________ (写出计算式)。

(1)上述元素中,属于s区的是
(2)写出元素⑩的基态原子的电子排布式
(3)元素第一电离能为⑤
(4)元素③气态氢化物的中心原子有

(5)元素⑦的钠盐晶胞结构如上图所示,每个Na+周围与之距离最近的Na+的个数为
您最近一年使用:0次
【推荐2】实验室模拟某含有机酸 工业废水的处理过程。
工业废水的处理过程。
 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:
(1) 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:


①基态 的价电子排布式为
的价电子排布式为___________ 。
②下列有关上述络合反应的说法中,正确的有___________ (填标号)。
A.反应达平衡时,溶液的颜色不再变化
B.增大 浓度,逆反应速率减小
浓度,逆反应速率减小
C. 过低不利于
过低不利于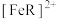 的生成
的生成
D.升高温度,该平衡正向移动
(2)紫外光催化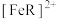 降解:
降解:
若有机酸为 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为:___________ 。
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:
(i)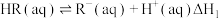
(ii)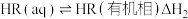
(iii)
(3)根据盖斯定律,反应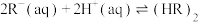 (有机相)的
(有机相)的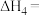
___________ 。
(4)水相的 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比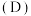 有影响。
有影响。
已知: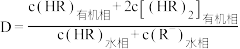 。
。
①常温下,配制体积相同、 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因___________ 。 溶液
溶液 时,
时,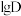 随
随 的变化曲线如图所示。
的变化曲线如图所示。 萃取宜在
萃取宜在___________ 温度下进行(填“较高”或“较低”)。
 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数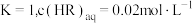 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中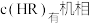
___________ 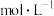 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
___________ (写出计算过程)。
 工业废水的处理过程。
工业废水的处理过程。 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:(1)
 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:

①基态
 的价电子排布式为
的价电子排布式为②下列有关上述络合反应的说法中,正确的有
A.反应达平衡时,溶液的颜色不再变化
B.增大
 浓度,逆反应速率减小
浓度,逆反应速率减小C.
 过低不利于
过低不利于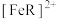 的生成
的生成 D.升高温度,该平衡正向移动
(2)紫外光催化
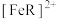 降解:
降解:若有机酸为
 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为: ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:(i)
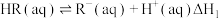
(ii)
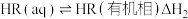
(iii)

(3)根据盖斯定律,反应
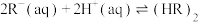 (有机相)的
(有机相)的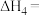
(4)水相的
 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比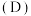 有影响。
有影响。已知:
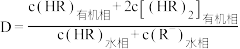 。
。①常温下,配制体积相同、
 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因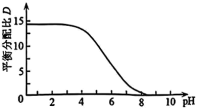
 溶液
溶液 时,
时,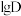 随
随 的变化曲线如图所示。
的变化曲线如图所示。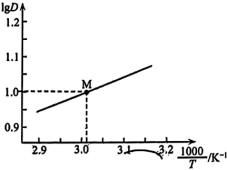
 萃取宜在
萃取宜在 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数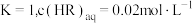 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中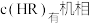
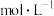 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】I.金(79Au)是一种非常稳定的金属,但也可以形成多种化合物,并在化合物中呈一价或三价。
(1)已知Au的基态原子的价电子排布式为5dl06s1,则Au位于周期表______ 区。基态Au3+的价电子中空间运动状态不同的电子数为______ 种
(2)有一种化合物由Cs、Cl、Au三种元素组成,其晶胞如下。大球为Cs,小球为Cl,其余球为Au。
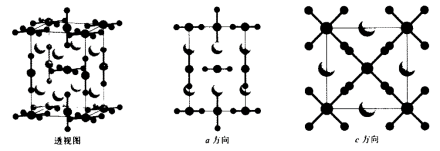
该化合物的化学式为______ ,其中金原子有2种不同的化学环境,形成2种不同的配离子,它们分别是______ 和______ 。
II.过渡金属钛、铜、锌等金属及其化合物在工业上有重要用途。
(3)TiOSO4溶液中加入H2O2可以生成稳定的[TiO(H2O2)]+。己如SzCl2的分子结构与H2O2相似,第一电离能(I1): I1(O)______ I1(S)(填“大于或“小于”),原因是______ ;沸点: H2O2______ S2Cl2(填“>”或“<”),其原因是______ 。
(4)超细铜粉可用作导电材料、催化剂等,制备方法如下:
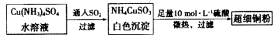
①关于[Cu(NH3)4]SO4和NH4CuSO3中的阴离子相同之处为______ 不同之处为______ ( 填标号)
A.中心原子的杂化轨道类型 B.中心原子的孤电子对数
C.立体结构 D.VSEPR模型
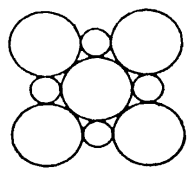
III.(5)MgO具有NaCl型结构(示意图如图所示),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为______ nm(结果保留三位小数)。
(1)已知Au的基态原子的价电子排布式为5dl06s1,则Au位于周期表
(2)有一种化合物由Cs、Cl、Au三种元素组成,其晶胞如下。大球为Cs,小球为Cl,其余球为Au。

该化合物的化学式为
II.过渡金属钛、铜、锌等金属及其化合物在工业上有重要用途。
(3)TiOSO4溶液中加入H2O2可以生成稳定的[TiO(H2O2)]+。己如SzCl2的分子结构与H2O2相似,第一电离能(I1): I1(O)
(4)超细铜粉可用作导电材料、催化剂等,制备方法如下:

①关于[Cu(NH3)4]SO4和NH4CuSO3中的阴离子相同之处为
A.中心原子的杂化轨道类型 B.中心原子的孤电子对数
C.立体结构 D.VSEPR模型
III.(5)MgO具有NaCl型结构(示意图如图所示),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】(Ⅰ)Q、W、X、Y、Z五种短周期元素原子序数依次增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)W、X、Y三种元素的第一电离能由大到小的顺序是__________ 。
(2) 与
与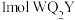 所含
所含 键的比值为
键的比值为__________ 。
(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为__________ 。
①该化合物的化学式为:__________ 。
②预测该化合物熔点应__________ 金刚石(填“高于”或“低于”)。
(Ⅱ)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5) 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的电子排布式为
的电子排布式为__________ 。
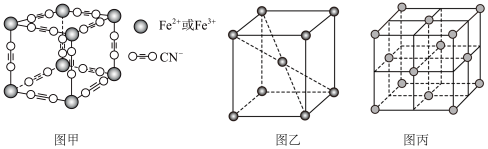
(6)普鲁士蓝俗称铁蓝,结构如图甲所示( 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为__________ 。又知该晶体中铁元素有 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为__________ 。
(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为__________ 。
(1)W、X、Y三种元素的第一电离能由大到小的顺序是
(2)
 与
与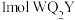 所含
所含 键的比值为
键的比值为(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为
①该化合物的化学式为:
②预测该化合物熔点应
(Ⅱ)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(5)
 可以与
可以与 、
、 、有机分子等形成配合物。基态
、有机分子等形成配合物。基态 的电子排布式为
的电子排布式为(6)普鲁士蓝俗称铁蓝,结构如图甲所示(
 未画出),平均每两个立方体中含有一个
未画出),平均每两个立方体中含有一个 ,该晶体的化学式为
,该晶体的化学式为 价和
价和 价两种,则
价两种,则 与
与 的个数比为
的个数比为(7)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】已知Mn、Fe、Co是合金中的重要元素,而P、S、C1是农药中的重要元素。请回答下列问题:
(1)基态锰原子的价电子排布图为___________ 。
(2)已知PCl3的沸点高于SCl2,原因是___________ 。
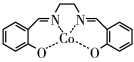
(3)以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构如图所示,下列说法错误的是___________ 。
A.第一电离能:H<O<N
B.该配合物中C原子的杂化方式均为sp
C.该配合物中Co原子的配位数为4
D.基态Co原子核外电子的空间运动状态有27种
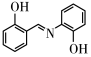
(4)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与Mn2+形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与Mn2+形成配位键的原子有___________ (填元素符号),锰试剂___________ (填“能”或“不能”)形成分子内氢键。
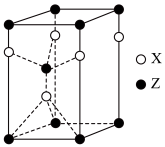
(5)阿拉班达石(alabandite)是一种属于立方晶系的硫锰矿,其晶胞如图a所示(●=Mn,○=S)。在该晶胞中,硫原子的堆积方式为___________ 。
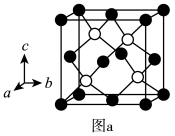
(6)已知阿拉班达石晶胞中最近两个硫原子之间的距离为dÅ(1Å=10-10m),晶体密度为ρg▪cm-3,则阿伏加德罗常数的值NA=___________ (不要求化简)。
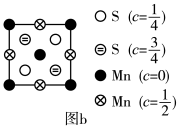
(7)为更清晰地展示晶胞中原子所在的位置,晶体化学中常将立体晶胞结构转化为平面投影图。例如:沿阿拉班达石晶胞的c轴将原子投影到ab平面,即可用图b表示。下列晶体结构投影图可能表示MnS晶体的是___________ 。
A.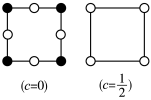 B.
B.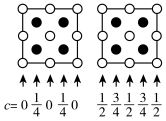
C. D.
D.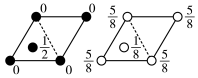
(1)基态锰原子的价电子排布图为
(2)已知PCl3的沸点高于SCl2,原因是
(3)以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构如图所示,下列说法错误的是

A.第一电离能:H<O<N
B.该配合物中C原子的杂化方式均为sp
C.该配合物中Co原子的配位数为4
D.基态Co原子核外电子的空间运动状态有27种
(4)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与Mn2+形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与Mn2+形成配位键的原子有

(5)阿拉班达石(alabandite)是一种属于立方晶系的硫锰矿,其晶胞如图a所示(●=Mn,○=S)。在该晶胞中,硫原子的堆积方式为

(6)已知阿拉班达石晶胞中最近两个硫原子之间的距离为dÅ(1Å=10-10m),晶体密度为ρg▪cm-3,则阿伏加德罗常数的值NA=
(7)为更清晰地展示晶胞中原子所在的位置,晶体化学中常将立体晶胞结构转化为平面投影图。例如:沿阿拉班达石晶胞的c轴将原子投影到ab平面,即可用图b表示。下列晶体结构投影图可能表示MnS晶体的是

A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】图1是元素周期表的一部分,已知A、B、C、D、E、F、G都是周期表中的前四周期元素,它们在周期表中的位置如图1所示。
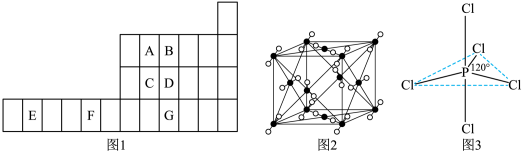
试回答下列问题:
(1)F元素基态原子的核外电子排布式为_________________ 。
(2)ABC的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)B元素单质分子中的_______ 个π键,与其互为等电子体的阴离子为____________________ 。
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用________ 杂化,每个分子周围有_____ 个分子与之距离相等且最近。若晶胞棱长为a pm,则该晶体密度的表达式为________ g·cm-3。
(5)G元素的氢化物分子的空间构型为________ ,其沸点与B元素的氢化物相比________ (填高或低),其原因是________ 。
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式________ 。
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同__________ ?(填“相同”或“不同”)。

试回答下列问题:
(1)F元素基态原子的核外电子排布式为
(2)ABC的第一电离能由大到小的顺序
(3)B元素单质分子中的
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用
(5)G元素的氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同
您最近一年使用:0次



