下列说法正确的是( )
| A.pH=4的醋酸中:c(H+)=4.0mol/L |
B.饱和小苏打溶液中:c(Na+)=c(HCO ) ) |
| C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(CH3COO-)=c(Cl-) |
| D.室温时,用广泛pH试纸测得某溶液pH为2.3 |
更新时间:2020-10-29 18:04:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知在常温下常见弱酸的电离平衡常数 如表所示,下列判断正确的是
如表所示,下列判断正确的是
 如表所示,下列判断正确的是
如表所示,下列判断正确的是| 溶质 |  |  |  |  |
电离平衡常数 |  | 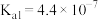 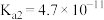 | 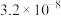 |  |
A.结合 的能力: 的能力: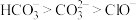 |
B.相同温度下, 溶液的电离常数大于 溶液的电离常数大于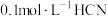 |
C.少量 通入NaClO溶液中的离子方程式: 通入NaClO溶液中的离子方程式: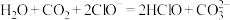 |
| D.相同温度下,等体积等pH的醋酸和HClO溶液中和氢氧化钠的量:HClO>醋酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】丙二酸(H2A)是一种二元弱酸,其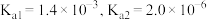 。丙二酸能与
。丙二酸能与 溶液反应生成
溶液反应生成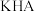 。下列叙述正确的是
。下列叙述正确的是
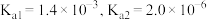 。丙二酸能与
。丙二酸能与 溶液反应生成
溶液反应生成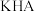 。下列叙述正确的是
。下列叙述正确的是A.常温下, 的KHA溶液呈碱性 的KHA溶液呈碱性 |
B.KHA溶液中: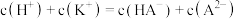 |
C.加水稀释KHA溶液,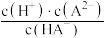 增大 增大 |
D.适当加热 溶液,溶液中 溶液,溶液中 减少 减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,下列各溶液的叙述中正确的是
| A.NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-) |
| B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性:c(CH3COO-)>c(CH3COOH) >c(Cl-)>c(H+) |
| C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D.向1.00 L 0.3 mol/LNaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:氟锑酸(HSbF6)是一种比硫酸强的酸,叫超强酸。常温下。Ka(HF)=3.5×10-4。常温下,向20mL,浓度均为0.1mol·L-1的HF和HSbF6的混合溶液中逐滴缓慢加入cmol·L-1NaOH溶液(忽略混合时溶液体积变化)。利用传感器测得该过程中溶液的pM随溶液体积的变化曲线如图所示。已知溶液中阳离子总浓度用c(M)表示,pM=-lgc(M)。下列叙述错误的是
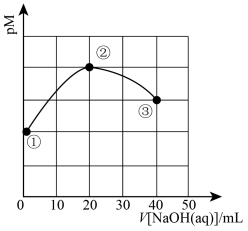

| A.在①、②、③中,导电率最大的是① |
B.某点c(Na+)=c(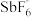 )+c(F-)存在于②和③之间 )+c(F-)存在于②和③之间 |
| C.上述滴加NaOH溶液浓度为0.1mol·L-1 |
| D.①点溶液中c(F-)≈3.5×10-3mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常稳下,某绝热容器中盛有50mLc(H+)=10-3mol·L-1的HX溶液,向该容器中滴加c(OH-)=10-2mol·L-1的NaOH溶液,滴加过程中混合溶液的温度(T)与所加溶液体积(V)的关系如图所示。下列叙述不正确的是
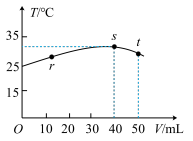

| A.s点时:c(Na+)>c(X-)>c(OH-)>c(H+) |
| B.r→s的过程中,混合溶液中可能存在c(X-)=c(Na+) |
| C.pH=10的NaX溶液,用蒸馏水稀释10倍后,溶液的pH>9 |
| D.已知某温度下CaX2的Ksp=5.3×10-9mol·L-3,在该温度下c(X-)=0.1mol·L-1的溶液中Ca2+可能的最高浓度是5.3×10-8mol·L-1 |
您最近一年使用:0次

 溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系
溶液中,各含碳粒子的物质的量分数与pH的关系。在图2中,曲线Ⅰ满足关系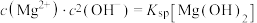 ,曲线Ⅱ满足关系
,曲线Ⅱ满足关系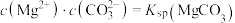 。[不同pH下
。[不同pH下 由图1得到]。下列说法不正确的是
由图1得到]。下列说法不正确的是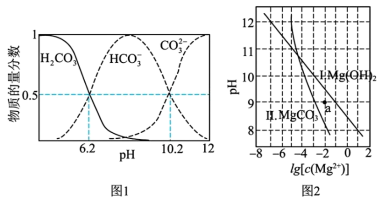
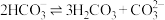 的平衡常数
的平衡常数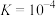
 发生水解时,溶液
发生水解时,溶液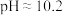
 沉淀
沉淀


