I.二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ· mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ· mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
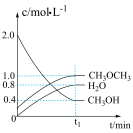
相同条件下改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4 mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4 mol·L-1,此时正、逆反应速率的大小:v正_____ v逆(填“>”、“<”或“=”),反应向______ 反应方向进行(填“正”或“逆”)。
II.若在恒温恒容条件下,仅发生反应MoS2(s) Mo(s)+S2(g)
Mo(s)+S2(g)
①下列说法正确的是________ (填字母)。
A.气体的密度不变,则反应一定达到了平衡状态
B.气体的相对分子质量不变,反应不一定处于平衡状态
C.增加MoS2的量,平衡正向移动
②达到平衡时S2(g)的浓度为1.4mol•L-1,充入一定量的S2(g),反应再次达到平衡,S2(g)浓度____ (填“>”“<”或“=”)1.4mol•L-1。
III.在2L恒容密闭容器中充入1.0molS2(g)和1.5molO2(g),若仅发生反应:S2(g)+2O2(g) 2SO2(g),5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内,S2(g)的反应速率为
2SO2(g),5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内,S2(g)的反应速率为__________ 。
 CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ· mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ· mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
相同条件下改变起始浓度,某时刻各组分浓度依次为c(CH3OH)=0.4 mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4 mol·L-1,此时正、逆反应速率的大小:v正
II.若在恒温恒容条件下,仅发生反应MoS2(s)
 Mo(s)+S2(g)
Mo(s)+S2(g)①下列说法正确的是
A.气体的密度不变,则反应一定达到了平衡状态
B.气体的相对分子质量不变,反应不一定处于平衡状态
C.增加MoS2的量,平衡正向移动
②达到平衡时S2(g)的浓度为1.4mol•L-1,充入一定量的S2(g),反应再次达到平衡,S2(g)浓度
III.在2L恒容密闭容器中充入1.0molS2(g)和1.5molO2(g),若仅发生反应:S2(g)+2O2(g)
 2SO2(g),5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内,S2(g)的反应速率为
2SO2(g),5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内,S2(g)的反应速率为
更新时间:2020-11-10 10:27:12
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】工业上,在催化剂条件下,用NH3作为还原剂将烟气中的NOx还原成无害的氮气和水,反应方程式可表示为:2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)
(1)一定条件下,在容积为2L的密闭容器内反应,20min时达到平衡,生成N20.6mol,则平均反应速率v(NO)=_______ 。可从混合气体的颜色变化判断上述反应是否达到平衡,其理由是_______ 。
(2)该反应平衡常数表达式K=_______ 。在温度不变的条件下将容器体积压缩至原来的一半,达到新的平衡后NO的浓度为原来的1.6倍,平衡常数为K2,则K1与K2的大小关系是_______ (选填编号)。
a.K1<K2 b.K1=K2 c.K1>K2 d.无法确定
(3)若其中的反应转化率(α)与反应温度(T)和压强(P)的关系如图所示。

根据图象判断:P1_______ P2(填“>”、“<”或“=”)。该反应是_______ 反应(填“吸热”或“放热”)。
(4)与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2+HCl→ClO2↑+NaCl+ (没有配平)
补全方程式并配平,标出电子转移方向和数目。_______
NaClO2+ HCl→ ClO2↑+ NaCl+
(5)该反应中氧化剂和还原剂的物质的量之比是_______ 。若生成0.2 mol ClO2,转移电子数为_______ 个。
 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)(1)一定条件下,在容积为2L的密闭容器内反应,20min时达到平衡,生成N20.6mol,则平均反应速率v(NO)=
(2)该反应平衡常数表达式K=
a.K1<K2 b.K1=K2 c.K1>K2 d.无法确定
(3)若其中的反应转化率(α)与反应温度(T)和压强(P)的关系如图所示。

根据图象判断:P1
(4)与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2+HCl→ClO2↑+NaCl+ (没有配平)
补全方程式并配平,标出电子转移方向和数目。
NaClO2+ HCl→ ClO2↑+ NaCl+
(5)该反应中氧化剂和还原剂的物质的量之比是
您最近半年使用:0次
【推荐2】(1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1molN2中的 键需要吸收
键需要吸收 能量;破坏
能量;破坏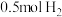 中的
中的 键需要吸收
键需要吸收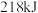 能量;形成
能量;形成 中的
中的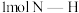 键能释放
键能释放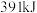 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
①________________  ,②
,②____________________  。
。

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为__________________ 。
②装置乙中正极的电极反应式为________________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是________ 。
(3)一定温度下,在体积为 的恒容密闭容器中充入
的恒容密闭容器中充入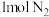 和
和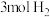 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
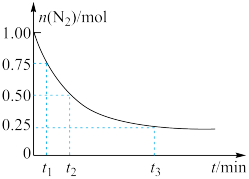
从开始反应到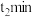 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_________ 。
 键需要吸收
键需要吸收 能量;破坏
能量;破坏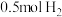 中的
中的 键需要吸收
键需要吸收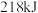 能量;形成
能量;形成 中的
中的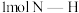 键能释放
键能释放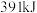 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。①
 ,②
,② 。
。
(2)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 |  甲 |  乙 |  丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为
 的恒容密闭容器中充入
的恒容密闭容器中充入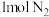 和
和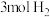 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
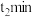 ,用
,用 表示的化学反应速率为
表示的化学反应速率为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究性学习组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
(1)通过实验A、B,可探究出_______ 的改变对反应速率的影响,其中
_______ ,
_______ ,通过实验_______ 可探究出温度变化对化学反应速率的影响。
(2)利用实验B中数据计算,从反应开始到结束,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为___ 。
(3)已知 是一种弱酸,该反应中有无色无味气体产生,且锰元素被还原为
是一种弱酸,该反应中有无色无味气体产生,且锰元素被还原为 ,写出相应反应的离子方程式
,写出相应反应的离子方程式_______ 。
(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对 与
与 之间的反应有某种特殊的作用,则该作用是
之间的反应有某种特殊的作用,则该作用是___ 。
 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:| 实验序号 | 实验温度 |  溶液 溶液 |  溶液 溶液 |  | 溶液褪色时间 | ||
| V(mL) | c(mol/L) | V(mL) | c(mol/L) | V(mL) | t(s) | ||
| A | 293K | 2 | 0.02 | 4 | 0.1 | 0 |  |
| B |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313K | 2 | 0.02 |  | 0.1 | 1 |  |


(2)利用实验B中数据计算,从反应开始到结束,用
 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为(3)已知
 是一种弱酸,该反应中有无色无味气体产生,且锰元素被还原为
是一种弱酸,该反应中有无色无味气体产生,且锰元素被还原为 ,写出相应反应的离子方程式
,写出相应反应的离子方程式(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对
 与
与 之间的反应有某种特殊的作用,则该作用是
之间的反应有某种特殊的作用,则该作用是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】深入研究碳、氮元素的物质转化有着重要的实际意义,按要求回答下列问题:
(1)合成尿素的反应为:2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(l),若向某恒温且恒容的密闭容器中加入等物质的量的NH3和CO2,发生上述反应。下列叙述不能说明反应已经达到平衡状态的是
CO(NH2)2(g)+H2O(l),若向某恒温且恒容的密闭容器中加入等物质的量的NH3和CO2,发生上述反应。下列叙述不能说明反应已经达到平衡状态的是_______ (填标号)。
(2)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g) CO2(g)+N2(g)。在Zn2+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
CO2(g)+N2(g)。在Zn2+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。

总反应:CO(g)+N2O(g) CO2(g)+N2(g) △H=
CO2(g)+N2(g) △H=_______ kJ•mol-1;该总反应的决速步是反应_______ (填“①”或“②”)。
(3)已知:CO(g)+N2O(g) CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是
CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是_______ (填字母序号)。
(4)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和N2O(g)发生上述反应,在不同条件下达到平衡时,在T1K时N2O的转化率与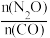 ,在
,在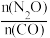 =1时N2O的转化率与
=1时N2O的转化率与 的变化曲线如图3所示:
的变化曲线如图3所示:
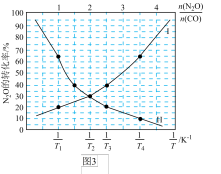
①表示N2O的转化率随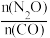 的变化曲线为
的变化曲线为_______ 曲线(填“Ⅰ”或“Ⅱ”)。
②已知:该反应的标准平衡常数KΘ=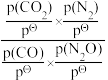 ,其中pΘ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数KΘ=
,其中pΘ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数KΘ=_______ (计算结果保留两位有效数字,P分=P总×物质的量分数)。
(1)合成尿素的反应为:2NH3(g)+CO2(g)
 CO(NH2)2(g)+H2O(l),若向某恒温且恒容的密闭容器中加入等物质的量的NH3和CO2,发生上述反应。下列叙述不能说明反应已经达到平衡状态的是
CO(NH2)2(g)+H2O(l),若向某恒温且恒容的密闭容器中加入等物质的量的NH3和CO2,发生上述反应。下列叙述不能说明反应已经达到平衡状态的是| A.断裂6molN-H键的同时断裂2molO-H键 | B.压强不再变化 |
| C.混合气体的密度不再变化 | D.CO2的体积分数不再变化 |
(2)CO用于处理大气污染物N2O的反应为CO(g)+N2O(g)
 CO2(g)+N2(g)。在Zn2+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
CO2(g)+N2(g)。在Zn2+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。
总反应:CO(g)+N2O(g)
 CO2(g)+N2(g) △H=
CO2(g)+N2(g) △H=(3)已知:CO(g)+N2O(g)
 CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是
CO2(g)+N2(g)的速率方程为v=k•c(N2O),k为速率常数,只与温度有关。为提高反应速率,可采取的措施是| A.升温 | B.恒容时,再充入CO |
| C.恒容时,再充入N2O | D.恒压时,再充入N2 |
(4)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和N2O(g)发生上述反应,在不同条件下达到平衡时,在T1K时N2O的转化率与
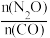 ,在
,在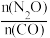 =1时N2O的转化率与
=1时N2O的转化率与 的变化曲线如图3所示:
的变化曲线如图3所示:
①表示N2O的转化率随
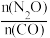 的变化曲线为
的变化曲线为②已知:该反应的标准平衡常数KΘ=
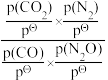 ,其中pΘ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数KΘ=
,其中pΘ为标准压强(100kPa),p(CO2)、p(N2)、p(N2O)和p(CO)为各组分的平衡分压,则T4时,该反应的标准平衡常数KΘ=
您最近半年使用:0次
【推荐2】CO2、CO 转化重整是环保的重要举措,受到社会越来越多的关注。回答下列问题:
(1)CO2与 H2在催化剂作用反应的能量变化如图甲所示。
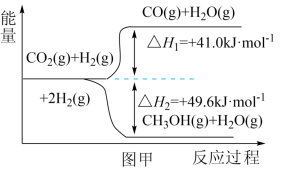
①CO2与H2在催化作用下发生吸热反应的产物为___________ 。
②写出CO(g)和H2(g)合成CH3OH(g)的热化学方程式为___________ 。
(2)a mol CO2和 3a mol H2混和气体在 Cu-ZnO/ZrO2催化下反应,测得 CO2转化率及 CH3OH 和 CO 选择率随温度变化如图乙所示(选择率:转化的 CO2中生成 CH3OH 或 CO 的百分比)。

图乙中 CH3OH 选择率对应的曲线是___________ (填“b”或“c”)
(3)400 K, 反应物的起始浓度 c(H2)=0.20 mol·L -1,c(CO)=0.10 mol·L -1,达平衡时 c(CH3OH) =0.080 mol·L-1,则:
①CO 的平衡转化率为___________ ,
②该温度下平衡常数 K的数值为___________ 。
③等温等容时下列说法不能证明该反应达到平衡状态的是( )
A.混合气体的平均摩尔质量不变 B.消耗1molCO的同时生成1mol CH3OH
C.体系的压强不变时 D.H2的浓度不变时
(1)CO2与 H2在催化剂作用反应的能量变化如图甲所示。

①CO2与H2在催化作用下发生吸热反应的产物为
②写出CO(g)和H2(g)合成CH3OH(g)的热化学方程式为
(2)a mol CO2和 3a mol H2混和气体在 Cu-ZnO/ZrO2催化下反应,测得 CO2转化率及 CH3OH 和 CO 选择率随温度变化如图乙所示(选择率:转化的 CO2中生成 CH3OH 或 CO 的百分比)。

图乙中 CH3OH 选择率对应的曲线是
(3)400 K, 反应物的起始浓度 c(H2)=0.20 mol·L -1,c(CO)=0.10 mol·L -1,达平衡时 c(CH3OH) =0.080 mol·L-1,则:
①CO 的平衡转化率为
②该温度下平衡常数 K的数值为
③等温等容时下列说法不能证明该反应达到平衡状态的是
A.混合气体的平均摩尔质量不变 B.消耗1molCO的同时生成1mol CH3OH
C.体系的压强不变时 D.H2的浓度不变时
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】研究氮的氧化物、碳的氧化物等大气污染物的处理具有重要意义。
I. 已知:①N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol-1
②CO的燃烧热△H= - 283 kJ·mol-1
(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物(NO和CO)转化为无毒的大气循环物质,该反应的热化学方程式为___________ 。
(2)一定温度下,在恒容密闭容器中充入1 molNO和2 molCO进行该反应,下列能判断反应达到化学平衡状态的是___________ 。
①单位时间内消耗a mol CO的同时生成2a mol NO
②混合气体的平均相对分子质量不再改变
③混合气体中NO和CO的物质的量之比保持不变
④混合气体的密度不再改变
II. 臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g) N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:
N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:
(3)T1___________ T2(填>、<或=,下同),该反应ΔH___________ 0 。简述理由___________ 。
(4)甲容器中,0~3s内的平均反应速率v(NO2)=___________ 。
(5)甲容器中NO2平衡转化率为___________ ,T1时该反应的平衡常数为___________ 。
I. 已知:①N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol-1
②CO的燃烧热△H= - 283 kJ·mol-1
(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物(NO和CO)转化为无毒的大气循环物质,该反应的热化学方程式为
(2)一定温度下,在恒容密闭容器中充入1 molNO和2 molCO进行该反应,下列能判断反应达到化学平衡状态的是
①单位时间内消耗a mol CO的同时生成2a mol NO
②混合气体的平均相对分子质量不再改变
③混合气体中NO和CO的物质的量之比保持不变
④混合气体的密度不再改变
II. 臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)
 N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:
N2O5(g)+O2(g),向甲、乙两个体积都为1.0 L的恒容密闭容器中分别充入2.0 mol NO2和1.0 mol O3,分别在T1、T2温度下,经过一段时间后达到平衡。反应过程中n(O2)随时间(t)变化情况见下表:| t/s | 0 | 3 | 6 | 12 | 24 | 36 |
| 甲容器(T1)n(O2)/mol | 0 | 0.36 | 0.60 | 0.80 | 0.80 | 0.80 |
| 乙容器(T2)n(O2)/mol | 0 | 0.30 | 0.50 | 0.70 | 0.85 | 0.85 |
(4)甲容器中,0~3s内的平均反应速率v(NO2)=
(5)甲容器中NO2平衡转化率为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】根据下表所示化学反应与数据关系:
(1)反应①是__________  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(2)写出反应③的平衡常数 的表达式
的表达式 __________ 。
(3)根据反应①与②可推导出 、
、 与
与 之间的关系,则
之间的关系,则
__________  用
用 、
、 表示
表示 。
。
(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有__________  填写字母序号
填写字母序号 。
。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO浓度
(5)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在 、
、 、
、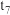 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断
时都改变了一种条件,试判断 时改变的是
时改变的是___
②若 时降压,
时降压,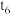 时增大反应物的浓度,请在图中画出
时增大反应物的浓度,请在图中画出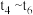 时逆反应速率与时间的关系曲线
时逆反应速率与时间的关系曲线___ 。
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
①Fe(s)+CO2(g) FeO(s)+CO(s) FeO(s)+CO(s) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g)  FeO(s)+H2(g) FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g)  CO2(g)+H2(g) CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(2)写出反应③的平衡常数
 的表达式
的表达式 (3)根据反应①与②可推导出
 、
、 与
与 之间的关系,则
之间的关系,则
 用
用 、
、 表示
表示 。
。(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有
 填写字母序号
填写字母序号 。
。A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO浓度
(5)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在
 、
、 、
、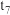 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断
时都改变了一种条件,试判断 时改变的是
时改变的是②若
 时降压,
时降压,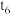 时增大反应物的浓度,请在图中画出
时增大反应物的浓度,请在图中画出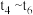 时逆反应速率与时间的关系曲线
时逆反应速率与时间的关系曲线
您最近半年使用:0次
【推荐2】汽车尾气是造成大气污染的主要来源之一。
(1)已知:①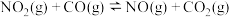

②

③

则反应④

________ 
(2)在某温度下的2L密闭容器中充入NO,CO各0.4mol发生上述④反应,测得NO物质的量变化如图所示:
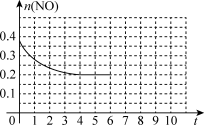
5分钟末反应达到如图所示的平衡状态,某实验人员在第6分钟继续加入0.2mol NO,0.2mol CO,0.2mol 和0.3mol
和0.3mol  ,请在图中画出到第6分钟到第9分钟末反应达到平衡状态时NO的物质的量随时间的变化曲线。
,请在图中画出到第6分钟到第9分钟末反应达到平衡状态时NO的物质的量随时间的变化曲线。_____________
(3)为了探究温度和催化剂对反应 的影响,设计了一系列实验。
的影响,设计了一系列实验。
①其它条件相同,在三个体积均为5L的密闭容器内,分别加入不同的催化剂,反应产生 的量随时间变化如图所示。
的量随时间变化如图所示。

下列说法正确的是__________ 。
A.该反应的活化能大小顺序是:
B.一定温度下,反应到达平衡时,在催化剂A作用下的转化率最高
C.当 的逆反应速率等于
的逆反应速率等于 逆反应速率的2倍时,说明该反应已经达到平衡状态
逆反应速率的2倍时,说明该反应已经达到平衡状态
D.反应到第4分钟时 的反应速率为
的反应速率为
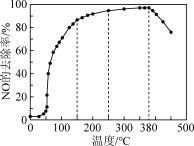
②其它条件相同,在催化剂A作用下,经过相同反应时间,NO的去除率随反应温度的变化曲线如图所示,在 范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是______________________________ ;当反应温度高于380℃时,NO的去除率迅速下降的原因可能是______________________________ 。
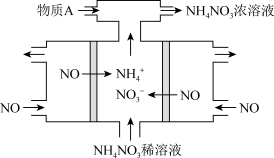
(4)电解NO可以制备氮肥 ,其工作原理如下图所示,为使电解产物全部转化为
,其工作原理如下图所示,为使电解产物全部转化为 浓溶液,需补充物质A,A是
浓溶液,需补充物质A,A是__________ ,写出电解时阴极所发生的电极反应式:__________________________ 。
(1)已知:①
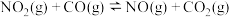

②


③


则反应④



(2)在某温度下的2L密闭容器中充入NO,CO各0.4mol发生上述④反应,测得NO物质的量变化如图所示:

5分钟末反应达到如图所示的平衡状态,某实验人员在第6分钟继续加入0.2mol NO,0.2mol CO,0.2mol
 和0.3mol
和0.3mol  ,请在图中画出到第6分钟到第9分钟末反应达到平衡状态时NO的物质的量随时间的变化曲线。
,请在图中画出到第6分钟到第9分钟末反应达到平衡状态时NO的物质的量随时间的变化曲线。(3)为了探究温度和催化剂对反应
 的影响,设计了一系列实验。
的影响,设计了一系列实验。①其它条件相同,在三个体积均为5L的密闭容器内,分别加入不同的催化剂,反应产生
 的量随时间变化如图所示。
的量随时间变化如图所示。
下列说法正确的是
A.该反应的活化能大小顺序是:

B.一定温度下,反应到达平衡时,在催化剂A作用下的转化率最高
C.当
 的逆反应速率等于
的逆反应速率等于 逆反应速率的2倍时,说明该反应已经达到平衡状态
逆反应速率的2倍时,说明该反应已经达到平衡状态D.反应到第4分钟时
 的反应速率为
的反应速率为
②其它条件相同,在催化剂A作用下,经过相同反应时间,NO的去除率随反应温度的变化曲线如图所示,在
 范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
(4)电解NO可以制备氮肥
 ,其工作原理如下图所示,为使电解产物全部转化为
,其工作原理如下图所示,为使电解产物全部转化为 浓溶液,需补充物质A,A是
浓溶液,需补充物质A,A是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】近年来雾霾天气经常肆虐北京、天津、河北等地区,其中汽车尾气和燃煤是造成空气污染的原因之一。因此研究氮氧化物的反应机理,对消除和防治环境污染有重要意义。
(1) 对于2NO(g) + 2H2(g) = N2(g) + 2H2O(g) △H = − 665 kJ/mol 的反应分三步完成:
① 2NO(g) = N2O2(g) (快)
② N2O2(g) + H2(g) = N2O(g) + H2O(g) (慢)
③______________________________ (快),请完成第③步的化学方程式。因此决定此总反应速率的是第_____ 步的反应。(填序号)
(2) 已知:H2(g) + CO2(g) = H2O(g) + CO(g) △H = + 41 kJ/mol汽车尾气的净化原理主要是用催化剂把NO与CO反应转化为两种对大气无污染的气体,试写出该反应的热化学方程式:______________ 。
该反应在一定条件下达到平衡后,为了能加快反应速率并让反应向正方向移动,可采取的措施有:( )
A.适当升高温度 B.适当降低温度 C.压缩体积增大压强 D.使用正催化剂
该反应采取上述措施重新达到平衡后K值将______ (填“增大”、“减小”和“不变”)
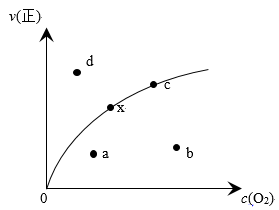
(3) 升高温度能让绝大多数的化学反应加快反应速率,但是研究发现2NO(g) + O2(g) = 2NO2(g) △H < 0 存在一些特殊现象。现有某化学小组通过实验测得不同温度下该反应速率常数k (代表反应速率的一个常数)的数值如下表:
由实验数据测到v(正)~c(O2)的关系如图所示,当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为_____ 点(填字母),并解析原因:①__________ ,②__________ 。
(1) 对于2NO(g) + 2H2(g) = N2(g) + 2H2O(g) △H = − 665 kJ/mol 的反应分三步完成:
① 2NO(g) = N2O2(g) (快)
② N2O2(g) + H2(g) = N2O(g) + H2O(g) (慢)
③
(2) 已知:H2(g) + CO2(g) = H2O(g) + CO(g) △H = + 41 kJ/mol汽车尾气的净化原理主要是用催化剂把NO与CO反应转化为两种对大气无污染的气体,试写出该反应的热化学方程式:
该反应在一定条件下达到平衡后,为了能加快反应速率并让反应向正方向移动,可采取的措施有:
A.适当升高温度 B.适当降低温度 C.压缩体积增大压强 D.使用正催化剂
该反应采取上述措施重新达到平衡后K值将
(3) 升高温度能让绝大多数的化学反应加快反应速率,但是研究发现2NO(g) + O2(g) = 2NO2(g) △H < 0 存在一些特殊现象。现有某化学小组通过实验测得不同温度下该反应速率常数k (代表反应速率的一个常数)的数值如下表:
| T(K) | k | T(K) | k | T(K) | k |
| 143 | 1.48 × 105 | 273 | 1.04 × 104 | 514 | 3.00 × 103 |
| 195 | 2.58 × 104 | 333 | 5.50 × 103 | 613 | 2.80 × 103 |
| 254 | 1.30 × 104 | 414 | 4.00 × 103 | 663 | 2.50 × 103 |

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知:Ti(s) +2Cl2(g) = TiCl4(l) △H = -804.2 kJ ·mol-1;
2Na(s) +Cl2(g) = 2NaCl(s) △H = -882.0 kJ ·mol-1
Na(s) = Na(l) △H =2.6 kJ ·mol-1
请写出用液态钠与四氯化钛置换出钛的热化学方程式__________________________ 。
(2)已知:向一个体积恒定为2L的密闭容器中充入4mol A、1mol B,发生如下反应:4A(g)+B(s) 3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。
3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。
①不能够说明该反应已达到平衡的是:________ 。
A.恒温下,容器内的压强不再变化
B.恒温下,容器内混合气体的密度不再变化
C.一定条件下,D的体积分数保持不变
D.一定条件下,单位时间内消耗4molA的同时生成1 mol B
②平衡后测得D的浓度为0.3mol·L-1,则从反应开始到平衡时,A的平均反应速率为________ ,B转化率为________ 。
(3)用活性炭还原法可以处理氮氧化物,有关反应为:2NO(g)+C(s) N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:
N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:
①在t℃下,该反应的平衡常数为________ (保留两位有效数字)。
②平衡后升高温度,再次达到平衡,测得容器中NO、N2、CO2的浓度之比为2:1:1,则该反应的
ΔH________ 0(填“>”、“<”或“=”),此时NO的转化率为________ 。
2Na(s) +Cl2(g) = 2NaCl(s) △H = -882.0 kJ ·mol-1
Na(s) = Na(l) △H =2.6 kJ ·mol-1
请写出用液态钠与四氯化钛置换出钛的热化学方程式
(2)已知:向一个体积恒定为2L的密闭容器中充入4mol A、1mol B,发生如下反应:4A(g)+B(s)
 3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。
3C(s)+4D(g)。该反应中各物质的摩尔质量(单位g·mol-1)都不一样,在一定条件下该反应2分钟达到平衡。①不能够说明该反应已达到平衡的是:
A.恒温下,容器内的压强不再变化
B.恒温下,容器内混合气体的密度不再变化
C.一定条件下,D的体积分数保持不变
D.一定条件下,单位时间内消耗4molA的同时生成1 mol B
②平衡后测得D的浓度为0.3mol·L-1,则从反应开始到平衡时,A的平均反应速率为
(3)用活性炭还原法可以处理氮氧化物,有关反应为:2NO(g)+C(s)
 N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:
N2(g)+CO2(g);△H,向某密闭容器加入一定量的活性炭和NO,在t℃下反应,有关数据如图:| NO | N2 | CO2 | |
| 起始浓度/mol•L─1 | 0.10 | 0 | 0 |
| 平衡浓度/mol•L─1 | 0.04 | 0.03 | 0.03 |
①在t℃下,该反应的平衡常数为
②平衡后升高温度,再次达到平衡,测得容器中NO、N2、CO2的浓度之比为2:1:1,则该反应的
ΔH
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值。
已知:①CH4(g)+H2O(g) CO(g)+3H2(g)ΔH=+206.2kJ·mol-1
CO(g)+3H2(g)ΔH=+206.2kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g)ΔH=-42.3kJ·mol-1
CO2(g)+H2(g)ΔH=-42.3kJ·mol-1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为___________________ 。
(2)为了探究反应条件对反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-42.3kJ·mol-1
CO2(g)+H2(g) ΔH=-42.3kJ·mol-1
的影响,某活动小组设计了三个实验,实验曲线如图3所示
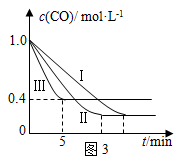
①请依据实验曲线图补充完整表格中的实验条件:X=______ ℃,Y=______ MPa。
②实验Ⅲ从开始至平衡,其平均反应速度率v(CO)=___________ mol·L-1·min-1。
③实验Ⅱ达平衡时CO的转化率________ 实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”)。
④在530℃时,平衡常数K=1,若往1L容器中投入0.2molCO(g)、0.2molH2O(g)、0.1molCO2(g) 、0.1 mol H2(g),此时化学反应将_________ (填“正向”、“逆向”或“不”) 移动。
已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g)ΔH=+206.2kJ·mol-1
CO(g)+3H2(g)ΔH=+206.2kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g)ΔH=-42.3kJ·mol-1
CO2(g)+H2(g)ΔH=-42.3kJ·mol-1(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为
(2)为了探究反应条件对反应CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-42.3kJ·mol-1
CO2(g)+H2(g) ΔH=-42.3kJ·mol-1的影响,某活动小组设计了三个实验,实验曲线如图3所示
| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol·L-1 | 3.0mol·L-1 |
| Ⅱ | X | Y | 1.0mol·L-1 | 3.0mol·L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol·L-1 | 3.0mol·L-1 |

①请依据实验曲线图补充完整表格中的实验条件:X=
②实验Ⅲ从开始至平衡,其平均反应速度率v(CO)=
③实验Ⅱ达平衡时CO的转化率
④在530℃时,平衡常数K=1,若往1L容器中投入0.2molCO(g)、0.2molH2O(g)、0.1molCO2(g) 、0.1 mol H2(g),此时化学反应将
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】雾霾中的NO对人体健康有严重危害,一种新技术用H2还原NO的反应原理为:2H2(g)+2NO(g) N2(g)+2H2O(g)△H<0.回答下列问题:
N2(g)+2H2O(g)△H<0.回答下列问题:
(1)该反应的能量变化过程如图:

△H=___________ (用图中字母表示)。
(2)该反应的机理如下:
①2NO(g) N2O2(g)(快)
N2O2(g)(快)
②N2O2(g)+H2(g) N2O(g)+H2O(g)(慢)
N2O(g)+H2O(g)(慢)
③N2O(g)+H2(g) N2(g)+H2O(g)(快)
N2(g)+H2O(g)(快)
下列各反应的活化能最大的是___________(填标号)。
(3)现向甲、乙、丙三个体积均为2L的密闭容器中加入一定量H2和NO发生反应,为研究H2和NO最合适的起始投料比,分别在T1℃、T2℃、T3℃进行实验(T1<T2<T3),结果如图。
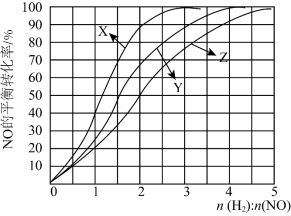
①其中T1℃的实验结果所对应的曲线是___________ (填标号);当曲线X、Y、Z达到相同的NO平衡转化率时,对应的反应温度与投料比的规律是___________ 。
②T2℃时,若充入H2、NO分别为5mol、2mol,容器内的压强为p0Pa,反应进行到5min时达平衡,该反应的平衡常数Kp=___________ Pa-1(用平衡分压代替平衡浓度写出计算表达式,分压=总压×物质的量分数)。
(4)可利用如图装置,模拟电化学方法除去雾霾中的NO、SO2,则a极为___________ 极(填“阳”或“阴”),b极的电极反应式为___________ 。
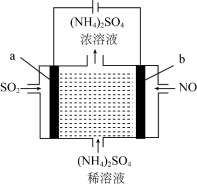
 N2(g)+2H2O(g)△H<0.回答下列问题:
N2(g)+2H2O(g)△H<0.回答下列问题:(1)该反应的能量变化过程如图:

△H=
(2)该反应的机理如下:
①2NO(g)
 N2O2(g)(快)
N2O2(g)(快)②N2O2(g)+H2(g)
 N2O(g)+H2O(g)(慢)
N2O(g)+H2O(g)(慢)③N2O(g)+H2(g)
 N2(g)+H2O(g)(快)
N2(g)+H2O(g)(快)下列各反应的活化能最大的是___________(填标号)。
| A.反应②的正反应 | B.反应①或③的正反应 |
| C.总反应的正反应 | D.总反应的逆反应 |

①其中T1℃的实验结果所对应的曲线是
②T2℃时,若充入H2、NO分别为5mol、2mol,容器内的压强为p0Pa,反应进行到5min时达平衡,该反应的平衡常数Kp=
(4)可利用如图装置,模拟电化学方法除去雾霾中的NO、SO2,则a极为

您最近半年使用:0次



