用pH大小表示溶液的酸碱性相对强弱有许多不足之处.因此,荷兰科学家HenkVanlubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为 与
与 比值的对数,用公式表示为
比值的对数,用公式表示为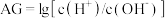 。常温下,在
。常温下,在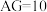 的溶液中能大量共存的离子是( )
的溶液中能大量共存的离子是( )
 与
与 比值的对数,用公式表示为
比值的对数,用公式表示为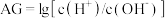 。常温下,在
。常温下,在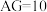 的溶液中能大量共存的离子是( )
的溶液中能大量共存的离子是( )A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
更新时间:2019-09-12 14:40:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列溶液中各组离子一定能大量共存的是
A.使甲基橙红色的溶液: 、 、 、 、 、 、 |
B.由水电离产生的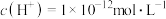 的溶液: 的溶液: 、 、 、 、 、 、 |
C.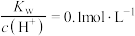 的溶液: 的溶液: 、 、 、 、 、 、 |
D.pH=8的溶液中, 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某无色溶液中存在大量的H+、NH4+、Cl-,该溶液中还可能大量存在的离子是( )
| A.Al3+ | B.Cu2+ | C.CO32- | D.OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】食用磷酸钾(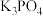 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:
ⅰ. ,控制
,控制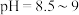 左右;
左右;
ⅱ.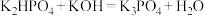 ,控制pH=14左右。
,控制pH=14左右。
已知常温下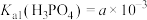 、
、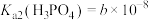 、
、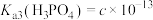 。
。
常温下,下列说法正确的是
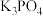 )可用作食品乳化剂,工业制备原理为:
)可用作食品乳化剂,工业制备原理为:ⅰ.
 ,控制
,控制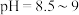 左右;
左右;ⅱ.
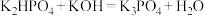 ,控制pH=14左右。
,控制pH=14左右。已知常温下
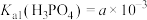 、
、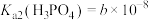 、
、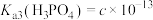 。
。常温下,下列说法正确的是
A. 溶液中由水电离出的氢离子浓度一定大于 溶液中由水电离出的氢离子浓度一定大于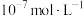 |
B.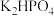 溶液中 溶液中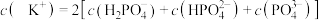 |
C.向 溶液中滴加少量KOH溶液,反应的离子方程式为 溶液中滴加少量KOH溶液,反应的离子方程式为 |
D.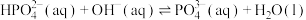 的化学平衡常数为10c 的化学平衡常数为10c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,有下列四种溶液:① 的
的 溶液 ②
溶液 ② 的HCl溶液 ③
的HCl溶液 ③ 的氨水 ④
的氨水 ④ 的NaOH溶液,下列有关说法正确的是
的NaOH溶液,下列有关说法正确的是
 的
的 溶液 ②
溶液 ② 的HCl溶液 ③
的HCl溶液 ③ 的氨水 ④
的氨水 ④ 的NaOH溶液,下列有关说法正确的是
的NaOH溶液,下列有关说法正确的是A.四种溶液的Kw相同,由水电离的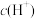 :①=③>②=④ :①=③>②=④ |
| B.向等体积的四种溶液中分别加入100mL水后,溶液的pH:③>④>②>① |
| C.①、②、④溶液分别与足量铝粉反应,生成H2的量:①最大 |
D.将②、③两种溶液混合后,若 ,消耗溶液的体积为:③>② ,消耗溶液的体积为:③>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】甲胺(CH3NH2)的性质与氨气相似。已知pKb= - lgKb,pKb(CH3NH2·H2O)=3.4,pKb(NH3·H2O)=4.8。常温下,向10.00 mL 0.1000mol/L的甲胺溶液中滴加0.0500 mol/L的稀硫酸溶液中c(OH-)的负对数[pOH= -lgc(OH-)]与所加稀硫酸溶液的体积(V)的关系如图所示。

下列说法错误的是

下列说法错误的是
A.甲胺溶于水后存在平衡:CH3NH2+H2O CH3NH CH3NH +OH- +OH- |
| B.A、B、C三点对应的溶液中,水电离出来的c(H+):C>B>A |
C.A、B、C、D四点对应的溶液中,(CH3NH )的大小顺序:D>C>B>A )的大小顺序:D>C>B>A |
| D.B点对应的溶液的pOH>3.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知25 ℃时,K=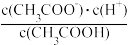 =1.8×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是
=1.8×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是
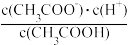 =1.8×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是
=1.8×10-5,其中K是该温度下CH3COOH的电离平衡常数。下列说法正确的是| A.向该溶液中加入一定量的硫酸,K增大 |
| B.在绝热的容器里,向少量CH3COOH溶液中加入NaOH固体,K增大 |
| C.向CH3COOH溶液中加入少量水,K增大 |
| D.向CH3COOH溶液中加入少量氢氧化钠溶液,K增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,向10 mL 0.01 mol·L-1的NaCN溶液中逐滴加入0.01mol·L-1的盐酸,其pH变化曲线如图甲所示,溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如图乙所示。
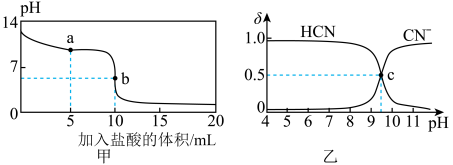
| A.图甲中a点对应的溶液中:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) |
| B.图甲中b点对应的溶液中:c(Na+)+c(H+)=0.01mol·L-1+c(OH-)+c(CN-) |
| C.25℃时 ,HCN的电离常数的数量级为10-9 |
| D.图乙中pH=7的溶液中:c(Cl-)=c(HCN) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-4,将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
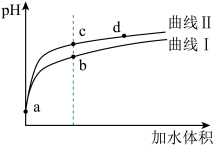

| A.b点酸的总物质的量浓度小于c点酸的总物质的量浓度 |
B.酸的电离程度:c>d;a点溶液中,c(NO )<c(CH3COO-) )<c(CH3COO-) |
| C.导电能力强弱:d>c;a点Ka的数值比d点Ka的数值大 |
| D.c点和d点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,Ka(HCOOH)=1.77×10−4,Ka(CH3COOH)=1.75×10−5,Kb(NH3·H2O) =1.75×10−5,下列说法正确的是
| A.相同体积pH均为3的HCOOH和CH3COOH溶液,中和NaOH的能力相同 |
| B.0.2 mol·L-1 HCOOH与0.1 mol·L-1 NaOH 等体积混合后:c(HCOO−) + c(OH−) < c(HCOOH) + c(H+) |
| C.浓度均为0.1 mol·L−1的 HCOONa和NH4Cl 溶液中阳离子的物质的量浓度之和:前者大于后者 |
D.将CH3COONa溶液从20℃升温至30℃,溶液中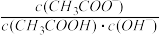 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,将NaOH固体逐渐加到某浓度的一元酸HA溶液中,测得混合溶液的pH与微粒浓度lg 的变化关系如图所示。下列叙述不正确的是( )
的变化关系如图所示。下列叙述不正确的是( )

 的变化关系如图所示。下列叙述不正确的是( )
的变化关系如图所示。下列叙述不正确的是( )
| A.Ka(HA)的数量级为10-5 |
| B.A点所表示的溶液中:c(HA)>c(A-)>c(Na+)>c(OH-) |
| C.B点所表示的溶液中:c(H+)=c(HA)+c(OH-)-c(Na+) |
| D.从A点到C点,水的电离程度先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NaH2A—Na2HA溶液是人体存在的缓冲溶液。常温下,H3A溶液中各微粒组成随着pH而变化,溶液中A3-、HA2-、H2A-、H3A浓度所占分数(δ)随pH变化的关系如图所示。
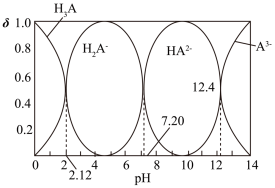
下列说法错误的是

下列说法错误的是
| A.0.1mol/LNaH2A溶液显酸性 |
| B.H3A+HA2—=2H2A—的平衡常数K=105.08 |
| C.将等物质的量的Na2HA和NaH2A配制成溶液,pH=7.20 |
| D.pH=12.40时,存在关系:c(H+)<2c(HA2—)+c(H2A—)+3c(A3—)+c(OH—) |
您最近一年使用:0次



