以“坚持围绕锂电新能源,推动新时代动力电池高质量发展”为主题的2018第二届深圳国际锂电技术展览会于12月10日在深圳开幕,倾力打造高端锂电产业平台。工业上合成锂离子电池的正极材料LiFePO4的原理是2FePO4+Li2CO3+H2C2O4 2LiFePO4+H2O↑+3CO2↑。
2LiFePO4+H2O↑+3CO2↑。
回答下列问题:
(1)基态Li+的核外电子云轮廓图的形状为___________ 。画出基态Li原子的电子排布图___________ 。
(2)从核外电子排布分析,Fe3+比Fe2+稳定的原因是___________ 。
(3)已知草酸的结构简式为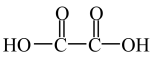 ,其中碳原子的杂化类型是
,其中碳原子的杂化类型是___________ ;9.0 g草酸中含σ键的数目为___________ 。
(4)PO 的立体构型是
的立体构型是___________ ;与PO 互为等电子体的分子有
互为等电子体的分子有___________ (写两种)。
(5)FeO晶胞的结构类似于NaCl晶胞,其中Fe2+构成面心立方结构如图所示。已知FeO晶胞的棱长为a cm,NA为阿伏加德罗常数的值。
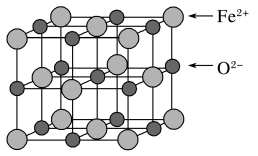
①与O2-等距离且最近的Fe2+构成的空间结构是正八面体,该正八面体的边长为___________ pm。
②FeO晶体的密度为___________ g·cm-3(用含a、NA的代数式表示)。
 2LiFePO4+H2O↑+3CO2↑。
2LiFePO4+H2O↑+3CO2↑。回答下列问题:
(1)基态Li+的核外电子云轮廓图的形状为
(2)从核外电子排布分析,Fe3+比Fe2+稳定的原因是
(3)已知草酸的结构简式为
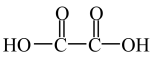 ,其中碳原子的杂化类型是
,其中碳原子的杂化类型是(4)PO
 的立体构型是
的立体构型是 互为等电子体的分子有
互为等电子体的分子有(5)FeO晶胞的结构类似于NaCl晶胞,其中Fe2+构成面心立方结构如图所示。已知FeO晶胞的棱长为a cm,NA为阿伏加德罗常数的值。

①与O2-等距离且最近的Fe2+构成的空间结构是正八面体,该正八面体的边长为
②FeO晶体的密度为
更新时间:2021-01-14 19:13:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】根据要求回答下列问题:
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是_________ 。
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:________ (用序号表示)。
(3)下列属于氧原子激发态的轨道表示式的有___________ (填字母)。_________ ,位于在周期表______ 区(填s、p、d或ds)。
(5)基态Si原子中,电子占据的最高能层符号为________ 。
(6)基态S原子的原子核外电子有______ 种空间运动状态,其能量最高的电子电子云轮廓图为______ 形。
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:________ 。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①O2- ②Al3+ ③Cl- ④Ca2+的半径由大到小排列为:
(3)下列属于氧原子激发态的轨道表示式的有
a.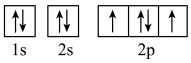 b.
b.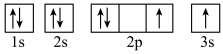
c.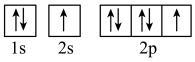 d.
d.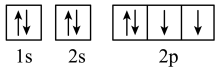
(5)基态Si原子中,电子占据的最高能层符号为
(6)基态S原子的原子核外电子有
(7)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】第四周期过渡元素常用于制造催化剂。请回答下列问题:
(1)石墨烯氧化锰复合催化剂能够使甲醛(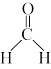 )转化生成
)转化生成 和
和 。
。
① 的基态原子的价层电子的轨道表示式为
的基态原子的价层电子的轨道表示式为_______ 。
② 是制备这种催化剂的原料,
是制备这种催化剂的原料, 中阴离子的立体构型为
中阴离子的立体构型为_______ 。
③在反应所涉及的物质中,属于极性分子的有_______ (填标号)。
A. B.
B. C.
C.
(2)铜可用作醇氧化反应的催化剂。例如苯甲醇氧化成苯甲醛:
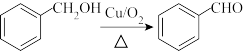 。
。
① 原子位于元素周期表中的
原子位于元素周期表中的_______ 区。
②苯甲醇分子中的碳原子的杂化类型为_______ 。
③在常压下,苯甲醇的沸点比苯甲醛的沸点高,主要原因是_______ 。
(1)石墨烯氧化锰复合催化剂能够使甲醛(
 )转化生成
)转化生成 和
和 。
。①
 的基态原子的价层电子的轨道表示式为
的基态原子的价层电子的轨道表示式为②
 是制备这种催化剂的原料,
是制备这种催化剂的原料, 中阴离子的立体构型为
中阴离子的立体构型为③在反应所涉及的物质中,属于极性分子的有
A.
 B.
B. C.
C.
(2)铜可用作醇氧化反应的催化剂。例如苯甲醇氧化成苯甲醛:
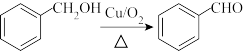 。
。①
 原子位于元素周期表中的
原子位于元素周期表中的②苯甲醇分子中的碳原子的杂化类型为
③在常压下,苯甲醇的沸点比苯甲醛的沸点高,主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铍及其化合物的应用正日益被重视。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为____________ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有________ (填字母)。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.铍、镁和铝与氯气形成的化合物晶体类型相同
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(1551K)比铝的熔点(930K)高,原因是____________________ 。
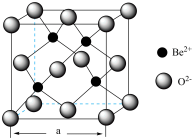
(4)BeO立方晶胞如图所示,若BeO晶体的密度为dg·cm-3,则晶胞边长为________ nm。
(1)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子的轨道表示式为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.铍、镁和铝与氯气形成的化合物晶体类型相同
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(1551K)比铝的熔点(930K)高,原因是
(4)BeO立方晶胞如图所示,若BeO晶体的密度为dg·cm-3,则晶胞边长为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】金属、非金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)FeCl3溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,Fe3+ 的M层电子排布式为_________ ;
②此配离子中配体为C6H10O3,则该配离子的化学式为_________ ,配位数为_______ 。
(2)杂化轨道理论认为六配位的正八面体构型是由中心原子提供2个d轨道、1个s轨道和3个p轨道形成的杂化轨道,根据中心原子提供的d轨道是内层的还是外层的分为内轨型和外轨型。Fe(CN) 属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取
属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取_________ 杂化。
(3)科学家合成了一种阳离子为“N ”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为“N8”的离子晶体,写出“N
”化学式为“N8”的离子晶体,写出“N ”结构式
”结构式__________ ,写出一种与阴离子互为等电子体的分子的化学式:_________ 。
(4)N4H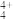 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H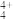 中含有
中含有______ 个σ键。
(5)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为______ 。若晶胞底边长为a nm,高为c nm,则这种磁性氮化铁的晶体密度为 ___________ g/㎝3(用含a、c和NA的式子表示)。

(1)FeCl3溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,Fe3+ 的M层电子排布式为
②此配离子中配体为C6H10O3,则该配离子的化学式为
(2)杂化轨道理论认为六配位的正八面体构型是由中心原子提供2个d轨道、1个s轨道和3个p轨道形成的杂化轨道,根据中心原子提供的d轨道是内层的还是外层的分为内轨型和外轨型。Fe(CN)
 属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取
属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取(3)科学家合成了一种阳离子为“N
 ”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为“N8”的离子晶体,写出“N
”化学式为“N8”的离子晶体,写出“N ”结构式
”结构式(4)N4H
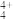 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H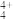 中含有
中含有(5)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
【推荐2】高氯酸三碳酰肼合镍的化学式为[NiA3](ClO4)2,它是一种新型的起爆药,可由NiO、HClO4及有机物A化合而成,A称为碳酰肼,组成为CO(N2H3)2。请回答下列问题:
(1)Ni在周期表中的位置是________________ ,Ni2+核外有_________ 个未成对电子。
(2)ClO 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为_______ ,与Cl 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是_________ (填化学式,分子、离子各填一种)。
(3)1.8 g A分子中含有σ键的数目为__________________ 。(用NA表示)
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有_____________ 个。已知NiO晶胞的密度为ρ g·cm−3,则晶胞边长为______________ cm。
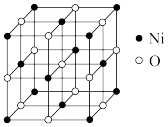
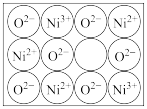
②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为____________ (保留4位有效数字)。
(1)Ni在周期表中的位置是
(2)ClO
 中氯原子的轨道杂化类型为
中氯原子的轨道杂化类型为 互为等电子体的分子、离子分别是
互为等电子体的分子、离子分别是(3)1.8 g A分子中含有σ键的数目为
(4)①NiO晶胞结构如图所示,与Ni2+最近且等距离的Ni2+有

②天然的和绝大部分人工制备的晶体都存在各种缺陷。某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其晶体仍呈电中性,但化合物中Ni和O的个数比却发生了变化,经测定某氧化镍晶体样品中N(Ni2+)∶N(Ni3+)=91∶6,则该晶体中氧元素的质量分数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx分别氧化为SO42-和NO3-,NOx也可在其他条件下被还原为N2。
(1)Fe3+基态核外电子排布式为__________________ 。
(2)与O3分子互为等电子体的一种阴离子为_____________ (填化学式)。
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=__________________ 。
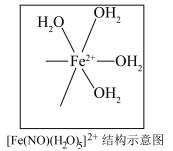
(4)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体__________________________
(1)Fe3+基态核外电子排布式为
(2)与O3分子互为等电子体的一种阴离子为
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=
(4)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】元素及其化合物在生活及生产中有很多重要用途。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)基态碳原子价电子的电子轨道表达式为____ ,第一电离能Ga____ As(填“>”、 “<”、“=”)。
(2)BN和GaAs都是原子晶体,它们的硬度和熔点BN>GaAs,原因是________________ 。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。 (CN)2分子中氮原子的轨道杂化类型为_____ ,σ 键与 π 键数目之比为_______ ; (SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H—N=C=S),其原因是_________ 。
(4)①卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为_____________ ;②一定条件下(SCN)2可氧化为CO32—和SO32—等离子,其中SO32—的立体构型为_________ 。
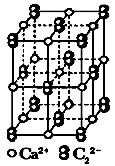
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图1 所示),CaC2 晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。写出与C22﹣互为等电子体的微粒符号________ 、_______ ;此晶体中 1 个 C22﹣周围距离最近的Ca2+为______ 个;若该晶胞的边长为a、a、b(nm),则该晶体的密度为______ g·cm-3(写出表达式)。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)基态碳原子价电子的电子轨道表达式为
(2)BN和GaAs都是原子晶体,它们的硬度和熔点BN>GaAs,原因是
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。 (CN)2分子中氮原子的轨道杂化类型为
(4)①卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图1 所示),CaC2 晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。写出与C22﹣互为等电子体的微粒符号

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】第四周期某些过渡元素在工业生产中有着极其重要的作用。
Ⅰ.中国锰矿资源较多,分布广泛。
(1)写出基态锰原子的价电子排布图:___________ 。
(2) 用于
用于 分解制氧气的催化剂,
分解制氧气的催化剂, 中氧原子的杂化轨道类型为
中氧原子的杂化轨道类型为___________ 。
Ⅱ.铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1) 常作净水剂和补铁剂,SO
常作净水剂和补铁剂,SO 的立体构型是
的立体构型是___________ 。
(2)铁氰化钾 是检验
是检验 的重要试剂。
的重要试剂。
①写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式___________ 。
②铁氰化钾中存在的化学键有___________ (填字母标号)。
A.离子键 B.σ键 C.π键 D.氢键 E。金属键
Ⅲ.锌在工业中有重要作用,也是人体必需的微量元素。硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图所示。
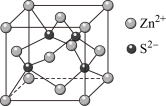
(1)该晶胞中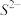 的配位数为
的配位数为___________ 。
(2)若晶胞参数为 ,则该晶体密度的计算式为
,则该晶体密度的计算式为___________  (用
(用 表示阿伏加德罗常数的值,不用化简)。
表示阿伏加德罗常数的值,不用化简)。
Ⅰ.中国锰矿资源较多,分布广泛。
(1)写出基态锰原子的价电子排布图:
(2)
 用于
用于 分解制氧气的催化剂,
分解制氧气的催化剂, 中氧原子的杂化轨道类型为
中氧原子的杂化轨道类型为Ⅱ.铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)
 常作净水剂和补铁剂,SO
常作净水剂和补铁剂,SO 的立体构型是
的立体构型是(2)铁氰化钾
 是检验
是检验 的重要试剂。
的重要试剂。①写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式
②铁氰化钾中存在的化学键有
A.离子键 B.σ键 C.π键 D.氢键 E。金属键
Ⅲ.锌在工业中有重要作用,也是人体必需的微量元素。硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图所示。

(1)该晶胞中
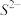 的配位数为
的配位数为(2)若晶胞参数为
 ,则该晶体密度的计算式为
,则该晶体密度的计算式为 (用
(用 表示阿伏加德罗常数的值,不用化简)。
表示阿伏加德罗常数的值,不用化简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钴元素的用途广泛,据古文献记载:宜德时期青花瓷使用的颜料“苏勃泥青"是从一种进口钴毒矿[主要成分:(FeCo)xAsS]中提取出来的。
(1)Co的价电子排布式为_______
(2)无水CoCl2的熔点是735°C ,沸点1049°C ,CoCl2属于_______ 晶体;砷酸(H3AsO4)分子中As原子的杂化方式为_______ 杂化;砷酸根离子的空间构型为_______ ;第一电离能I1(As)_______ I1(Se)(填“大于”或“小于")。
(3)[Co(NH3)4(H2O)2]Cl3是一种特殊的配合物,其中心离子的配位数是_______ ,每个[Co(NH3)4(H2O)2]3+所含共价键的数目是_______ ,配体NH3的熔沸点大于同族元素氢化物AsH3的原因是_______ 。
(4)钴氰化钾K3[Co(CN)6]是一种浅黄色单斜棱晶体,与配体CN-原子总数相等的等电子体是_______ 。
(5)金属钴晶体的晶胞结构如图所示,其中正六边形的面积为apm2,棱长为bpm;每个Co距离最近且相等的Co原子数目为_______ ; 设阿伏加德罗常数的值为NA,则该晶体的密度为_______ (用含a、b、NA的代数式表示) g·cm-3。

(1)Co的价电子排布式为
(2)无水CoCl2的熔点是735°C ,沸点1049°C ,CoCl2属于
(3)[Co(NH3)4(H2O)2]Cl3是一种特殊的配合物,其中心离子的配位数是
(4)钴氰化钾K3[Co(CN)6]是一种浅黄色单斜棱晶体,与配体CN-原子总数相等的等电子体是
(5)金属钴晶体的晶胞结构如图所示,其中正六边形的面积为apm2,棱长为bpm;每个Co距离最近且相等的Co原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。预计在未来20年里,不可能有替代钕铁硼磁铁的磁性材料出现。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他稀土原料。
(1)钕(Nd)为60号元素,在周期表中第______ 周期;基态铁原子的外围电子排布式为______
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。
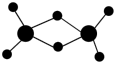
①已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于_________ 分子(填“极性”或“非极性”),分子中A1原采取______ 杂化。
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有_____ (填选项字母)。
A.离子键B.共价键C.金属键D.配位键E.氢键
(3) B元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为______ (用元素符号表示)。B元素可在一定条件下生成H3O+•[B(OH)F3]-,该化合物中电负性最大的元素的原子中,所有能层电子的电子云轮廓图形状有______ 种
(4)因材料中含有大量的钕和铁,容易锈蚀是它的一大弱点。可电镀镍(Ni)、锌(Zn)等进行表面涂层处理。已知Ni可以形成[Ni(NH3)6]Cl2,该配合物中配体分子的空间构型为_______ 。
(5)已知立方BN晶体硬而脆,其晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为anm,晶体的密度为bg·cm-3,则阿伏加 德罗常数为_________ mol-1(用含a、b的代数式表示)

(1)钕(Nd)为60号元素,在周期表中第
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。

①已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于
②Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有
A.离子键B.共价键C.金属键D.配位键E.氢键
(3) B元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为
(4)因材料中含有大量的钕和铁,容易锈蚀是它的一大弱点。可电镀镍(Ni)、锌(Zn)等进行表面涂层处理。已知Ni可以形成[Ni(NH3)6]Cl2,该配合物中配体分子的空间构型为
(5)已知立方BN晶体硬而脆,其晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为anm,晶体的密度为bg·cm-3,则阿伏加 德罗常数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】过渡元素Ti、Mn、Fe、Cu等可与C、H、O形成多种化合物。请回答下列问题:
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于________ 区。某一次性电池负极材料是Zn,正极材料是Mn的一种常见氧化物,放电后生成MnOOH,电解质是KOH。该电池的正极反应式为__________________________ 。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的最高能层符号为________ ,该能层具有的原子轨道数为________ 。BH4-的立体构型是________ 。
(3)单质Cu的晶体类型为______ ,晶体中组成微粒通过________ 作用形成面心立方密堆积,其中Cu原子的配位数为______ 。在Cu的催化作用下,乙醇可被空气中氧气氧化为乙醛,乙醛分子中碳原子的杂化方式是________ ,乙醛分子中∠HCO的键角________ 乙醇分子中∠HCO的键角(填“大于”、“等于”或“小于”)。
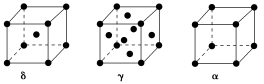
(4)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为________ ,δ、γ、α三种晶胞的边长之比为________ 。
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的最高能层符号为
(3)单质Cu的晶体类型为
(4)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氧化锌在液晶显示器、薄膜晶体管、发光二极管等产品中均有应用,常用下列三种锌盐为原料经高温分解制备。
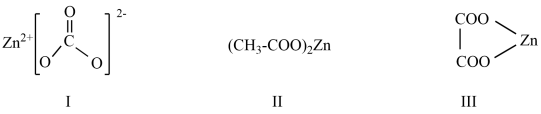
回答下列问题:
(1)Zn为30号元素,它在元素周期表中的位置是_______ 。
(2)原料Ⅰ中阴离子空间结构为_______ ,其等电子体为_______ (写出1种即可)。
(3)原料Ⅱ、Ⅲ阴离子对应的酸沸点较高的是_______ (写结构简式),原因是_______ 。
(4)关于以上几种锌盐说法正确的是_______。
(5)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。

①图a不是纤锌矿型ZnO的晶胞单元,原因是_______ 。
②图b闪锌矿型属于立方晶胞,原子1的坐标为 ,则原子2的坐标为
,则原子2的坐标为_______ 。
③图 的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为
的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为_______ ,其晶胞参数为a nm,阿伏加德罗常数的值为NA,则晶体密度为_______ g/cm3(列出计算式)。
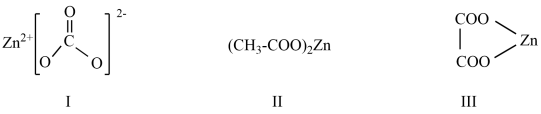
回答下列问题:
(1)Zn为30号元素,它在元素周期表中的位置是
(2)原料Ⅰ中阴离子空间结构为
(3)原料Ⅱ、Ⅲ阴离子对应的酸沸点较高的是
(4)关于以上几种锌盐说法正确的是_______。
| A.化合物Ⅱ中电负性最大的元素是O |
| B.化合物Ⅱ中所有C原子的杂化形式均为sp3 |
| C.化合物Ⅲ中只存在离子键和极性共价键 |
| D.化合物Ⅰ阴离子中σ键和π键数目比为2:1 |

①图a不是纤锌矿型ZnO的晶胞单元,原因是
②图b闪锌矿型属于立方晶胞,原子1的坐标为
 ,则原子2的坐标为
,则原子2的坐标为③图
 的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为
的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为
您最近一年使用:0次



