盐在化学工业中有重要的应用,请回答下列问题。
(1)用离子方程式表示明矾可作净水剂的原因:_______ 。
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为_______ 。
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是_______ (用序号表示)
(4)25℃,两种酸的电离平衡常数如下表:
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为_______ ;
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式_______ 。
③向NaHS溶液中通入少量CO2时反应的离子方程式_______ 。
(1)用离子方程式表示明矾可作净水剂的原因:
(2)常温下,在pH=3的硫酸与pH=11的Na2S溶液中,水电离出来的c(OH-)之比为
(3)物质的量浓度相等的下列溶液①NH4Cl;②NH4HSO4;③(NH4)2SO4;④CH3COONH4;⑤NH3·H2O,溶液中的pH由大到小的顺序是
(4)25℃,两种酸的电离平衡常数如下表:
| H2SO3 | H2CO3 | H2S | |
| Ka1 | 1.3×10-2 | 4.2×10-7 | 1.9×10-8 |
| Ka2 | 6.3×10-8 | 5.6×10-11 | 1.0×10-12 |
①0.10mol/L NaHSO3溶液中离子浓度由大到小的顺序为
②向Na2S溶液中通入足量二氧化硫时反应的离子方程式
③向NaHS溶液中通入少量CO2时反应的离子方程式
更新时间:2021-02-10 22:21:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某温度时,纯水的pH为6。
(1)该温度下水的离子积Kw为_______ mol2·L-2,此时pH=7的溶液______ (填“酸性”“中性”或“碱性”)。
(2)该温度下,0.05 mol·L-1的Ba(OH)2溶液的pH=________ ,该溶液中由水电离出的c(H+)的大小为_____________ 。
(3)将此温度下pH=10的NaOH溶液与pH=2的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的PH=__________ 。
(4)将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合。若所得的混合溶液pH=10,则a:b=_____________ 。
(5)对此温度下pH均为3的盐酸和醋酸溶液进行微热(忽略溶质的挥发),溶液pH的变化分别为(填“增大” “减小”或 “不变”):盐酸________ ,醋酸________ 。
(1)该温度下水的离子积Kw为
(2)该温度下,0.05 mol·L-1的Ba(OH)2溶液的pH=
(3)将此温度下pH=10的NaOH溶液与pH=2的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的PH=
(4)将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合。若所得的混合溶液pH=10,则a:b=
(5)对此温度下pH均为3的盐酸和醋酸溶液进行微热(忽略溶质的挥发),溶液pH的变化分别为(填“增大” “减小”或 “不变”):盐酸
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)常温下,某溶液中由水电离出的c(OH-)=1.0×10-10mol•L-1,该溶液可以是______ (填字母)。
a.pH=4的CH3COOH b.pH=10的NaOH c.pH=2的H2SO4
(2)某温度下,向pH=6的蒸馏水中加入2.3g的金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=______ 。
(3)常温下,向pH=4的醋酸和c(H+)=1.0×10-4mol•L-1的稀硫酸中分别加入大小、质量相同的金属锌,反应刚开始时,产生H2的速率前者与后者相比是______ (填字母)。
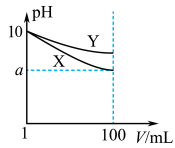
(4)常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是______ (填字母)。
(5)常温下,分别用pH为10和11的氨水中和等量的盐酸,若所需氨水的体积分别为V1和V2,则V1______ 10V2(填“>”“=”或“<”)。
(6)常温下,将pH=6的硫酸稀释1000倍,稀释后溶液中c(H+):c(SO )=
)=______ 。
(1)常温下,某溶液中由水电离出的c(OH-)=1.0×10-10mol•L-1,该溶液可以是
a.pH=4的CH3COOH b.pH=10的NaOH c.pH=2的H2SO4
(2)某温度下,向pH=6的蒸馏水中加入2.3g的金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=
(3)常温下,向pH=4的醋酸和c(H+)=1.0×10-4mol•L-1的稀硫酸中分别加入大小、质量相同的金属锌,反应刚开始时,产生H2的速率前者与后者相比是
| A.一样快 | B.前者快 | C.后者快 | D.无法比较 |
(4)常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是

| A.X、Y两种碱溶液中溶质的物质的量浓度一定相等 |
| B.稀释后,两种碱溶液中和硫酸的能力Y大于X |
| C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积Vx>VY |
| D.若8<a<10,则X、Y都是弱碱 |
(5)常温下,分别用pH为10和11的氨水中和等量的盐酸,若所需氨水的体积分别为V1和V2,则V1
(6)常温下,将pH=6的硫酸稀释1000倍,稀释后溶液中c(H+):c(SO
 )=
)=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用化学反应原理研究溶液的组成与性质具有重要意义,已知水存在如下平衡:H2O H++OH-△H>0,现有常温条件下甲、乙、丙三种溶液,甲为0.1mol/LNaOH溶液,乙为0.1mol/LCH3COOH,丙为0.1mol/LAlCl3溶液。试回答下列问题:
H++OH-△H>0,现有常温条件下甲、乙、丙三种溶液,甲为0.1mol/LNaOH溶液,乙为0.1mol/LCH3COOH,丙为0.1mol/LAlCl3溶液。试回答下列问题:
(1)甲溶液的pH=___ 。甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为___ 。
(2)将此乙溶液加水稀释100倍,其他条件不变,其pH变化小于2的原因是___ 。在此过程中,随着加水体积的增加而逐渐增大的是___ (填写序号)
A. B.
B.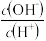 C.c(H+)和c(OH–)的乘积 D.c(H+)
C.c(H+)和c(OH–)的乘积 D.c(H+)
(3)丙溶液中存在的水解平衡为___ (用离子方程式表示)。
(4)室温下,向20.00mL乙溶液中逐滴加入甲溶液,溶液pH的变化曲线如图所示。请分析:

①pH=7时,溶液中c(CH3COO-)、c(Na+)二者之间的关系为___ 。
②下列关系式中,能同时代表图中a、b、c三点所对应溶液中微粒之间浓度关系的是___ 。
A.c(CH3COO-)+c(CH3COOH)=0.1mol/L
B.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.c(Na+)-c(CH3COO-)=c(OH-)-c(H+)
D.c(CH3COO-)+c(CH3COOH)>c(Na+)
 H++OH-△H>0,现有常温条件下甲、乙、丙三种溶液,甲为0.1mol/LNaOH溶液,乙为0.1mol/LCH3COOH,丙为0.1mol/LAlCl3溶液。试回答下列问题:
H++OH-△H>0,现有常温条件下甲、乙、丙三种溶液,甲为0.1mol/LNaOH溶液,乙为0.1mol/LCH3COOH,丙为0.1mol/LAlCl3溶液。试回答下列问题:(1)甲溶液的pH=
(2)将此乙溶液加水稀释100倍,其他条件不变,其pH变化小于2的原因是
A.
 B.
B.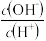 C.c(H+)和c(OH–)的乘积 D.c(H+)
C.c(H+)和c(OH–)的乘积 D.c(H+)(3)丙溶液中存在的水解平衡为
(4)室温下,向20.00mL乙溶液中逐滴加入甲溶液,溶液pH的变化曲线如图所示。请分析:

①pH=7时,溶液中c(CH3COO-)、c(Na+)二者之间的关系为
②下列关系式中,能同时代表图中a、b、c三点所对应溶液中微粒之间浓度关系的是
A.c(CH3COO-)+c(CH3COOH)=0.1mol/L
B.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.c(Na+)-c(CH3COO-)=c(OH-)-c(H+)
D.c(CH3COO-)+c(CH3COOH)>c(Na+)
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁器的修复是文物保护的重要课题。
(1)潮湿环境中,铁器发生电化学腐蚀的负极反应式是_______ 。
(2)铁器表面氧化层的成分有多种,部分性质见表:
在有氧条件下, 在含
在含 溶液中会转化为
溶液中会转化为 ,写出该离子方程式
,写出该离子方程式_______ 。
(3)化学修复可以使 转化为
转化为 致密保护层:用
致密保护层:用 和
和 混合溶液浸泡锈蚀的铁器,一段时间后取出,再用
混合溶液浸泡锈蚀的铁器,一段时间后取出,再用 溶液反复洗涤。
溶液反复洗涤。
① 在
在 的作用下转变为
的作用下转变为 ,推测溶解度
,推测溶解度
_______  (填“
(填“ ”或“
”或“ ”)
”)
②关于Na2SO3和NaOH混合溶液的说法正确的是_______ 。
A.该溶液显碱性,水的电离一定被抑制
B.往溶液中逐滴滴加盐酸至过量,保持温度不变,水的电离经历先减小后增大的过程
C.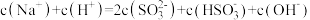
D.若 和
和 物质的量之比为
物质的量之比为 ,则有:
,则有: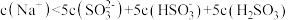
(1)潮湿环境中,铁器发生电化学腐蚀的负极反应式是
(2)铁器表面氧化层的成分有多种,部分性质见表:
| 成分 |  |  |  |
| 性质 | 致密 | 疏松 | 疏松 |
在有氧条件下,
 在含
在含 溶液中会转化为
溶液中会转化为 ,写出该离子方程式
,写出该离子方程式(3)化学修复可以使
 转化为
转化为 致密保护层:用
致密保护层:用 和
和 混合溶液浸泡锈蚀的铁器,一段时间后取出,再用
混合溶液浸泡锈蚀的铁器,一段时间后取出,再用 溶液反复洗涤。
溶液反复洗涤。①
 在
在 的作用下转变为
的作用下转变为 ,推测溶解度
,推测溶解度
 (填“
(填“ ”或“
”或“ ”)
”)②关于Na2SO3和NaOH混合溶液的说法正确的是
A.该溶液显碱性,水的电离一定被抑制
B.往溶液中逐滴滴加盐酸至过量,保持温度不变,水的电离经历先减小后增大的过程
C.
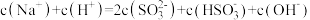
D.若
 和
和 物质的量之比为
物质的量之比为 ,则有:
,则有: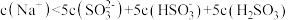
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】25℃时,下表是几种弱酸的电离平衡常数,回答下列问题。
(1)某温度时,水的 ,
, 的NaOH溶液aL与
的NaOH溶液aL与 的
的 溶液bL混合,若所得混合溶液
溶液bL混合,若所得混合溶液 ,则a∶b为
,则a∶b为_______ 。
(2)25℃时,某NaHB与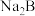 混合溶液的
混合溶液的 ,求
,求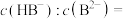
_______ 。
(3)浓度均为 的
的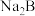 与
与 的混合溶液中,
的混合溶液中,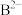 、
、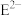 、
、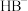 、
、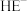 浓度从大到小的顺序为
浓度从大到小的顺序为_______ 。
(4)现有浓度为0.02mol/L的HA溶液与0.01mol/LNaOH溶液等体积混合后,下列关系正确的是_______(填标号)。
| 化学式 | HA |  | 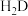 | 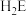 |
| 电离常数 |  | 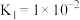 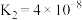 | 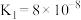 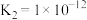 | 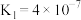  |
(1)某温度时,水的
 ,
, 的NaOH溶液aL与
的NaOH溶液aL与 的
的 溶液bL混合,若所得混合溶液
溶液bL混合,若所得混合溶液 ,则a∶b为
,则a∶b为(2)25℃时,某NaHB与
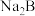 混合溶液的
混合溶液的 ,求
,求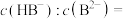
(3)浓度均为
 的
的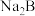 与
与 的混合溶液中,
的混合溶液中,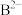 、
、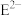 、
、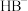 、
、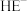 浓度从大到小的顺序为
浓度从大到小的顺序为(4)现有浓度为0.02mol/L的HA溶液与0.01mol/LNaOH溶液等体积混合后,下列关系正确的是_______(填标号)。
A.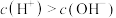 | B.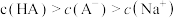 |
C. | D.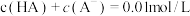 |
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D四种无色溶液,它们分别是一定浓度的AlCl3溶液、盐酸、氨水、Na2SO4溶液中的一种。已知A、B溶液中水的电离程度相同,A、C溶液的pH相同。请回答下列问题:
(1)A是___ ,D是___ 。
(2)写出足量B溶液与少量C溶液混合后发生反应的离子方程式:___ 。
(3)A、B溶液等体积混合后,溶液中各离子浓度由大到小的顺序是:___ 。
(1)A是
(2)写出足量B溶液与少量C溶液混合后发生反应的离子方程式:
(3)A、B溶液等体积混合后,溶液中各离子浓度由大到小的顺序是:
您最近半年使用:0次



