下列叙述正确的是
| A.pH=3的醋酸溶液,稀释至10倍时溶液的pH<4 |
| B.等浓度的醋酸溶液与氢氧化钠溶液等体积混合后pH=7 |
| C.等体积pH均为3的醋酸和盐酸分别与足量Zn反应,盐酸产生的H2多 |
| D.室温下,测得pH=5的NaHSO4溶液与pH=9的NaHCO3溶液中水的电离程度相等 |
更新时间:2021-03-04 08:51:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示水中c(H+)和c(OH-)的关系,下列判断正确的是
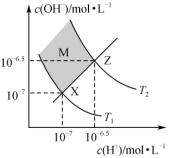

| A.M区域内任意点均有c(H+)>c(OH-) |
| B.两条曲线间任意点均有c(H+)·c(OH-)=1.0×10-14 |
| C.XZ线上任意点均呈中性 |
| D.图中T1>T2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
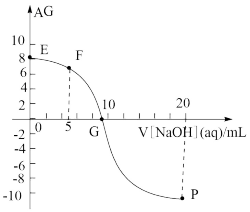
【推荐2】已知AG=lg ,电离度(α)=
,电离度(α)= ×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
 ,电离度(α)=
,电离度(α)= ×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
| A.F点溶液pH<7 |
| B.水的电离程度G>P>F>E |
C.点P前随着NaOH溶液的加入, 增大 增大 |
| D.常温下,HR的电离度约为1% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法错误的是
A.用 相同的氢氟酸溶液和盐酸中和等体积、等浓度的 相同的氢氟酸溶液和盐酸中和等体积、等浓度的 溶液,盐酸消耗的体积多 溶液,盐酸消耗的体积多 |
B.向   溶液中加入 溶液中加入   溶液,现白色沉淀后,继续滴入几滴 溶液,现白色沉淀后,继续滴入几滴 浓溶液,静置,出现红褐色沉淀,则说明同温下 浓溶液,静置,出现红褐色沉淀,则说明同温下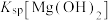 大于 大于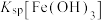 |
C.常温下, 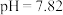 的 的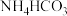 溶液中: 溶液中: |
D.常温下, 的氨水,稀释10倍后,其 的氨水,稀释10倍后,其 ,则 ,则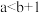 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是
| A.加入10mL 0.08mol·L-1的NaOH溶液 | B.加入100mL 的水进行稀释 |
| C.加水稀释成1L | D.加入10mL 0.01mol·L-1的盐酸溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.常温下,用湿润的pH试纸测得0.01mol/L的HCl水溶液的pH为2 |
| B.常温下,0.1mol/LCH3COONa溶液的pH>7,说明CH3COOH是弱酸 |
| C.常温下,pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低 |
| D.常温下,pH=3的酸与pH=11的碱等体积混合所得溶液一定显中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确 的是
| A.向CH3COOH溶液中加入少量CH3COONa固体,电离常数不变 |
B.pH相同的氨水和氢氧化钠加水稀释相同倍数后,c(NH )>c(Na+) )>c(Na+) |
| C.同温下,强酸溶液的pH不一定小于弱酸溶液的pH |
| D.足量的锌分别与等体积等浓度的稀硫酸和醋酸完全反应,在相同条件下产生的氢气体积相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃下,根据三种酸的电离常数,下列判断正确的是
| 酸 | HX | HY | HZ |
| 电离常数K | 1×10-7 | 9×10-6 | 1×10-2 |
| A.三种酸的强弱关系:HX>HY>HZ |
| B.相同温度下,0.1 mol/L的NaX、NaY、NaZ溶液,NaZ溶液碱性最强 |
| C.反应HX+Y-=HY+X-能够发生 |
| D.25℃时,0.1 mol/L HX溶液的pH约为4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】有关盐类水解的应用,下列说法错误的是
| A.热的纯碱溶液去油污效果好 |
B.金属焊接时,常用 溶液作除锈剂 溶液作除锈剂 |
C.加热 晶体可制得无水 晶体可制得无水 |
D.用 溶液和 溶液和 溶液可以制作泡沫灭火剂 溶液可以制作泡沫灭火剂 |
您最近一年使用:0次

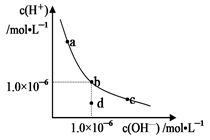
 均为
均为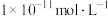 的4种溶液:①HCl溶液②
的4种溶液:①HCl溶液② 溶液③NaOH溶液④氨水。有关上述溶液的比较中正确的是
溶液③NaOH溶液④氨水。有关上述溶液的比较中正确的是 的量①最小
的量①最小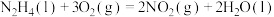

 的浓度相同
的浓度相同

