(1)将等体积等物质的量浓度的盐酸和氨水混合后,呈___________ 性,溶液中c( )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是___________ ;
(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈___________ 性,溶液中c( )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是___________ ;
(3)将物质的量浓度相同的盐酸与氨水混合后,溶液中c( )与c(Cl-)浓度相等,则混合溶液呈
)与c(Cl-)浓度相等,则混合溶液呈___________ 性,盐酸与氨水体积大小关系是___________ ;
(4)常温下,将m mol/L的盐酸和n mol/L氨水等体积混合后,溶液的pH=7,m与n的大小关系是___________ ,则盐酸中c(H+)与氨水中c(OH-)的大小关系是___________ 。
 )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈
 )与c(Cl-)的大小关系是
)与c(Cl-)的大小关系是(3)将物质的量浓度相同的盐酸与氨水混合后,溶液中c(
 )与c(Cl-)浓度相等,则混合溶液呈
)与c(Cl-)浓度相等,则混合溶液呈(4)常温下,将m mol/L的盐酸和n mol/L氨水等体积混合后,溶液的pH=7,m与n的大小关系是
更新时间:2021-03-06 21:16:52
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度为______ ;
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________ ,
②所得溶液中的物料守恒式为:________ +________ =__________ =_________ mol•L-1。
③c(CH3COOH)=_____________ mol•L-1(写出算式,不做近似计算)
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度为
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:
②所得溶液中的物料守恒式为:
③c(CH3COOH)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】 和
和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。
 的除去:
的除去:
方法1(双碱法):用NaOH吸收 ,并用CaO使NaOH再生NaOH溶液
,并用CaO使NaOH再生NaOH溶液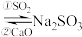 溶液
溶液
(1)写出过程①的离子方程式:_______________________________ ;CaO在水中存在如下转化: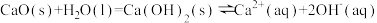 。从平衡移动的角度,简述过程②NaOH再生的原理
。从平衡移动的角度,简述过程②NaOH再生的原理______________________________________ 。
方法2:用氨水除去
(2)已知25℃, 的
的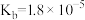 ,
, 的
的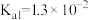 ,
,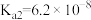 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
__________  。将
。将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的
__________ 。
 和
和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列各方法中的问题。 的除去:
的除去:方法1(双碱法):用NaOH吸收
 ,并用CaO使NaOH再生NaOH溶液
,并用CaO使NaOH再生NaOH溶液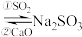 溶液
溶液(1)写出过程①的离子方程式:
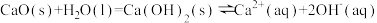 。从平衡移动的角度,简述过程②NaOH再生的原理
。从平衡移动的角度,简述过程②NaOH再生的原理方法2:用氨水除去

(2)已知25℃,
 的
的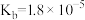 ,
, 的
的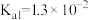 ,
,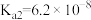 。若氨水的浓度为
。若氨水的浓度为 ,溶液中的
,溶液中的
 。将
。将 通入该氨水中,当
通入该氨水中,当 降至
降至 时,溶液中的
时,溶液中的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下将0.010mol CH3COONa和0.004mol HCl溶于水,配制成0.5L混合溶液,判断:
(1)溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是______ 和______ ;
(2)溶液中n(CH3COO-) + n(OH-) - n(H+) =______ mol。
(1)溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是
(2)溶液中n(CH3COO-) + n(OH-) - n(H+) =
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中HCO3―、CO32―、H2CO3 三种微粒的浓度由大到小 的顺序为:_______________________________ 。
(2)NaHCO3溶液与硫酸铝溶液混合的离子方程式 _______________________________ 。
(3)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液与某浓度盐酸溶液按体积比(碱与酸之比)1 :9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=____________ 。
(2)NaHCO3溶液与硫酸铝溶液混合的
(3)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液与某浓度盐酸溶液按体积比(碱与酸之比)1 :9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】常温下,用0.1 mol·L-1的盐酸和25.00 mL 0.1 mol·L-1氨水混合。
(1)当加入10.00 mL稀盐酸时,溶液中的溶质是_______________________ (填化学式),溶液的pH________ (填“>”、“<”或“=”)7。
(2)当某一时刻溶液中c(NH4+)=c(Cl-),此时溶液的pH________ (填“>”、“<”或“=”)7。所加的盐酸体积V是不是等于25.00 mL?______ (填“是”或“不是”)。其原因是_______
(3)某一时刻溶液中会不会存在:c(Cl-)>c(NH4+),且c(OH-)>c(H+)的关系?________ (填“会”或“不会”)。其原因是_____________________________
(4)当盐酸过量时,下列离子浓度的大小关系是:c(Cl-)________ c(NH4+),c(OH-)___ c(H+)。(填“>”、“<”或“=”)
(1)当加入10.00 mL稀盐酸时,溶液中的溶质是
(2)当某一时刻溶液中c(NH4+)=c(Cl-),此时溶液的pH
(3)某一时刻溶液中会不会存在:c(Cl-)>c(NH4+),且c(OH-)>c(H+)的关系?
(4)当盐酸过量时,下列离子浓度的大小关系是:c(Cl-)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA- HA-⇌H++A2-,完成以下问题:
(1)Na2A溶液显_______ (填“酸性”、“中性”或“碱性”),理由是_______ (用离子方程式表示)。
(2)已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度_______ 0.11mol·L-1(填“>”、“=”或“<”)。
(1)Na2A溶液显
(2)已知0.1 mol·L-1的NaHA溶液pH=2,则0.1 mol·L-1的H2A溶液中氢离子的物质的量浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:25℃时,CH3COOH和NH3·H2O的电离平衡常数近似相等。
(1)关于0.1 mol/LCH3COOH溶液,回答下列问题。
①25℃时,测得0.1 mol/LCH3COOH溶液的pH= 3,则由水电离出的H+的浓度为______ mol/L。
②CH3COONa溶液显____ (填“酸性”“碱性”或“中性”),用离子方程式表示其原因:_____ 。
③能证明醋酸是弱酸的实验事实是_____ (填字母)。
a.同浓度的CH3COOH溶液和盐酸分别与相同的Mg条反应。放出H2的初始速率醋酸慢
b.常温下0.1 mol/LCH3COONa溶液的pH >7
c.CH3COOH溶液与Na2CO3反应生成CO2
d.0.1 mol/LCH3COOH溶液可使紫色石蕊溶液变红
e.常温下0.1mol/L醋酸溶液的pH > 1
(2)关于0.1 mol/L氨水,回答下列问题。
①NH3·H2O的电离方程式为,NH3·H2O的电离平衡常数表达式Kb=_______ 。
②25℃时,0.1 mol/L氨水的pH=___________ 。
③25℃时,向10 mL0.1 mol/L氨水中加入同体积同浓度的盐酸。下列说法正确的是________ 。
a.c(Cl-)>c( )>c(OH-)>c(H+) b.c(Cl-) = c(
)>c(OH-)>c(H+) b.c(Cl-) = c( ) + c(NH3·H2O)
) + c(NH3·H2O)
(1)关于0.1 mol/LCH3COOH溶液,回答下列问题。
①25℃时,测得0.1 mol/LCH3COOH溶液的pH= 3,则由水电离出的H+的浓度为
②CH3COONa溶液显
③能证明醋酸是弱酸的实验事实是
a.同浓度的CH3COOH溶液和盐酸分别与相同的Mg条反应。放出H2的初始速率醋酸慢
b.常温下0.1 mol/LCH3COONa溶液的pH >7
c.CH3COOH溶液与Na2CO3反应生成CO2
d.0.1 mol/LCH3COOH溶液可使紫色石蕊溶液变红
e.常温下0.1mol/L醋酸溶液的pH > 1
(2)关于0.1 mol/L氨水,回答下列问题。
①NH3·H2O的电离方程式为,NH3·H2O的电离平衡常数表达式Kb=
②25℃时,0.1 mol/L氨水的pH=
③25℃时,向10 mL0.1 mol/L氨水中加入同体积同浓度的盐酸。下列说法正确的是
a.c(Cl-)>c(
 )>c(OH-)>c(H+) b.c(Cl-) = c(
)>c(OH-)>c(H+) b.c(Cl-) = c( ) + c(NH3·H2O)
) + c(NH3·H2O)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸,请回答相关问题:
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c_ >c_____ >c_____ >c_____
②当盐酸与氨水等物质的量反应时,溶液的pH_____ 7(填“>”或“<”或“=”,下同).
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为: n(NH3·H2O)___ n(HCl),溶液中c( NH4+)_______ c(Cl﹣).
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c
②当盐酸与氨水等物质的量反应时,溶液的pH
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为: n(NH3·H2O)
您最近一年使用:0次

 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
 的
的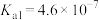 ,
,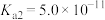 )。
)。


