(1)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中HCO3―、CO32―、H2CO3 三种微粒的浓度由大到小 的顺序为:_______________________________ 。
(2)NaHCO3溶液与硫酸铝溶液混合的离子方程式 _______________________________ 。
(3)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液与某浓度盐酸溶液按体积比(碱与酸之比)1 :9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=____________ 。
(2)NaHCO3溶液与硫酸铝溶液混合的
(3)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液与某浓度盐酸溶液按体积比(碱与酸之比)1 :9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=
更新时间:2018-11-17 22:56:30
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是不同温度下水的离子积的数据。试回答以下问题:
(1)若 ,则a
,则a_______  (填“>”、“<”或“=”),做此判断的理由是
(填“>”、“<”或“=”),做此判断的理由是_______ 。
(2) 时,某
时,某 溶液中
溶液中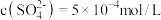 ,取该溶液
,取该溶液 加水稀释至
加水稀释至 ,则稀释后溶液中
,则稀释后溶液中
_______ 。
(3)在 温度下,测得某溶液
温度下,测得某溶液 ,①则该溶液显
,①则该溶液显_______ (填“酸”、“碱”或“中)性;
同样在 温度下
温度下 的
的 溶液
溶液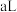 与
与 的
的 溶液
溶液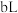 混合:
混合:
②若所得混合液为中性,则
_______ ;
③若所得混合液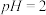 ,则
,则
_______ 。
(4)加热蒸干 溶液并灼烧所得固体,最终得到的产物是
溶液并灼烧所得固体,最终得到的产物是_______ 。
(5)常温下,已知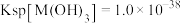 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液
_______ 。
(6)已知:a.常温下,醋酸和 的电离平衡常数均为
的电离平衡常数均为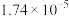 ;
;
b.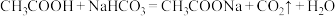 。
。
则 溶液呈
溶液呈_______ 性(填“酸”“碱”或“中”,下同), 溶液呈
溶液呈_______ 性, 溶液中物质的量浓度最大的离子是
溶液中物质的量浓度最大的离子是_______ (填化学式)。
温度/ | 25 |  |  |
| 水的离子积 |  | a |  |
 ,则a
,则a (填“>”、“<”或“=”),做此判断的理由是
(填“>”、“<”或“=”),做此判断的理由是(2)
 时,某
时,某 溶液中
溶液中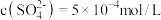 ,取该溶液
,取该溶液 加水稀释至
加水稀释至 ,则稀释后溶液中
,则稀释后溶液中
(3)在
 温度下,测得某溶液
温度下,测得某溶液 ,①则该溶液显
,①则该溶液显同样在
 温度下
温度下 的
的 溶液
溶液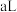 与
与 的
的 溶液
溶液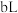 混合:
混合:②若所得混合液为中性,则

③若所得混合液
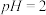 ,则
,则
(4)加热蒸干
 溶液并灼烧所得固体,最终得到的产物是
溶液并灼烧所得固体,最终得到的产物是(5)常温下,已知
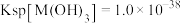 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液
(6)已知:a.常温下,醋酸和
 的电离平衡常数均为
的电离平衡常数均为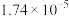 ;
;b.
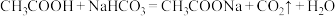 。
。则
 溶液呈
溶液呈 溶液呈
溶液呈 溶液中物质的量浓度最大的离子是
溶液中物质的量浓度最大的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液等体积混合,求混合溶液的pH___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】依据所学知识,回答下列问题:
(1)结合离子方程式说明配制氯化铁溶液时,将氯化铁固体溶于浓盐酸,再加水稀释的原因:___________ 。
(2)已知下列几种物质在常温下的电离常数Ka:
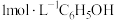 溶液的
溶液的
___________ ,向 溶液中加入足量
溶液中加入足量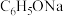 发生反应,该反应常温下的平衡常数
发生反应,该反应常温下的平衡常数
___________ 。
(3)室温时,将 溶液滴入
溶液滴入 未知浓度的某一元酸
未知浓度的某一元酸 溶液中,溶液
溶液中,溶液 随加入
随加入 溶液体积的变化曲线如图所示。当
溶液体积的变化曲线如图所示。当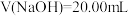 时,溶液恰好完全反应。该滴定过程选择
时,溶液恰好完全反应。该滴定过程选择___________ 指示剂,一元酸 属于
属于___________ (填“强酸”或“弱酸”), 的电离常数
的电离常数
___________ 。
(1)结合离子方程式说明配制氯化铁溶液时,将氯化铁固体溶于浓盐酸,再加水稀释的原因:
(2)已知下列几种物质在常温下的电离常数Ka:
| 物质 | C6H5OH(一元酸) | H2S |
| Ka | Ka=1.0×10-10 | Ka1=1.1×10-7 Ka2=1.3×10-13 |
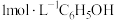 溶液的
溶液的
 溶液中加入足量
溶液中加入足量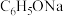 发生反应,该反应常温下的平衡常数
发生反应,该反应常温下的平衡常数
(3)室温时,将
 溶液滴入
溶液滴入 未知浓度的某一元酸
未知浓度的某一元酸 溶液中,溶液
溶液中,溶液 随加入
随加入 溶液体积的变化曲线如图所示。当
溶液体积的变化曲线如图所示。当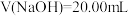 时,溶液恰好完全反应。该滴定过程选择
时,溶液恰好完全反应。该滴定过程选择 属于
属于 的电离常数
的电离常数

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题:
(1)HClO的电离方程式为__________________________ 。
(2)用离子方程式解释铁盐可用于净水的原理__________________________ 。
(3)在NaOH 溶液中逐渐加入稀醋酸至溶液呈中性,则所得溶液中c(Na+)_______ c(CH3COO-)(填“>”“<”或“=”下同)。
(4)相同pH的NH4Cl溶液与NH4HSO4溶液中NH4+浓度的大小关系:前者_______ 后者。
(5)用惰性电极电解500mL某浓度的CuSO4溶液一段时间后,CuSO4刚好反应完,需要加入16gCuO才能复原,则原CuSO4溶液的物质量浓度为___________ 。
(1)HClO的电离方程式为
(2)用离子方程式解释铁盐可用于净水的原理
(3)在NaOH 溶液中逐渐加入稀醋酸至溶液呈中性,则所得溶液中c(Na+)
(4)相同pH的NH4Cl溶液与NH4HSO4溶液中NH4+浓度的大小关系:前者
(5)用惰性电极电解500mL某浓度的CuSO4溶液一段时间后,CuSO4刚好反应完,需要加入16gCuO才能复原,则原CuSO4溶液的物质量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下列盐溶液中能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样并说明溶液的酸碱性:
(1)CH3COOK_________________________________________ ,溶液呈______ 性;
(2)K2SO4_____________________________________________ ,溶液呈______ 性;
(3)CuCl2_____________________________________________ ,溶液呈______ 性。
(1)CH3COOK
(2)K2SO4
(3)CuCl2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】甲、乙、丙、丁代表不同的一元酸,常温下,将它们分别和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合后溶液的pH如表所示:
完成下列填空:
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?____ 。
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为____ 。
(3)从实验3的结果分析,该混合溶液中离子浓度由大到小的顺序是____ 。
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=____ mol·L-1。
室温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1CH3COOH溶液,pH的变化如图所示。
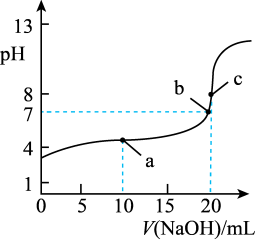
(5)用化学符号表示滴定过程中溶液里微粒之间的浓度关系
点a处:c(CH3COO-)+c(CH3COOH)=____ ;
点b处:溶液中各离子浓度大小关系:____ ;
点c处:c(CH3COOH)+c(H+)=____ 。
| 实验序号 | 所用酸 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合后溶液的pH |
| 实验1 | 甲 | 0.1000 | 0.1000 | pH=a |
| 实验2 | 乙 | 0.1200 | 0.1000 | pH=7 |
| 实验3 | 丙 | 0.2000 | 0.1000 | pH>7 |
| 实验4 | 丁 | 0.1000 | 0.1000 | pH=10 |
完成下列填空:
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为
(3)从实验3的结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=
室温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1CH3COOH溶液,pH的变化如图所示。

(5)用化学符号表示滴定过程中溶液里微粒之间的浓度关系
点a处:c(CH3COO-)+c(CH3COOH)=
点b处:溶液中各离子浓度大小关系:
点c处:c(CH3COOH)+c(H+)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电解质的溶液中存在着众多的化学平衡。
(1)25℃时向浓度均为0.1mol/L的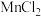 和
和 混合溶液中逐滴加入氨水,首先生成的沉淀为
混合溶液中逐滴加入氨水,首先生成的沉淀为_______ 。已知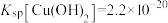 ,
, 。
。
(2)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中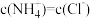 ,则溶液显
,则溶液显_______ 性(填“酸”或“碱”或“中”)。
(3)25℃时向含有 的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将
的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将_______ (填“正向”、“不”或“逆向”)移动。
(4)甲酸钠 属于
属于_______ (填“强”或“弱”)电解质, 溶液呈碱性的原因是
溶液呈碱性的原因是_______ (用离子方程式表示)。
(1)25℃时向浓度均为0.1mol/L的
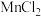 和
和 混合溶液中逐滴加入氨水,首先生成的沉淀为
混合溶液中逐滴加入氨水,首先生成的沉淀为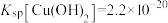 ,
, 。
。(2)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中
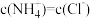 ,则溶液显
,则溶液显(3)25℃时向含有
 的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将
的溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将(4)甲酸钠
 属于
属于 溶液呈碱性的原因是
溶液呈碱性的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
Ⅰ.已知H2A在水中存在以下平衡:H2A = H++HA-,HA-⇌H++A2-。
(1)常温下NaHA溶液的pH________ (填序号),原因是_________________ 。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是________ 。
A.c(H+)·c(OH-)=1.0×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05 mol·L-1
(3)室温下若0.1mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1 H2A溶液中c(H+)______ (填“>"、“<”或“=“)0.11 mol·L-1,理由为______________ 。
Ⅰ.已知H2A在水中存在以下平衡:H2A = H++HA-,HA-⇌H++A2-。
(1)常温下NaHA溶液的pH
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向0.1 mol·L-1的NaHA溶液中逐滴滴加0.1 mol·L-1KOH溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是
A.c(H+)·c(OH-)=1.0×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05 mol·L-1
(3)室温下若0.1mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1 H2A溶液中c(H+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】常温下,将0.01molNH4Cl和0.002molNaOH溶于水,形成1L混合溶液:
(1)该溶液中存在三个平衡体系,用电离方程式或离子方程式表示:
①____________
②____________
③____________ 。
(2)溶液中含有的微粒是__________________ 。
(3)在上述溶液中,电荷守恒是:____________ 。
(1)该溶液中存在三个平衡体系,用电离方程式或离子方程式表示:
①
②
③
(2)溶液中含有的微粒是
(3)在上述溶液中,电荷守恒是:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时溶液的酸碱性变化不大。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是____________________ ;向其中加入少量KOH溶液时,发生反应的离子方程式是____________________ 。
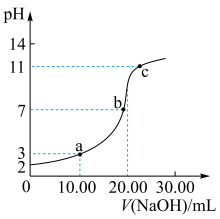
(2)现将 HA溶液和
HA溶液和 NaOH溶液等体积混合,得到缓冲溶液。
NaOH溶液等体积混合,得到缓冲溶液。
①若HA为 ,该溶液显酸性,则溶液中
,该溶液显酸性,则溶液中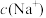
________ 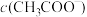 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
②若HA为 ,该溶液显碱性,溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显碱性,溶液中所有的离子按浓度由大到小排列的顺序是_______________ 。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是
(2)现将
 HA溶液和
HA溶液和 NaOH溶液等体积混合,得到缓冲溶液。
NaOH溶液等体积混合,得到缓冲溶液。①若HA为
 ,该溶液显酸性,则溶液中
,该溶液显酸性,则溶液中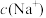
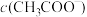 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②若HA为
 ,该溶液显碱性,溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显碱性,溶液中所有的离子按浓度由大到小排列的顺序是
您最近一年使用:0次



