常温下,0.1 mol·L-1某一元酸(HA)溶液中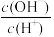 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
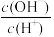 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是| A.溶液中水电离出的c(H+)=10-10 mol·L-1 |
| B.溶液中c(H+)+c(A-)=0.1 mol·L-1 |
| C.与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中离子浓度大小关系为:c(A-)>c(Na+)>c(OH-)>c(H+) |
| D.上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液c(OH-)均增大 |
12-13高二上·陕西·期末 查看更多[5]
广东省揭阳市惠来县第一中学2021-2022学年高二上学期第二次阶段考试化学试题吉林省辽源市田家炳高级中学2019-2020学年高二12月月考化学试题(已下线)2011-2012学年陕西省陕师大附中高二上学期期末试题化学(理)试卷2014-2015山东省潍坊一中高二上学期1月质量检测化学试卷(已下线)2012届甘肃省天水市二中高三模拟(5月)考试化学试卷
更新时间:2016-12-09 03:30:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,Kw不变 |
| B.25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃,向20mL0.1mol·L-1的H3PO2溶液中滴加0.1mol·L-1的NaOH溶液直至过量,滴定曲线如图1,所有含磷微粒的分布系数δ随pH变化关系如图2,[如 的分布系数:
的分布系数: ]
]

则下列说法错误的是
 的分布系数:
的分布系数: ]
]
则下列说法错误的是
| A.H3PO2为一元弱酸,电离常数Ka约为1×10-5 |
| B.水的电离程度按a、b、c、d、e顺序依次增大 |
C.当混合溶液pH=7时,c( )>c(H3PO2) )>c(H3PO2) |
D.b点溶液中存在关系2c(H+)+c(H3PO2)=2c(OH-)+c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】室温下,向20mL浓度均为0.2mol⋅L﹣1的NaOH和NH3⋅H2O的混合溶液中滴加0.2mol⋅L﹣1的标准硫酸溶液,滴加过程中溶液导电能力与所加硫酸溶液体积关系如图所示(已知c点处pH=5)。下列说法正确的是


A.ab段反应的离子方程式为NH3⋅H2O+H+= +H2O +H2O |
| B.室温下NH3⋅H2O的电离平衡常数Kb≈10﹣5 |
| C.a、b、c三点中,b点处水的电离程度最大 |
D.c点溶液中c(Na+)>c(H+)>c( )>c(OH﹣) )>c(OH﹣) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】由下列实验及现象能推出相应结论的是
| 实验操作及实验现象 | 结 论 | |
| A | 向2mL 0.5mol/L FeCl3溶液中滴加2mL 1mol/L KSCN溶液,振荡后静置,观察到溶液变成红色,加入1mL 2mol/L KCl溶液后溶液红色变浅 | c(KCl)增大使该反应[FeCl3+ 3KSCN  Fe(SCN)3+3KCl]的化学平衡逆向移动 Fe(SCN)3+3KCl]的化学平衡逆向移动 |
| B | 向做了相同标记的2支试管中均加入2mL 0.1mol/L Na2S2O3溶液,再分别向2支试管中加入4mL浓度为0.1mol/L、0.5mol/L 的H2SO4溶液,测定恰好遮挡全部标记所用时间 | 其他条件一定时,反应物浓度越大,化学反应速率越快 |
| C | 室温下,用广泛pH试纸测定0.1 mol/L Na2SO3溶液的pH为10,0.1mol/L NaHSO3溶液的pH为5 | 相同条件下,HSO3-的水解能力强于SO32- |
| D | 向2 mL0.1mol/LAgNO3溶液中加入1mL0.1mol/LNaCl溶液,生成白色沉淀,再加入1mL0.1mol/L KI溶液,生成黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关离子浓度大小比较正确的是
| A.物质的量浓度均为0.1mol·L-1的三种物质的溶液:①NaAlO2,②CH3COONa,③NaHCO3,pH由大到小的顺序是①>③>② |
B.等pH的①(NH4)2SO4,②NH4HSO4,③NH4Cl,c(NH )由大到小的顺序是①>③>② )由大到小的顺序是①>③>② |
C.等浓度的①NH4Al(SO4)2,②(NH4)2CO3,③(NH4)2Fe(SO4)2,c(NH )由大到小的顺序是②>③>① )由大到小的顺序是②>③>① |
| D.相同温度下,将足量AgCl固体分别放入相同体积的①0.1mol·L-1盐酸,②0.1mol·L-1MgCl2溶液,③0.1mol·L-1AgNO3溶液中,c(Ag+)由大到小的顺序是③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,用 的
的 溶液滴定
溶液滴定 和
和 的混合酸,测得溶液的导电能力随
的混合酸,测得溶液的导电能力随 滴入体积V的关系如图所示。已知
滴入体积V的关系如图所示。已知 为强酸,
为强酸, 为弱酸,N点和P点可分别看作
为弱酸,N点和P点可分别看作 和
和 恰好与
恰好与 完全反应的点,忽略溶液混合时引起的体积变化。下列叙述中正确的是
完全反应的点,忽略溶液混合时引起的体积变化。下列叙述中正确的是

 的
的 溶液滴定
溶液滴定 和
和 的混合酸,测得溶液的导电能力随
的混合酸,测得溶液的导电能力随 滴入体积V的关系如图所示。已知
滴入体积V的关系如图所示。已知 为强酸,
为强酸, 为弱酸,N点和P点可分别看作
为弱酸,N点和P点可分别看作 和
和 恰好与
恰好与 完全反应的点,忽略溶液混合时引起的体积变化。下列叙述中正确的是
完全反应的点,忽略溶液混合时引起的体积变化。下列叙述中正确的是
A.M点溶液中 和 和 的浓度均为 的浓度均为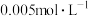 |
B.P点溶液中存在: |
C.Q点溶液中存在: |
D.水的电离程度: |
您最近一年使用:0次
单选题
|
适中
(0.65)
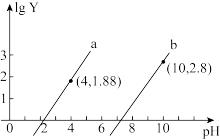
【推荐2】25℃时,向 的二元酸H2A溶液中逐滴滴入等浓度的NaOH溶液,测得溶液的pH与lg Y[Y代表
的二元酸H2A溶液中逐滴滴入等浓度的NaOH溶液,测得溶液的pH与lg Y[Y代表 或
或 ]关系如图。下列相关结论正确的是
]关系如图。下列相关结论正确的是
 的二元酸H2A溶液中逐滴滴入等浓度的NaOH溶液,测得溶液的pH与lg Y[Y代表
的二元酸H2A溶液中逐滴滴入等浓度的NaOH溶液,测得溶液的pH与lg Y[Y代表 或
或 ]关系如图。下列相关结论正确的是
]关系如图。下列相关结论正确的是 
A.曲线a表示pH与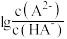 的变化关系 的变化关系 |
B.25℃时,H2A的 约为10-7.2 约为10-7.2 |
C.当溶液的pH=6时, |
D.滴入20.00mL NaOH溶液时,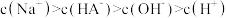 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,体积均为20mL、浓度均为0.1mol/L的HX溶液、HY 溶液中分别滴加同浓度的 NaOH 溶液,反应后溶液中水电离的c(H+)水的负对数[-lgc(H+)水]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是


| A.HX、HY 均为弱酸 |
| B.a、b、c三点溶液均显中性 |
| C.b、d 两点溶液的离子总浓度不同 |
| D.c 点溶液中c(X-)+c(HX)=0.1mol /L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
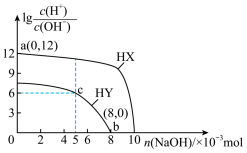
【推荐2】25℃时,向浓度均为0.1mol·L-1、体积均为100mL的两种一元酸HX、HY溶液中分别加入NaOH固体,溶液中 随n(NaOH)的变化如图所示。下列说法正确的是
随n(NaOH)的变化如图所示。下列说法正确的是
 随n(NaOH)的变化如图所示。下列说法正确的是
随n(NaOH)的变化如图所示。下列说法正确的是
| A.HX为弱酸,HY为强酸 |
| B.水的电离程度:b>c>d |
| C.C点对应的溶液中:c(HY)>c(Y-) |
| D.若将c点与d点的溶液全部混合,溶液中离子浓度大小:c(Na+)>c(X-)>c(Y-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,往0.01 mol·L 的NaHA溶液中通入HCl(g)或加入NaOH固体调节溶液的pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图所示。下列说法正确的是
的NaHA溶液中通入HCl(g)或加入NaOH固体调节溶液的pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图所示。下列说法正确的是

 的NaHA溶液中通入HCl(g)或加入NaOH固体调节溶液的pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图所示。下列说法正确的是
的NaHA溶液中通入HCl(g)或加入NaOH固体调节溶液的pH(忽略体积变化),溶液中c(HA-)随pH变化的曲线如图所示。下列说法正确的是
| A.水的电离程度:c>b=d>a |
B.c点溶液中存在: |
C.d点溶液中存在: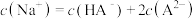 |
D.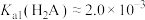 |
您最近一年使用:0次

 浓度与
浓度与 浓度比为
浓度比为 的溶液,可在
的溶液,可在 溶液中加入
溶液中加入


