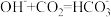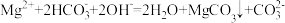根据下列实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 在0.1 mol·L-1Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深 |  水解是吸热反应 水解是吸热反应 |
| B | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性HA比HB强 |
| C | 常温下,用饱和NaI溶液可将AgCl沉淀转化为AgI | Ksp(AgI)>Ksp(AgCl) |
| D | 室温下,用pH试纸测得:0.1 mol·L-1NaHSO3溶液的pH约为5 |  水解能力比电离能力弱 水解能力比电离能力弱 |
| A.A | B.B | C.C | D.D |
更新时间:2021-03-14 21:57:14
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】常温下,分别取未知浓度的AOH和BOH两种碱的稀溶液,加水稀释至原体积的n倍。两溶液稀释倍数的对数值(lgn)与溶液的pH变化关系如图所示。下列叙述正确的是


| A.水的电离程度:Z>X=Y |
| B.常温下,Kb(BOH)<Kb(AOH) |
| C.中和等体积X、Y两点溶液,后者消耗HCl的物质的量多 |
| D.物质的量浓度相同的AC1溶液和BC1溶液,前者阳离子浓度之和小于后者 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】现有a mol/L NaX和bmol/L NaY两种盐溶液。下列说法正确的是
| A.若a=b且c(X-)=c(Y-)+c(HY),则酸性HX>HY |
| B.若a>b且c(X-)=c(Y-),则酸性HX<HY |
| C.若a=b且pH(NaX)>pH(NaY),则酸性HX>HY |
| D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)=0.1mol/L,则a=b=0.1mol/L, |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】常温下,若HA溶液和NaOH溶液混合后pH=7,下列说法不合理 的是
| A.反应后HA溶液可能有剩余 |
| B.生成物NaA的水溶液的pH可能小于7 |
| C.HA溶液和NaOH溶液的体积相等 |
| D.HA溶液的c(H+)和NaOH溶液的c(OH-)可能不相等 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】以下实验操作和现象,所得结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 取5mL0.1mol/LKI溶液于试管中,加入1mL0.1mol/LFeCl3溶液,充分反应后滴入2滴15%KSCN溶液,溶液变血红色 | KI与FeCl3的反应有一定限度 |
| B | 取2mL0.1mol/LAgNO3溶液,先进行加热,后置于冷水中,发现溶液的颜色先由蓝色转变为黄色然后又由黄色转变为蓝色 | CuCl2溶液中存在以下平衡:[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O △H>0 [CuCl4]2-+4H2O △H>0 |
| C | 取2mL0.1mol/LAgNO3溶液于试管中,滴加1mL0.1mol/LNaCl溶液,待不再出现白色沉淀后,再滴加1mL0.1mol/LKI溶液白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 分别测浓度均为0.1mol/L的CH3COONH4和NaHCO3溶液的pH,后者大于前者 | 水解常数:Kh(CH3COO-)<Kh(HCO ) ) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】常温下向浓度均为0.10 mol·L-1、体积均为1 mL的NaOH溶液和Na2CO3溶液中分别加水,均稀释至V mL,两种溶液的pH与lg V的变化关系如图所示。下列叙述中错误的是
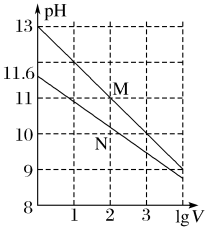
A.Kh1(CO )(Kh1为第一级水解平衡常数)的数量级为10-4 )(Kh1为第一级水解平衡常数)的数量级为10-4 |
| B.曲线M表示Na2CO3溶液的pH随lg V的变化关系 |
C.Na2CO3溶液中存在:c(Na+)>c(CO )>c(OH-)>c(HCO )>c(OH-)>c(HCO )>c(H+) )>c(H+) |
D.若将Na2CO3溶液加热蒸干,由于CO 水解,最终析出的是NaOH固体 水解,最终析出的是NaOH固体 |
您最近一年使用:0次
【推荐1】下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 常温下﹐用pH计测得CH3COONa溶液的pH>7 | 说明CH3COOH是弱酸 |
| B | 将装有二氧化氮的玻璃球置于热水中,球内气体颜色加深 | 说明2NO2(g) N2O4(g),正反应放热 N2O4(g),正反应放热 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 | 说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
| D | 乙醇与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 | 检验制得气体是否为乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】化学与生活、生产密切相关,下列说法错误的是
| A.可乐打开时产生气泡,是因为压强减小促使CO2逸出 |
| B.去除锅炉水垢中的CaSO4,用饱和Na2CO3溶液浸泡预处理 |
| C.误食可溶性钡盐造成中毒,可以服用Na2CO3溶液来解毒 |
| D.工业合成氨,常采用铁触媒、减小氨气的浓度来提高反应速率 |
您最近一年使用:0次

 的浓度与
的浓度与 的浓度比为
的浓度比为 的溶液,可在
的溶液,可在 溶液中加入下列试剂
溶液中加入下列试剂
 溶液中通入过量
溶液中通入过量 :
: