下列说法正确的是
A.常温下,由水电离产生的c(OH-)=10-11mol•L-1的溶液中,Cu2+、CO 、Cl-、Na+一定能大量共存 、Cl-、Na+一定能大量共存 |
| B.等物质的量浓度的稀盐酸与稀硫酸的pH相等 |
| C.对于反应N2H4(l)=N2(g)+2H2(g)∆H=-50.6kJ•mol-1,它只在高温下自发进行 |
| D.25℃时在醋酸钠溶液和盐酸混合后呈中性的溶液中:c(Na+)>c(Cl-) |
更新时间:2021-03-31 16:10:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
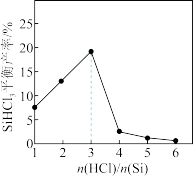
【推荐1】有关反应Si(s)+3HCl(g) SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
 SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
| A.该反应在低温条件下不能自发 |
| B.其他条件不变,增大压强SiHCl3平衡产率减小 |
| C.实际工业生产选择高温,原因是高温时Si的平衡转化率比低温时大 |
D.如图所示,当 >3,SiHCl3平衡产率减小可能发生了副反应 >3,SiHCl3平衡产率减小可能发生了副反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列变化过程中,ΔS <0的是
| A.氯化钠溶于水中 | B.NH3(g)和HCl(g)反应生成NH4Cl |
| C.干冰的升华 | D.CaCO3(s)分解为CaO(s)和CO2(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在常温下,有关下列4种溶液的叙述中错误的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
A.将溶液①、④等体积混合,所得溶液中:c(Cl-)>c(NH )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| B.在溶液①、②中分别加入适量的氯化铵晶体后,两种溶液的pH均减小 |
| C.分别取1mL稀释至10mL,四种溶液的pH:①>②>④>③ |
| D.将aL溶液④与bL溶液②混合后,若所得溶液的pH=4,则a:b=11:9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向1LpH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示。下列叙述错误的是


| A.a点溶液中,水电离出的c(H+)=1×10-10mol•L-1 |
| B.b点溶液中,水电离出的c(H+)=1×10-7mol•L-1 |
C.c点溶液中,c(Na+)>c(HCO )>c(CO )>c(CO ) ) |
D.d点溶液中,c(Na+)=2c(CO )+c(HCO )+c(HCO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
A.常温下,0.5mol/LHB溶液和0.5mol/LNaOH溶液等体积混合后溶液的 ,则混合溶液中离子浓度的大小顺序为: ,则混合溶液中离子浓度的大小顺序为: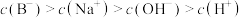 |
B.常温下,0.2mol/L的下列溶液① ,② ,② ,③ ,③ ,④ ,④ 中, 中, 由大到小的顺序是:②>①>④>③ 由大到小的顺序是:②>①>④>③ |
C.常温下0.1mol/LpH为3的NaHA溶液中: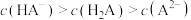 |
D.常温下,pH均为4的HF溶液和 溶液、pH均为10的氨水和 溶液、pH均为10的氨水和 溶液,四种溶液中由水电离的 溶液,四种溶液中由水电离的 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.100g质量分数为46%的乙醇(C2H5OH)水溶液中含有的氧原子数为4NA |
| B.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
| C.电解精炼铜过程中,当电路中通过0.5NA电子时,阳极有16g Cu转化为Cu2+ |
D.0.1mol KI与0.1mol FeCl3在溶液中反应转移的电子数为0.1NA(2Fe3++2I- 2Fe2++I2) 2Fe2++I2) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.3.4g H2O2中含有的共用电子对数为0.1NA |
| B.25 ℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA |
| C.标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0. 1 NA |
| D.标况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】H2S为二元弱酸。20℃时,向0.100mol·L-1的Na2S溶液中缓慢通入HCl气体(忽略溶液体积的变化及H2S的挥发)。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
| A.c(Cl-)=0.100mol·L-1的溶液中:c(OH-)-c(H+)=c(H2S)-2c(S2-) |
| B.通入HCl气体之前:c(S2-)>c(HS-)>c(OH-)>c(H+) |
| C.c(HS-)=c(S2-)的碱性溶液中:c(Cl-)+c(HS-)>0.100mol·L-1+c(H2S) |
| D.pH=7的溶液中:c(Cl-)=c(HS-)+2c(H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,SO2与NaOH溶液反应后的溶液中存在含硫微粒:H2SO3、HSO 和SO
和SO ,它们的物质的量分数
,它们的物质的量分数 与溶液pH的关系如图所示。根据信息判断下列不正确的是
与溶液pH的关系如图所示。根据信息判断下列不正确的是

 和SO
和SO ,它们的物质的量分数
,它们的物质的量分数 与溶液pH的关系如图所示。根据信息判断下列不正确的是
与溶液pH的关系如图所示。根据信息判断下列不正确的是
| A.pH控制在4-5时可活得较纯的NaHSO3 |
B.由图中数据,可估算出H2SO3的第二级电离平衡常数K2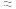 10-7 10-7 |
C.pH=7时,溶液中存在:c(Na+)<c(HSO )+c(SO )+c(SO ) ) |
D.pH=9时,溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】室温下用0.1mol•L-1NaOH溶液吸收SO2,若通入SO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c总=c(H2SO3)+c(HSO )+c(SO
)+c(SO )。H2SO3电离常数分别为Ka1=1.54×10-2、Ka2=1.00×10-7。下列说法正确的是
)。H2SO3电离常数分别为Ka1=1.54×10-2、Ka2=1.00×10-7。下列说法正确的是
 )+c(SO
)+c(SO )。H2SO3电离常数分别为Ka1=1.54×10-2、Ka2=1.00×10-7。下列说法正确的是
)。H2SO3电离常数分别为Ka1=1.54×10-2、Ka2=1.00×10-7。下列说法正确的是A.NaOH溶液吸收SO2所得到的溶液中:c(SO )>c(HSO )>c(HSO )>c(H2SO3) )>c(H2SO3) |
B.NaOH完全转化为NaHSO3时,溶液中:c(H+)+c(SO )=c(OH—)+c(H2SO3) )=c(OH—)+c(H2SO3) |
C.NaOH完全转化为Na2SO3时,溶液中:c(Na+)>c(SO )>c(OH—)>c(HSO )>c(OH—)>c(HSO ) ) |
D.NaOH溶液吸收SO2,c总=0.1mol•L-1溶液中:c(H2SO3)>c(SO ) ) |
您最近一年使用:0次



