现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为_________ 热反应,且m+n ________ p(填“>”、“=”或“<”)。
(2)减压时,A的质量分数________ (填“增大”、“减小”或“不变”,下同)。
(3)若容积不变加入B,则A的转化率__________ ,B的转化率________ 。
(4)若升高温度,则平衡常数k将________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________ 。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色________ ;而维持容器内压强不变,充入氖气时,混合物颜色___________ (填“变深”、“变浅”或“不变”)。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压时,A的质量分数
(3)若容积不变加入B,则A的转化率
(4)若升高温度,则平衡常数k将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色
11-12高二下·福建福州·期末 查看更多[1]
(已下线)2011-2012学年福建省福州八中高二下学期期末考试化学试卷
更新时间:2012-09-12 19:41:37
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】燃煤烟气脱硫有很多方法
方法I:先用氨水将SO2转化为NH4HSO3,再通入空气氧化成(NH4)2SO4。
方法II:用Na2SO3溶液吸收SO2,再经电解转化为H2SO4。
据此回答以下问题:
(1)方法I中发生氧化还原反应的离子方程式__________ 。能提高方法I燃煤烟气SO2中去除率的措施有__________ (填字母)。
A.增大氨水浓度 B.增大燃煤烟气的流速
C.事先去除燃煤烟气中的二氧化碳 D.增大压强
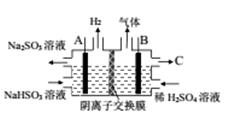
(2)采用方法II脱硫,燃煤烟气中的二氧化碳能否与生成的NaHSO3溶液反应_______ (说明理由)。已知H2SO3为的电离平衡常数为K1=1.54×10-2,K2=1.02×10-7。则NaHSO3溶液中含S元素粒子浓度由大到小的顺序为_______ 。通过右图所示电解装置可将生成的NaHSO3转化为硫酸,电极材料皆为石墨。则A为电解池的______ (填“阴极”或“阳极”)。C为______ (填物质名称)。若将阴离子交换膜换成阳子交换膜,写出阳极区域发生的电极反应______ 。
方法I:先用氨水将SO2转化为NH4HSO3,再通入空气氧化成(NH4)2SO4。
方法II:用Na2SO3溶液吸收SO2,再经电解转化为H2SO4。
据此回答以下问题:
(1)方法I中发生氧化还原反应的离子方程式
A.增大氨水浓度 B.增大燃煤烟气的流速
C.事先去除燃煤烟气中的二氧化碳 D.增大压强
(2)采用方法II脱硫,燃煤烟气中的二氧化碳能否与生成的NaHSO3溶液反应
您最近一年使用:0次
【推荐2】I.一定条件下,在容积为 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
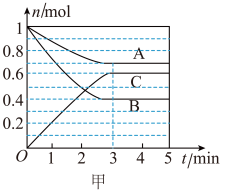
(1)该反应的化学方程式为___________ 。
(2)向一恒温恒容的密闭容器中充入 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
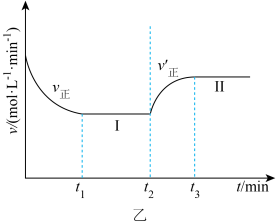
①根据图乙判断,在 时刻改变的外界条件是
时刻改变的外界条件是___________ 。
②平衡时A的体积分数
___________ 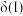 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
Ⅱ.在密闭容器中充入一定量的 ,发生反应:
,发生反应: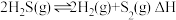 ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
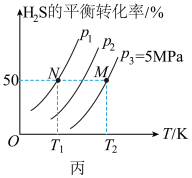
和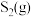 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)
___________ (填“>”“<”或“=”)0。
(4)图丙中压强( 、
、 、
、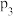 )由大到小的顺序为
)由大到小的顺序为___________ 。
(5)图丙中M点对应的平衡常数
___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
(1)该反应的化学方程式为
(2)向一恒温恒容的密闭容器中充入
 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
①根据图乙判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②平衡时A的体积分数

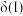 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。Ⅱ.在密闭容器中充入一定量的
 ,发生反应:
,发生反应: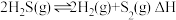 ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和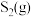 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)

(4)图丙中压强(
 、
、 、
、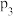 )由大到小的顺序为
)由大到小的顺序为(5)图丙中M点对应的平衡常数

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】对SO2、NOx、CO2和CO进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入NO2、SO2发生反应:NO2(g)+SO2(g)⇌SO3(g)+NO(g)。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是___________ (填序号)。
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是___________ (填字母)。
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为 密闭容器中充入
密闭容器中充入 和
和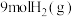 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
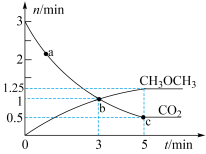
①反应到达3min时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②0~5min内,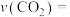
___________  。
。
③反应达到平衡状态时, 的体积分数为
的体积分数为___________ %(保留1位小数)。
④a、b、c三点中代表达到平衡的是___________ ,a点的正反应速率___________ (填>、<或=)b点的逆反应速率。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的物质的量
②下列能说明反应达到平衡状态的是
a.混合气体的密度保持不变
b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变
d.每生成1molSO3的同时消耗1molNO
(2)在体积为
 密闭容器中充入
密闭容器中充入 和
和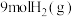 ,发生反应
,发生反应 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
①反应到达3min时,

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②0~5min内,
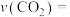
 。
。③反应达到平衡状态时,
 的体积分数为
的体积分数为④a、b、c三点中代表达到平衡的是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】砷(33As)在周期表中与氮同主族,砷及其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷化氢的电子式为_________ 。
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒。As2O3是一种两性氧化物,写出As2O3溶于浓盐酸的化学方程式_____________________ 。
(3)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式________________________________________ 。

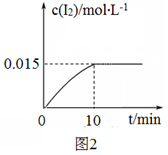
(4)砷酸钠(Na3AsO4)具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+ AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①0~10 min内,I−的反应速率v(I−)=______________ 。
②在该条件下,上述反应的平衡常数K=__________ 。
③升高温度,溶液中AsO43-的平衡转化率减小,则该反应的ΔH______ 0(填“大于”“小于”或“等于”)。
(5)已知砷酸(H3ASO4)是三元酸,有较强的氧化性。
①常温下砷酸的Ka1=6×10-3、Ka2=1×10-7,则 NaH2AsO4溶液中c(HAsO42-)___ c(H3AsO4)(填“>”、“<”或“=”)。
②某实验小组依据反应AsO43-+2H++2I-⇌AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响.测得输出电压与pH的关系如图。则a点时,盐桥中K+____ 移动(填“向左”、“向右”或“不”),c点时,负极的电极反应为____________________ 。

(1)砷化氢的电子式为
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒。As2O3是一种两性氧化物,写出As2O3溶于浓盐酸的化学方程式
(3)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式


(4)砷酸钠(Na3AsO4)具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+
 AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。①0~10 min内,I−的反应速率v(I−)=
②在该条件下,上述反应的平衡常数K=
③升高温度,溶液中AsO43-的平衡转化率减小,则该反应的ΔH
(5)已知砷酸(H3ASO4)是三元酸,有较强的氧化性。
①常温下砷酸的Ka1=6×10-3、Ka2=1×10-7,则 NaH2AsO4溶液中c(HAsO42-)
②某实验小组依据反应AsO43-+2H++2I-⇌AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响.测得输出电压与pH的关系如图。则a点时,盐桥中K+


您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】汽车尾气中含有CO、NO等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知:
①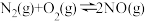
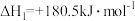
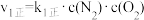 ,
,
②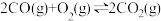
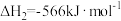
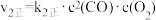 ,
,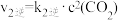
则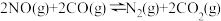
 =
=___________ ,请写出用k1正、k1逆、k2正、k2逆表示该反应在一定温度下的平衡常数表达式K=___________ 。
(2)某实验小组模拟汽车尾气CO与NO净化过程,将CO与NO混合气体充入密闭容器中,发生反应: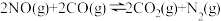 ,测得平衡时NO、CO的转化率(α)与起始投料比
,测得平衡时NO、CO的转化率(α)与起始投料比 关系如图1所示,v正~c(CO)的关系如图2所示。
关系如图1所示,v正~c(CO)的关系如图2所示。
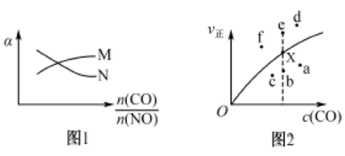
①图1中CO的转化率曲线为___________ (填“M”或“N”),图2中当X点升高到某一温度时,反应重新达到平衡,则变成相应的点为___________ (填图2中的字母)。
②一定温度下,若起始投料比 、反应开始刚性容器总压为80kPa,研究表明:该反应的正反应速率
、反应开始刚性容器总压为80kPa,研究表明:该反应的正反应速率 ,当反应达到平衡状态时测得该温度下
,当反应达到平衡状态时测得该温度下 ,则p(CO) =
,则p(CO) =___________ kPa,v正=___________ ( ),该温度下
),该温度下 的化学平衡常数Kp=
的化学平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
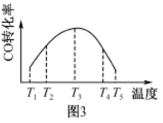
③为研究温度对CO转化率的影响,将一定量的CO与NO置于密闭容器中,保持相同的反应时间,CO转化率与温度关系如图3所示,在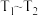 及
及 两个温度区间所示的CO转化率变化趋势不同,其原因是
两个温度区间所示的CO转化率变化趋势不同,其原因是___________ 。
(1)已知:
①
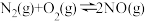
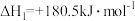
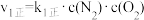 ,
,
②
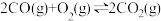
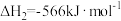
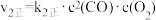 ,
,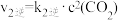
则
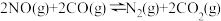
 =
=(2)某实验小组模拟汽车尾气CO与NO净化过程,将CO与NO混合气体充入密闭容器中,发生反应:
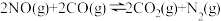 ,测得平衡时NO、CO的转化率(α)与起始投料比
,测得平衡时NO、CO的转化率(α)与起始投料比 关系如图1所示,v正~c(CO)的关系如图2所示。
关系如图1所示,v正~c(CO)的关系如图2所示。
①图1中CO的转化率曲线为
②一定温度下,若起始投料比
 、反应开始刚性容器总压为80kPa,研究表明:该反应的正反应速率
、反应开始刚性容器总压为80kPa,研究表明:该反应的正反应速率 ,当反应达到平衡状态时测得该温度下
,当反应达到平衡状态时测得该温度下 ,则p(CO) =
,则p(CO) = ),该温度下
),该温度下 的化学平衡常数Kp=
的化学平衡常数Kp=③为研究温度对CO转化率的影响,将一定量的CO与NO置于密闭容器中,保持相同的反应时间,CO转化率与温度关系如图3所示,在
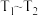 及
及 两个温度区间所示的CO转化率变化趋势不同,其原因是
两个温度区间所示的CO转化率变化趋势不同,其原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】利用 催化加氢合成二甲醚,其过程中同时发生以下两个主要反应:
催化加氢合成二甲醚,其过程中同时发生以下两个主要反应:
反应I:
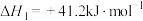
反应Ⅱ: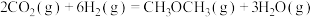

请回答:
(1)反应I的平衡常数表达式为
__________ ;反应Ⅱ发生自发反应的条件是__________ 。
(2)在一定温度和恒容条件下,可以作为判断上述两个反应均达到平衡状态的依据是__________。
(3)在恒压、 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如下图。(选择性的通俗理解:当两个反应同时发生时,选择更有利于哪个反应进行)
的选择性随温度的变化如下图。(选择性的通俗理解:当两个反应同时发生时,选择更有利于哪个反应进行)

①对于反应I,图中A点时,
__________  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
②可能有利于提高 平衡产率的措施有
平衡产率的措施有__________ 。
A.缩小容器的体积 B.升高反应的温度
C.选择更合适于反应Ⅱ的催化剂 D.适当调整 和
和 起始量的比例
起始量的比例
③图中温度高于300℃, 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是__________ 。
 催化加氢合成二甲醚,其过程中同时发生以下两个主要反应:
催化加氢合成二甲醚,其过程中同时发生以下两个主要反应:反应I:

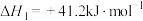
反应Ⅱ:
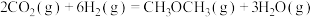

请回答:
(1)反应I的平衡常数表达式为

(2)在一定温度和恒容条件下,可以作为判断上述两个反应均达到平衡状态的依据是__________。
| A.体系内的压强保持不变 | B.两个反应的平衡常数不变 |
C. | D.反应体系中各物质的浓度不变 |
(3)在恒压、
 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如下图。(选择性的通俗理解:当两个反应同时发生时,选择更有利于哪个反应进行)
的选择性随温度的变化如下图。(选择性的通俗理解:当两个反应同时发生时,选择更有利于哪个反应进行)
①对于反应I,图中A点时,

 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)②可能有利于提高
 平衡产率的措施有
平衡产率的措施有A.缩小容器的体积 B.升高反应的温度
C.选择更合适于反应Ⅱ的催化剂 D.适当调整
 和
和 起始量的比例
起始量的比例③图中温度高于300℃,
 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】请回答下列问题
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是________ (填“强电解质”或“弱电解质”);
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是________ (填字母)。
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是_______ (填字母)。
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是__________ (用序号连接)
(3)对于2NO2(g) N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是____ 。

①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
(1)已知:25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.c(H+)/c(HA) B.c(HA)/ c (A-)
C.c(H+)与c(OH-)的乘积 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL与pH = 12的NaOH溶液V2 mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,现将足量AgCl分别放入:①100 mL 蒸馏水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
(3)对于2NO2(g)
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是
①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】肌肉中的肌红蛋白(Mb)可与O2结合生成MbO2:Mb(aq)+O2(g)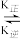 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=_______ kPa﹣1。(气体和溶液中的溶质分别用分压和物质的量浓度表达)
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=_______ (用含有k正、k逆的式子表示)。
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为_______ %(计算结果保留小数点后两位)
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时_______ (填“高”或“低”,下同);在温度不变的条件下,游客在高山山顶时体内MbO2的浓度比其在山下时_______ 。
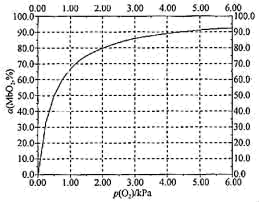
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向_______ 进行(填“左”或“右”),此时v正:v逆=_______ (填数值)。
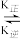 MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:
MbO2(aq)其中k正和k逆分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O2),v逆=k逆·c(MbO2)。37℃时测得肌红蛋白的结合度(α)与P(O2)的关系如下表[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的百分比]回答下列问题:| P(O2) | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
| α(MbO2%) | 50.0 | 67.0 | 80.0 | 85.0 | 88.0 | 90.3 | 91.0 |
(1)计算37℃、P(O2)为2.00kPa时,上述反应的平衡常数K=
(2)导出平衡时肌红蛋白与O2的结合度(α)与O2的压强[P(O2)]之间的关系式α=
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为
(4)一般情况下,高烧患者体内MbO2的浓度会比其健康时
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】在一容积为2 L的密闭容器内加入0.2 mol 的N2和0.6 mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
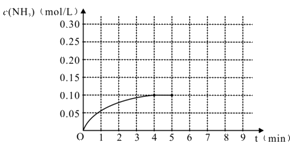
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为_________________ 。
(2)该反应的化学平衡常数表达式K=___________________ 。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________ 。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________ 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________ (填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。___________________
 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:
(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为
(2)该反应的化学平衡常数表达式K=
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
您最近一年使用:0次



