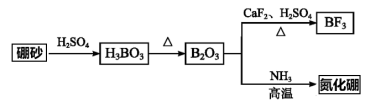
氮化硼是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到氮化硼和有机合成催化剂BF3的过程如下:___________ 杂化,BF3分子空间构型为___________ 。
(2)三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体的结构式:___________ (用←标注出其中的配位键)
(3)氮化硼晶体有多种相结构。六方相氮化硼(晶体结构如图所示)是通常存在的稳定相,可作高温润滑剂。立方相氮化硼(晶体结构如图所示)是超硬材料,有优异的耐磨性。___________ (填字母)。
A.两种晶体均为分子晶体 B.两种晶体中的B—N键均为共价键
C.六方相氮化硼层间作用力小,所以质地软 D.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B—N键数与硼原子数之比为___________ ,其结构与石墨相似却不导电,原因是___________ 。
③按粒子间作用力种类,与立方相氮化硼晶体类型相同的是___________ 。
A.干冰 B.铜 C.氯化铯晶体 D.晶体硅
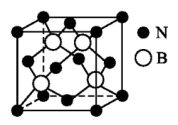
(4)利用“卤化硼法”也可合成含B和N两种元素的功能陶瓷,下图为该晶体的晶胞结构,该功能陶瓷晶体的化学式为___________ 。已知该晶胞的边长为a nm,则该晶体的密度为___________ g·cm-3(设NA为阿伏加德罗常数的数值)。
(2)三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体的结构式:
(3)氮化硼晶体有多种相结构。六方相氮化硼(晶体结构如图所示)是通常存在的稳定相,可作高温润滑剂。立方相氮化硼(晶体结构如图所示)是超硬材料,有优异的耐磨性。
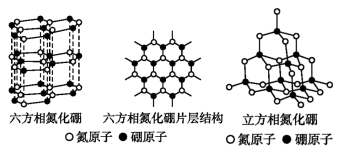
A.两种晶体均为分子晶体 B.两种晶体中的B—N键均为共价键
C.六方相氮化硼层间作用力小,所以质地软 D.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B—N键数与硼原子数之比为
③按粒子间作用力种类,与立方相氮化硼晶体类型相同的是
A.干冰 B.铜 C.氯化铯晶体 D.晶体硅
(4)利用“卤化硼法”也可合成含B和N两种元素的功能陶瓷,下图为该晶体的晶胞结构,该功能陶瓷晶体的化学式为
20-21高二下·天津滨海新·期末 查看更多[4]
天津市滨海新区2020-2021学年高二下学期期末考试化学试题重庆市缙云教育联盟2021-2022学年高三9月月度质量检测化学试题(已下线)题型01 分子的空间构型及杂化类型的判断-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)(已下线)综合01 物质结构与性质压轴80题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)
更新时间:2021-06-30 17:17:34
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】过渡金属及其化合物在生产生活中有着广泛应用。锰钢异常坚硬,且具抗冲击性能,是制造枪栓、保险库、挖掘机械和铁路设施的理想材料;锰也是人体的重要微量元素。请根据所学知识,回答下列问题:
(1)铬、锰、铁称为黑色金属,位于同一周期的相邻位置。锰的原子序数是______ ; 基态离子的价层电子排布图为
基态离子的价层电子排布图为______ 。
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是______ (填编号)。
A.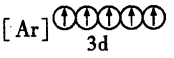 B.
B. 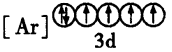
C. D.
D. 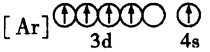
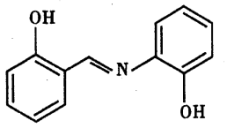
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与
形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与 形成配位键的原子有
形成配位键的原子有______ ;锰试剂______ (填“能”或“不能”)形成分子内氢键。
(4)锰试剂分子中,原子采取的杂化方式不涉及______ (填“ ”“
”“ ”或“
”或“ ”)杂化;分子中除氢以外的元素,第一电离能从小到大的顺序为
”)杂化;分子中除氢以外的元素,第一电离能从小到大的顺序为______ (用元素符号表示)。
(5)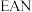 规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合
规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合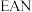 规则的配合物分子结构和化学性质都较稳定。已知
规则的配合物分子结构和化学性质都较稳定。已知 和
和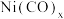 均符合
均符合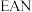 规则,性质稳定,而
规则,性质稳定,而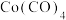 则容易在化学反应中表现氧化性。
则容易在化学反应中表现氧化性。
①x=______ 。
②从结构角度解释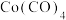 则容易在化学反应中表现氧化性的原因
则容易在化学反应中表现氧化性的原因______ 。
(1)铬、锰、铁称为黑色金属,位于同一周期的相邻位置。锰的原子序数是
 基态离子的价层电子排布图为
基态离子的价层电子排布图为(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是
A.
 B.
B. 
C.
 D.
D. 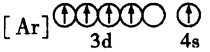
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与
形成黄色的配合物。锰试剂的结构如图所示,其分子中可能与 形成配位键的原子有
形成配位键的原子有
(4)锰试剂分子中,原子采取的杂化方式不涉及
 ”“
”“ ”或“
”或“ ”)杂化;分子中除氢以外的元素,第一电离能从小到大的顺序为
”)杂化;分子中除氢以外的元素,第一电离能从小到大的顺序为(5)
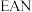 规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合
规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合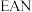 规则的配合物分子结构和化学性质都较稳定。已知
规则的配合物分子结构和化学性质都较稳定。已知 和
和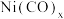 均符合
均符合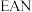 规则,性质稳定,而
规则,性质稳定,而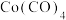 则容易在化学反应中表现氧化性。
则容易在化学反应中表现氧化性。①x=
②从结构角度解释
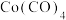 则容易在化学反应中表现氧化性的原因
则容易在化学反应中表现氧化性的原因
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】英菲替尼(化合物L)是治疗胆管癌的新型药物,其合成路线如下。
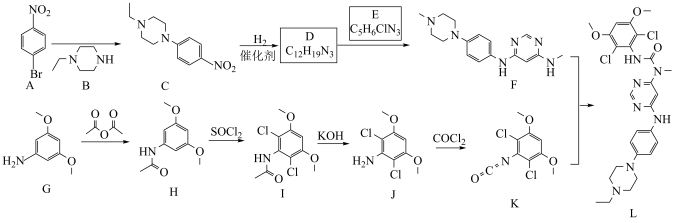
回答下列问题:
(1)A的化学名称是___________ 。
(2)由A生成C的反应类型是___________ 。
(3)E的结构简式为___________ 。
(4)由G→J的转化过程可知,G转化为H的目的是___________
(5)符合下列条件的B的同分异构体共有___________ 种,其中一种的结构简式为___________ 。
①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为___________ 。
(7)1,3-二苯基脲(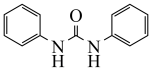 )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
)是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。 ___________

回答下列问题:
(1)A的化学名称是
(2)由A生成C的反应类型是
(3)E的结构简式为
(4)由G→J的转化过程可知,G转化为H的目的是
(5)符合下列条件的B的同分异构体共有
①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为
(7)1,3-二苯基脲(
 )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
)是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
您最近一年使用:0次
【推荐3】CuCl广泛应用于有机合成催化。例如 回答下列问题:
回答下列问题:
(1)CuCl中Cu+核外电子排布式为______________ ,Cu与Cl相比,第一电离能较大的是______________ 。
(2)已知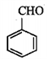 为平面分子,则-CHO中碳原子的杂化方式为
为平面分子,则-CHO中碳原子的杂化方式为______________ 。
(3)写出与CO互为等电子体的非极性分子的电子式______________ ,14gCO中含______________ molπ键。合成氨工业中用铜洗液吸收CO,形成配合物[Cu(NH3)3CO]Ac(HAc代表醋酸),其中______________ (填粒子符号)接受孤对电子形成配位键,配位数是______________ 。
(4)铜钙可形成合金,单质铜的熔点比单质钙高,其原因是____________________________ ,其中一种合金的晶胞结构构如图所示,已知:该晶体的密度为ρg·cm-3,NA是阿伏伽德罗常数的值,则其中两个Ca原子核之间距离为______________ 。
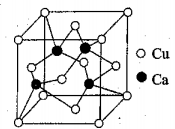
 回答下列问题:
回答下列问题:(1)CuCl中Cu+核外电子排布式为
(2)已知
 为平面分子,则-CHO中碳原子的杂化方式为
为平面分子,则-CHO中碳原子的杂化方式为(3)写出与CO互为等电子体的非极性分子的电子式
(4)铜钙可形成合金,单质铜的熔点比单质钙高,其原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】据报道,新疆南部发现稀有金属、铅、锌、铁、锰和金矿带约600 m。回答下列问题:
(1)基态锰的价层电子排布式为___________ ;预测:锰的第三电离能( )
)___________ (填“大于”“小于”或“等于”)铁的第三电离能( )。
)。
(2)氧化锰能催化氧化HCHO生成CO2和H2O。
①等物质的量的HCHO、CO2分子中π键数目之比为___________ 。
②在HCHO、CO2、H2O中,空间构型呈V形的分子是___________ 。
③HCHO中C原子的杂化类型是___________ 。
(3) 中不存在的作用力类型是___________(填字母)。
中不存在的作用力类型是___________(填字母)。
(4)配合物在水中的颜色与d轨道的分裂能有关。d轨道的分裂能是1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量。预测分裂能:
___________ (填“>”“<”或“=”)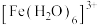 ,理由是
,理由是___________ 。
(5)铅晶胞如图所示。___________ ,它的配位数为___________ 。
②面心上六个铅原子相连构成的空间结构是___________ (填字母)。
A.正四方形 B.三角锥形 C.正八面体形 D.正四面体形
③已知:铅晶胞密度为 ,
, 代表阿伏加德罗常数的值。晶胞中两个面心上铅原子的最短距离为
代表阿伏加德罗常数的值。晶胞中两个面心上铅原子的最短距离为___________ pm。
(1)基态锰的价层电子排布式为
 )
) )。
)。(2)氧化锰能催化氧化HCHO生成CO2和H2O。
①等物质的量的HCHO、CO2分子中π键数目之比为
②在HCHO、CO2、H2O中,空间构型呈V形的分子是
③HCHO中C原子的杂化类型是
(3)
 中不存在的作用力类型是___________(填字母)。
中不存在的作用力类型是___________(填字母)。| A.非极性键 | B.配位键 | C.离子键 | D.金属键 |
(4)配合物在水中的颜色与d轨道的分裂能有关。d轨道的分裂能是1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量。预测分裂能:

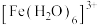 ,理由是
,理由是(5)铅晶胞如图所示。
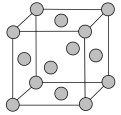
②面心上六个铅原子相连构成的空间结构是
A.正四方形 B.三角锥形 C.正八面体形 D.正四面体形
③已知:铅晶胞密度为
 ,
, 代表阿伏加德罗常数的值。晶胞中两个面心上铅原子的最短距离为
代表阿伏加德罗常数的值。晶胞中两个面心上铅原子的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____ ,与钛同周期的元素中,基态原子的未成对电子数与钛相同的元素分别是____ (填元素符号)。
(2)在浓的TiCl 3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配合物的化学式为______ ; 1mol该配合物中含有σ键的数目_______ 。
(3)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
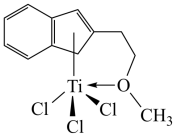
①组成M的元素中,电负性最大的是_________ (填名称)。
②M中非金属元素的第一电离能大小顺序_________ 。
③M中不含________ (填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(4)金红石(TiO 2)是含钛的主要矿物之一。其晶胞是典型的四方晶系,结构(晶胞中相同位置的原子相同)如图所示。
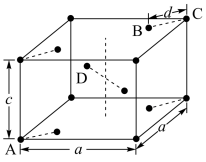
若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____ ,___ );钛氧键的键长d=______ (用代数式表示)。
(1)基态钛原子的价电子排布式为
(2)在浓的TiCl 3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配合物的化学式为
(3)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是
②M中非金属元素的第一电离能大小顺序
③M中不含
a.π键 b.σ键 c.离子键 d.配位键
(4)金红石(TiO 2)是含钛的主要矿物之一。其晶胞是典型的四方晶系,结构(晶胞中相同位置的原子相同)如图所示。

若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】主族元素碳、氧、氮、氟、磷、氯、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在___________ 对自旋相反的电子,基态氮原子的价层电子排布图为___________ 。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为___________ 其中氧原子的杂化方式为___________ 。
(3)基态Cl原子有___________ 种空间运动状态的电子,属于___________ 区(填“s”或“p”或“d”或“f”)。
(4)写出溴原子简化电子排布式:___________ 。溴的M层有___________ 种能量不同的电子。
(5)第三周期第一电离能处于Al和P之间的元素有___________ 种。
(6)某种原子的结构示意图为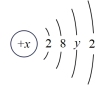 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为___________ 。
(7)一个青蒿素分子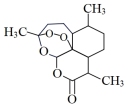 中含有
中含有___________ 个手性碳原子
(8)在[Ni(NH3)6]2+中存在的化学键有___________
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(9)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是___________ 。
(1)在基态14C原子中,核外存在
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
(3)基态Cl原子有
(4)写出溴原子简化电子排布式:
(5)第三周期第一电离能处于Al和P之间的元素有
(6)某种原子的结构示意图为
 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为(7)一个青蒿素分子
 中含有
中含有(8)在[Ni(NH3)6]2+中存在的化学键有
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(9)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】【化学—选修3:物质结构与性质】
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
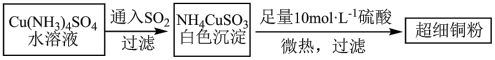
①铜元素位于周期表_________ 区;Cu+的基态价电子排布图_________ ;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为_________ (元素符号表示)。
②SO42-中心原子的杂化方式为_________ ,SO32-的价层电子互斥模型为_________ 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式_________ 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是_________ 。
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_________ 。
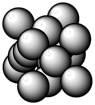
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为_________ ,用含有a、ρ的代数式表示的阿伏伽德罗常数为:_________ mol-1。
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
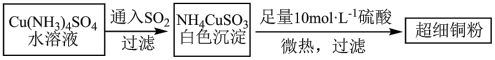
①铜元素位于周期表
②SO42-中心原子的杂化方式为
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的电子排布式为___________ ;价电子中成对电子数有___________ 个。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是___________ 。
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3___________ H3PO4 (填“>”或“<”)
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn___________ P。(填“>”、“<”或 “=”)
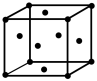
(4)某磷青铜晶胞结构如图所示。
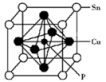
①则其化学式为___________ 。
②该晶体中距离Cu原子最近的Sn原子有___________ 个,这些Sn原子所呈现的构型为___________ 。
(1)基态铜原子的电子排布式为
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3
(3)磷青铜中的锡、磷两种元素电负性的大小为Sn
(4)某磷青铜晶胞结构如图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】工业上利用铁酸镓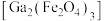 、铁酸锌
、铁酸锌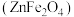 为原料可以提取铁、锌、镓,并采用MOCVD(金属有机物化学气相沉淀)技术制备砷化镓(GaAs),利用MOCVD技术制备GaAs的反应原理为
为原料可以提取铁、锌、镓,并采用MOCVD(金属有机物化学气相沉淀)技术制备砷化镓(GaAs),利用MOCVD技术制备GaAs的反应原理为 。
。
回答下列问题:
(1)基态铁原子的价层电子排布式为___________ 。
(2)在周期表中,铜和锌相邻。电离能:
___________  (填“>”“<”或“=”,下同),
(填“>”“<”或“=”,下同),
___________  。
。
(3) 、
、 分子相同的是___________(填字母)。
分子相同的是___________(填字母)。
(4)GaN、GaAs是常用的半导体材料,其晶体的熔点分别为1700℃、1238℃,前者熔点高于后者的主要原因是___________ ;它们的组成元素Ga、N、As的电负性由大到小的顺序是___________ 。
(5)砷化镓的晶胞结构如图所示。
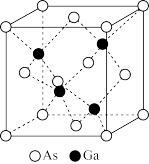
①镓原子可以看成是填充在砷原子构成的空隙中,镓原子填充这样的空隙中构成正四面体形,这样的空隙填充率为___________ 。
②设 是阿伏加德罗常数的值,晶体的密度为
是阿伏加德罗常数的值,晶体的密度为 。砷化镓晶胞中相邻两个面心上砷原子之间的距离为
。砷化镓晶胞中相邻两个面心上砷原子之间的距离为___________ pm(用含 、
、 的计算式表示)。
的计算式表示)。
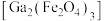 、铁酸锌
、铁酸锌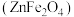 为原料可以提取铁、锌、镓,并采用MOCVD(金属有机物化学气相沉淀)技术制备砷化镓(GaAs),利用MOCVD技术制备GaAs的反应原理为
为原料可以提取铁、锌、镓,并采用MOCVD(金属有机物化学气相沉淀)技术制备砷化镓(GaAs),利用MOCVD技术制备GaAs的反应原理为 。
。回答下列问题:
(1)基态铁原子的价层电子排布式为
(2)在周期表中,铜和锌相邻。电离能:

 (填“>”“<”或“=”,下同),
(填“>”“<”或“=”,下同),
 。
。(3)
 、
、 分子相同的是___________(填字母)。
分子相同的是___________(填字母)。| A.空间构型 | B.中心原子的杂化轨道类型 | C.分子极性 | D.化学键类型 |
(5)砷化镓的晶胞结构如图所示。

①镓原子可以看成是填充在砷原子构成的空隙中,镓原子填充这样的空隙中构成正四面体形,这样的空隙填充率为
②设
 是阿伏加德罗常数的值,晶体的密度为
是阿伏加德罗常数的值,晶体的密度为 。砷化镓晶胞中相邻两个面心上砷原子之间的距离为
。砷化镓晶胞中相邻两个面心上砷原子之间的距离为 、
、 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硫化氢有毒是大气污染物,硫化氢的产生和治理是环境保护研究的重要问题,
(1)蛋白质在厌氧菌的作用下会生成H2S,
例如半胱氨酸在厌氧条件下的反应式如下:
HOOC-CH(NH2)CH2SH+2H2O→CH3COOH+HCOOH+NH3+H2S
回答下列问题:
①下列硫原子能量最高的是___________ 。
A.[He] 2s2 2p6 3s2 3p4 B.[He] 2s1 2p6 3s1 3p6
C.[He] 2s0 2p6 3s2 3p6 D.[He] 2s2 2p6 3s1 3p5
②甲基的供电子能力强于氢原子,则酸性:CH3COOH___________ HCOOH(填“>”“ <”)。
③氨分子中N-H键角比水分子的O-H键角大的原因是___________ 。
④半胱氨酸既能与酸反应,又能与碱反应,与酸反应通过形成___________ 键结合H+生成盐。半胱酰胺中有___________ 个手性碳原子。
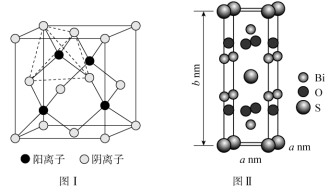
(2)硫化废物的产生除了有机物的分解,还有矿物的开采和硫化物的合成,闪锌矿(主要成分硫化锌),结构如I图,锌的位置为S的___________ 空隙处。人工合成Bi2O2S的结构如图II,结构中硫的配位数为___________ ,该晶体的密度为ρ g·cm3,NA为阿伏加德罗常数的值,该物质的摩尔质量可表示为___________ 。
(1)蛋白质在厌氧菌的作用下会生成H2S,
例如半胱氨酸在厌氧条件下的反应式如下:
HOOC-CH(NH2)CH2SH+2H2O→CH3COOH+HCOOH+NH3+H2S
回答下列问题:
①下列硫原子能量最高的是
A.[He] 2s2 2p6 3s2 3p4 B.[He] 2s1 2p6 3s1 3p6
C.[He] 2s0 2p6 3s2 3p6 D.[He] 2s2 2p6 3s1 3p5
②甲基的供电子能力强于氢原子,则酸性:CH3COOH
③氨分子中N-H键角比水分子的O-H键角大的原因是
④半胱氨酸既能与酸反应,又能与碱反应,与酸反应通过形成
(2)硫化废物的产生除了有机物的分解,还有矿物的开采和硫化物的合成,闪锌矿(主要成分硫化锌),结构如I图,锌的位置为S的

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有短周期元素性质的部分数据如下表,其中x的值表示不同元素的原子吸引电子的能力大小,若x值越大,元素的非金属性越强,金属性越弱。x值相对较大的元素在所形成的分子中化合价为负。⑩原子的核外电子层数与核外电子总数相同。
(1)根据以上条件,推断③④⑤的元素符号分别为:___ ,__ ,__ 。
(2)②的最高价氧化物的固体属于__ 晶体,空间构型__ 。
(3)用电子式表示下列原子相互结合成的化合物电子式:
①+⑦+⑩:___ ,
①+⑩形成原子个数比为1:1的化合物:__ 。
(4)写出①与⑦所形成仅含离子键的化合物和④与⑩所形成的化合物反应的离子方程式:___ 。
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| x | 3.44 | 2.55 | 0.98 | 3.16 | 2.19 | 3.98 | 0.93 | 3.04 | 1.91 | |
| 常见化合价 | 最高价 | +4 | +1 | +1 | +4 | |||||
| 最低价 | -2 | -1 | -3 | -1 | -3 | |||||
(1)根据以上条件,推断③④⑤的元素符号分别为:
(2)②的最高价氧化物的固体属于
(3)用电子式表示下列原子相互结合成的化合物电子式:
①+⑦+⑩:
①+⑩形成原子个数比为1:1的化合物:
(4)写出①与⑦所形成仅含离子键的化合物和④与⑩所形成的化合物反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(1)氯酸钾熔化,粒子间克服了________ ;(填“离子键”“共价键”或“分子间作用力”,下同);二氧化硅熔化,粒子间克服了______ ;碘升华,粒子间克服了______ 。三种晶体的熔点由高到低的顺序是______ 。
(2)下列六种晶体:①CO2、②NaCl、③Na、④Si、⑤CS2、⑥金刚石,它们的熔点由低到高的顺序为_______ (用序号表示)。
(3)A、B、C、D为四种不同类型的晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。
试推断它们的晶体类型:A.____________ ;B.____________ ;C.____________ ;D.____________ 。
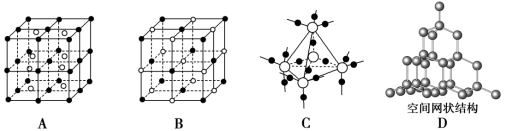
(4)A~D是化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.____________ ;B.____________ ;C.____________ ;D.____________ 。
(2)下列六种晶体:①CO2、②NaCl、③Na、④Si、⑤CS2、⑥金刚石,它们的熔点由低到高的顺序为
(3)A、B、C、D为四种不同类型的晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。
试推断它们的晶体类型:A.
(4)A~D是化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.

您最近一年使用:0次



