CuCl广泛应用于有机合成催化。例如 回答下列问题:
回答下列问题:
(1)CuCl中Cu+核外电子排布式为______________ ,Cu与Cl相比,第一电离能较大的是______________ 。
(2)已知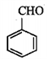 为平面分子,则-CHO中碳原子的杂化方式为
为平面分子,则-CHO中碳原子的杂化方式为______________ 。
(3)写出与CO互为等电子体的非极性分子的电子式______________ ,14gCO中含______________ molπ键。合成氨工业中用铜洗液吸收CO,形成配合物[Cu(NH3)3CO]Ac(HAc代表醋酸),其中______________ (填粒子符号)接受孤对电子形成配位键,配位数是______________ 。
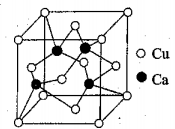
(4)铜钙可形成合金,单质铜的熔点比单质钙高,其原因是____________________________ ,其中一种合金的晶胞结构构如图所示,已知:该晶体的密度为ρg·cm-3,NA是阿伏伽德罗常数的值,则其中两个Ca原子核之间距离为______________ 。
 回答下列问题:
回答下列问题:(1)CuCl中Cu+核外电子排布式为
(2)已知
 为平面分子,则-CHO中碳原子的杂化方式为
为平面分子,则-CHO中碳原子的杂化方式为(3)写出与CO互为等电子体的非极性分子的电子式
(4)铜钙可形成合金,单质铜的熔点比单质钙高,其原因是

更新时间:2018-03-29 20:47:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】在周期表中1~36号元素之间的A、B、C、D、E五种元素,它们的原子序数依次增大,已知A与其余四种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E元素位于周期表的ds区,其基态原子最外能层只有一个电子。
(1)写出基态E原子的简化电子排布式_______ ,C的单质的电子式_______ 。
(2)A与B形成的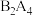 分子中,σ键和π键的个数比为
分子中,σ键和π键的个数比为_______ ,分子中B原子的杂化类型为_______ 。
(3)A与C形成 型分子,实验室制取
型分子,实验室制取 的化学方程式为
的化学方程式为_______ 。C的最高价氧化物的水化物与 所形成的盐呈酸性的原因
所形成的盐呈酸性的原因_______ (用离子方程式表示)
(4)B、C、D三种元素第一电离能由大到小的顺序为_______ (用元素符号表示)。
(5)已知D、E能形成一种化合物,其晶胞的结构如图所示,与D配位的E所形成的空间结构为_______ ,若该晶胞的棱长为apm,阿伏加德罗常数的数值为NA,则该晶体的密度为_______  (用含a、NA的符号表示)。
(用含a、NA的符号表示)。

(1)写出基态E原子的简化电子排布式
(2)A与B形成的
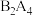 分子中,σ键和π键的个数比为
分子中,σ键和π键的个数比为(3)A与C形成
 型分子,实验室制取
型分子,实验室制取 的化学方程式为
的化学方程式为 所形成的盐呈酸性的原因
所形成的盐呈酸性的原因(4)B、C、D三种元素第一电离能由大到小的顺序为
(5)已知D、E能形成一种化合物,其晶胞的结构如图所示,与D配位的E所形成的空间结构为
 (用含a、NA的符号表示)。
(用含a、NA的符号表示)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示为元素周期表的一部分,其中的编号代表对应的元素。
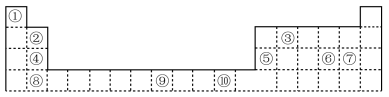
完成下列填空。
(1)表中属于d区的元素是_______ (填编号);④⑤⑥⑦⑧五种元素形成的稳定离子中,离子半径最小的是_______ (填离子符号)。
(2)表中元素③所形成的化合物种类最多,任意写出2种它与元素⑦组成的非极性分子的分子式_______ 。
(3)④⑤⑥三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是_______ (填化学式),碱性最强的是_______ (填化学式)。
(5)用原子结构的知识解释元素②、④的金属性强弱。______ 。

完成下列填空。
(1)表中属于d区的元素是
(2)表中元素③所形成的化合物种类最多,任意写出2种它与元素⑦组成的非极性分子的分子式
(3)④⑤⑥三种元素的第一电离能由大到小的顺序是
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是
(5)用原子结构的知识解释元素②、④的金属性强弱。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】天宫空间站有两对单翼翼展约30米的柔性太阳翼。关键部件为高性能颗粒增强铝基复合材料(SiC/Al)。请回答:
(1)基态Si的价电子轨道表示式是______ 。碳化硅的晶体类型是______ 晶体。
(2)矾土含Al3+,《诗经》言“缟衣茹蘆(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。
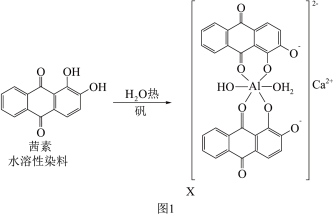
①C、N、O、Al的第一电离能从大到小的顺序为______ 。
②C的杂化轨道类型是______ 。
③茜素水溶性较好的原因是______ 。
(3)某硅、铁化合物晶胞如图2,铁有两种位置,分别用Fe1、Fe2(未画出)表示,Fe2占据硅形成的所有正四面体空隙。
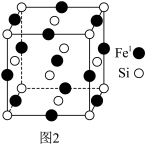
①距离Fe1最近的Fe1有______ 个。
②若将Fe1置于晶胞顶点,则位于此晶胞面心、体心的原子分别是______ 、______ (选填“Si”,“Fe1”、“Fe2”)。
③若晶胞的边长为apm,请计算该晶胞的密度为______ 。
(1)基态Si的价电子轨道表示式是
(2)矾土含Al3+,《诗经》言“缟衣茹蘆(茜草)”,茜草中的茜素与矾土中的Al3+、Ca2+生成的红色配合物X是最早的媒染染料。

①C、N、O、Al的第一电离能从大到小的顺序为
②C的杂化轨道类型是
③茜素水溶性较好的原因是
(3)某硅、铁化合物晶胞如图2,铁有两种位置,分别用Fe1、Fe2(未画出)表示,Fe2占据硅形成的所有正四面体空隙。

①距离Fe1最近的Fe1有
②若将Fe1置于晶胞顶点,则位于此晶胞面心、体心的原子分别是
③若晶胞的边长为apm,请计算该晶胞的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】Q、R、X、Y、Z为短周期主族元素,且原子序数依次递增。Q的低价氧化物与R单质分子的电子总数相等,X与Q同族,Y和Z的离子与Ar原子的电子结构相同。
(1)Q的最高价氧化物中Q的杂化类型为___ ,分子中含有___ 个σ键,___ 个π键。
(2)X的氢化物分子的立体构型是___ ,属于__ 分子(填“极性”或“非极性”);它与R形成的化合物可作为一种重要的陶瓷材料,其化学式是___ 。
(3)Q分别与Y、Z形成的共价化合物的化学式是___ 和___ ;Q与Y形成的分子的电子式是__ ,属于___ 分子(填“极性”或“非极性”)。
(1)Q的最高价氧化物中Q的杂化类型为
(2)X的氢化物分子的立体构型是
(3)Q分别与Y、Z形成的共价化合物的化学式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】氮化硼是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到氮化硼和有机合成催化剂BF3的过程如下:
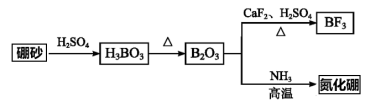
(1)BF3中B原子的杂化轨道类型为___________ 杂化,BF3分子空间构型为___________ 。
(2)三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体的结构式:___________ (用←标注出其中的配位键)
(3)氮化硼晶体有多种相结构。六方相氮化硼(晶体结构如图所示)是通常存在的稳定相,可作高温润滑剂。立方相氮化硼(晶体结构如图所示)是超硬材料,有优异的耐磨性。
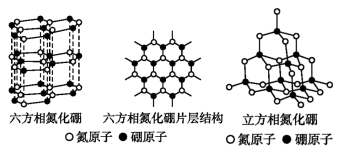
①关于这两种晶体的说法,不正确的是___________ (填字母)。
A.两种晶体均为分子晶体 B.两种晶体中的B—N键均为共价键
C.六方相氮化硼层间作用力小,所以质地软 D.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B—N键数与硼原子数之比为___________ ,其结构与石墨相似却不导电,原因是___________ 。
③按粒子间作用力种类,与立方相氮化硼晶体类型相同的是___________ 。
A.干冰 B.铜 C.氯化铯晶体 D.晶体硅
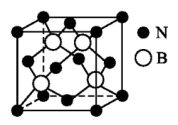
(4)利用“卤化硼法”也可合成含B和N两种元素的功能陶瓷,下图为该晶体的晶胞结构,该功能陶瓷晶体的化学式为___________ 。已知该晶胞的边长为a nm,则该晶体的密度为___________ g·cm-3(设NA为阿伏加德罗常数的数值)。

(1)BF3中B原子的杂化轨道类型为
(2)三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体的结构式:
(3)氮化硼晶体有多种相结构。六方相氮化硼(晶体结构如图所示)是通常存在的稳定相,可作高温润滑剂。立方相氮化硼(晶体结构如图所示)是超硬材料,有优异的耐磨性。

①关于这两种晶体的说法,不正确的是
A.两种晶体均为分子晶体 B.两种晶体中的B—N键均为共价键
C.六方相氮化硼层间作用力小,所以质地软 D.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B—N键数与硼原子数之比为
③按粒子间作用力种类,与立方相氮化硼晶体类型相同的是
A.干冰 B.铜 C.氯化铯晶体 D.晶体硅
(4)利用“卤化硼法”也可合成含B和N两种元素的功能陶瓷,下图为该晶体的晶胞结构,该功能陶瓷晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知Mn、Fe、Co是组成合金的重要元素,P、S、Cl是农药中的重要元素。回答下列问题:
(1)Mn元素位于元素周期表的______ 区,基态锰原子的价电子排布图为_____ 。
(2)P、S、Cl三种元素的第一电离能由大到小顺序为________ 。
(3)已知NH3的沸点高于PH3,原因是________ 。
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为: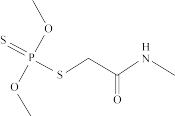 ,其中N原子的杂化类型为
,其中N原子的杂化类型为________ 。
(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为_______ 。
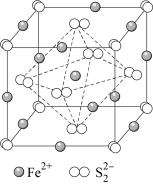
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S 的数目为
的数目为_____ 。如可用晶胞参数为单位长度建立的坐标系表示晶胞中各原子的位置,并称作原子分数坐标,则该晶胞中体心Fe2+的坐标为__________ 。
(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =______ (用d、NA表示a)。
(1)Mn元素位于元素周期表的
(2)P、S、Cl三种元素的第一电离能由大到小顺序为
(3)已知NH3的沸点高于PH3,原因是
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为:
 ,其中N原子的杂化类型为
,其中N原子的杂化类型为(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S
 的数目为
的数目为(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =

您最近一年使用:0次
【推荐1】按要求回答下列问题:
Ⅰ.在下列物质中:①CO2 ②KCl ③Ne ④金刚石 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2H4 ⑧SiO2
⑨液氨 ⑩SO3 ⑪NaCl,其中(1)~(4)题填写序号。
(1)既有离子键,又有极性键的是_______ 。
(2)含有非极性键的分子晶体是_______ 。
(3)①、②、④、⑨、⑪中,熔点由高到低的顺序为_______ 。
(4)①、④、⑨、⑩键角由大到小的顺序为_______ 。
(5)平均1molSiO2中,含有共价键数目为_______ 。
Ⅱ.
(6)金红石型TiO2的晶胞为长方体,晶胞参数如图所示。
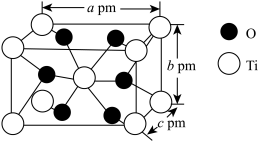
TiO2的摩尔质量为Mg/mol,阿伏加德罗常数为NA,该晶体的密度为_______ g/cm3。
(7)(CN)2是一种与Cl2性质相似的气体,分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式_______ ,分子中σ键与π键数目之比为_______ ,(CN)2分子为_______ (填“极性分子”或“非极性分子”)。
(8)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_______ 。
(9)布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的成酯修饰以减轻副作用:
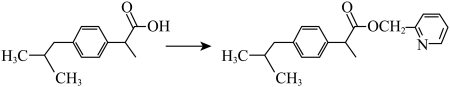
请用“*”标出以上两种分子中的所有手性碳原子_______ 。
Ⅰ.在下列物质中:①CO2 ②KCl ③Ne ④金刚石 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2H4 ⑧SiO2
⑨液氨 ⑩SO3 ⑪NaCl,其中(1)~(4)题填写序号。
(1)既有离子键,又有极性键的是
(2)含有非极性键的分子晶体是
(3)①、②、④、⑨、⑪中,熔点由高到低的顺序为
(4)①、④、⑨、⑩键角由大到小的顺序为
(5)平均1molSiO2中,含有共价键数目为
Ⅱ.
(6)金红石型TiO2的晶胞为长方体,晶胞参数如图所示。

TiO2的摩尔质量为Mg/mol,阿伏加德罗常数为NA,该晶体的密度为
(7)(CN)2是一种与Cl2性质相似的气体,分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式
(8)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
(9)布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的成酯修饰以减轻副作用:

请用“*”标出以上两种分子中的所有手性碳原子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有X、Y、Z、W、Q五种元素,它们的核电荷数依次增大,且都小于20,其中X为非金属元素。X和Q属于同一族,它们原子的最外层电子排布式为ns1;Y和W也属于同一族,它们原子的最外层的p能级电子数是s能级电子数的两倍;Z原子最外层上电子数等于W原子最外层上电子数的一半。请回答下列问题:
(1)X、Y可形成一种绿色氧化剂A,则A为__ (“极性分子”或“非极性分子”);试写出Cu、稀硫酸与A反应制备CuSO4的离子方程式___ 。
(2)由这5种元素组成的一种化合物是__ (填化学式),该物质主要用途是__ ,并解释其原理___ 。
(3)在第四周期中,与Z元素原子未成对电子数相同的金属元素有___ 种,该元素氯化物的二聚分子结构如图所示,在此化合物中Z原子的杂化类型为___ ,该化合物在熔融状态下___ 导电(“能”或“不能”)。
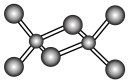
(4)分子WY2、WY3的键角相比,更大的是___ (填化学式),写出两种与WY3互为等电子体的微粒___ 。
(1)X、Y可形成一种绿色氧化剂A,则A为
(2)由这5种元素组成的一种化合物是
(3)在第四周期中,与Z元素原子未成对电子数相同的金属元素有

(4)分子WY2、WY3的键角相比,更大的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中⑨号属于______ 区元素。
(2)③和⑧形成的一种常见溶剂,其分子立体空间构型为________ 。
(3)元素①和⑥形成的最简单分子X属于________ 分子(填“极性”或“非极性”)
(4)元素⑥的第一电离能________ 元素⑦的第一电离能;元素②的电负性________ 元素④的电负性(选填“>”、“=”或“<”)。
(5)元素⑨的基态原子核外价电子排布式是________ 。
(6)元素⑧和④形成的化合物的电子式为________ 。
(7)某些不同族元素的性质也有一定的相似性,如表中元素⑩与元素⑤的氢氧化物有相似的性质。请写出元素⑩的氢氧化物与NaOH溶液反应的化学方程式:____________________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | ⑩ |
请回答下列问题:
(1)表中⑨号属于
(2)③和⑧形成的一种常见溶剂,其分子立体空间构型为
(3)元素①和⑥形成的最简单分子X属于
(4)元素⑥的第一电离能
(5)元素⑨的基态原子核外价电子排布式是
(6)元素⑧和④形成的化合物的电子式为
(7)某些不同族元素的性质也有一定的相似性,如表中元素⑩与元素⑤的氢氧化物有相似的性质。请写出元素⑩的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子排布式为_______ ;第一电离能
_______ 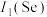 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是_______ 。
(2) 是一种剧毒气体,其中心原子杂化轨道类型
是一种剧毒气体,其中心原子杂化轨道类型_______ 。
(3) 的熔点约为712℃,
的熔点约为712℃, 的熔点约为194℃,其晶体类型分别是
的熔点约为194℃,其晶体类型分别是_______ 、_______ 。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止 刻蚀液与下层GaAs(砷化镓)反应。
刻蚀液与下层GaAs(砷化镓)反应。
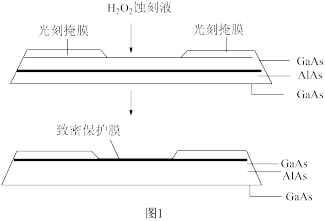
①上述致密保护膜是一种常见的金属氧化物,其化学式为_______ 。
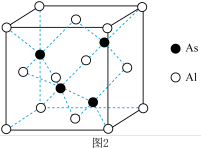
②已知AlAs的立方晶胞如图2所示,其中As的配位数为_______ ;该晶体密度为 ,设
,设 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为_______ pm。
(1)基态As原子的核外价电子排布式为

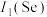 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是(2)
 是一种剧毒气体,其中心原子杂化轨道类型
是一种剧毒气体,其中心原子杂化轨道类型(3)
 的熔点约为712℃,
的熔点约为712℃, 的熔点约为194℃,其晶体类型分别是
的熔点约为194℃,其晶体类型分别是(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止
 刻蚀液与下层GaAs(砷化镓)反应。
刻蚀液与下层GaAs(砷化镓)反应。

①上述致密保护膜是一种常见的金属氧化物,其化学式为
②已知AlAs的立方晶胞如图2所示,其中As的配位数为
 ,设
,设 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】国内外学者近年来对金属-有机框架(MOFs)作为催化剂光解制氢和还原CO2等方面的研究取得了丰硕的成果。其中Masaya 等人利用Ti- MOF-NH2、H2PtCl6、 DMF 等原料制备了催化剂Pt/Ti- MOF-NH2,回答下列问题:
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是_______ ,处于_______ 区,未成对电子数是_______ 。
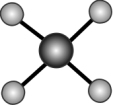
(2)PtCl 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是_______ , 中心原子采用的杂化类型可能是_______ (填 “dsp2”“sp3”“sp2”或“sp3d2”)。
(3)DMF的结构是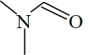 ,σ键与π键的数目比是
,σ键与π键的数目比是_______ ,其中N原子的杂化方式是_______ 。
(4)已知pKa=-lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因_______ 。
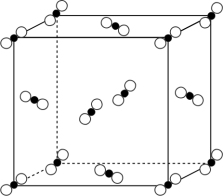
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。若阿伏加德罗常数为NA, 干冰的密度为ρg·cm-3, 则晶胞体对角线长度是_______ cm。
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是
(2)PtCl
 的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
的价层电子对互斥模型如图所示,已知该离子是平面形结构,则该离子中的键角是
(3)DMF的结构是
 ,σ键与π键的数目比是
,σ键与π键的数目比是(4)已知pKa=-lgKa,CCl3CH2OH 的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因
(5)一定条件下, CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。若阿伏加德罗常数为NA, 干冰的密度为ρg·cm-3, 则晶胞体对角线长度是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】锗及其化合物广泛用于半导体、催化剂、光伏、制药工业。回答下列问题:
(1)锗的基态原子核外电子排布式为_______ 。
(2)硅、锗、铅的氯化物的熔点如下表:
① 的分子空间构型为
的分子空间构型为_______ 。
②熔点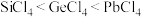 的原因是
的原因是_______ 。
(3)有机锗被称为“生命的奇效元素”,在医疗上具有重要应用。一种锗的有机配合物合成方法如下:
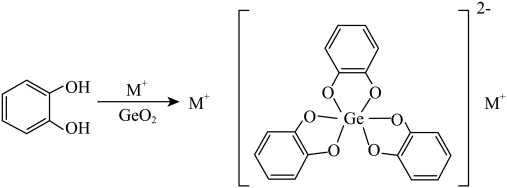
该有机配合物中锗的配位数为_______ ,其阴离子中C、 、O元素的第一电离能从大到小顺序为
、O元素的第一电离能从大到小顺序为_______ 。
(4)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):
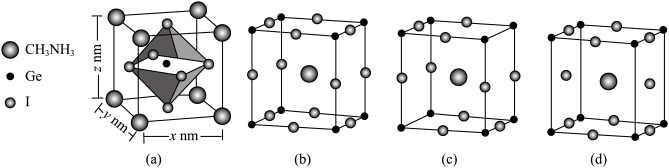
①该锗化合物晶胞的表示方式有多种,图中_______ (填“b”“c”或“d”)图也能表示此化合物的晶胞。
②用 表示阿伏加德罗常数的数值,计算晶胞(a)密度为
表示阿伏加德罗常数的数值,计算晶胞(a)密度为_______  (用含x、y、z和
(用含x、y、z和 的式子表示)。
的式子表示)。
(1)锗的基态原子核外电子排布式为
(2)硅、锗、铅的氯化物的熔点如下表:
| 物质 |  |  | 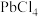 |
熔点( ) ) | 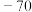 | 约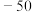 |  |
①
 的分子空间构型为
的分子空间构型为②熔点
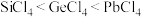 的原因是
的原因是(3)有机锗被称为“生命的奇效元素”,在医疗上具有重要应用。一种锗的有机配合物合成方法如下:

该有机配合物中锗的配位数为
 、O元素的第一电离能从大到小顺序为
、O元素的第一电离能从大到小顺序为(4)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):

①该锗化合物晶胞的表示方式有多种,图中
②用
 表示阿伏加德罗常数的数值,计算晶胞(a)密度为
表示阿伏加德罗常数的数值,计算晶胞(a)密度为 (用含x、y、z和
(用含x、y、z和 的式子表示)。
的式子表示)。
您最近一年使用:0次



