常温下,向20 mL浓度均为0.1 mol/L HX和CH3COOH的混合溶液中滴加0.1 mol/L的氨水,测得溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积(V)的关系如图。(CH3COOH的Ka=1.8×10-5,NH3·H2O的Kb=1.8×10-5)下列说法正确的是
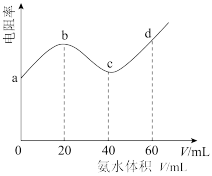

| A.同浓度的HX比CH3COOH的pH大 |
| B.a→c过程,水的电离程度逐渐减小 |
C.c点时,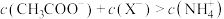 |
D.d点时, |
更新时间:2021-07-20 11:04:12
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知H2CO3的酸性强于H2S,将a mol·L-1NaHS与b mol·L-1NaOH两种稀溶液等体积混合(a>0,b>0),所得溶液中微粒间的物质的量浓度关系正确的是
| A.a=b时:c(OH-)=c(H+)+c(HS-) |
| B.a=2b时:c(S2-)>c(HS-)>c(OH-)>c(H+) |
| C.a=3b时:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| D.a=4b时:4c(Na+)=5c(S2-)+5c(HS-)+5c(H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列有关溶液中微粒的物质的量浓度关系正确的是
| A.1L 0.1 mol·L-1(NH4)2Fe(SO4)2 的溶液中c(NH4+) + c(Fe2+)+ c(H+)= c(OH−)+ c(SO42−) |
| B.0.1 mol·L-1 NH4HS溶液中:c(NH4+) < c(HS−) + c(S2−) + c(H2S) |
| C.0.1 mol·L-1pH为 4的 NaHA溶液中:c(HA−) > c(H2A) > c(A2−) |
| D.等浓度的碳酸钠和碳酸氢钠溶液混合后的溶液中:c(OH−) + c(CO32−) = c(HCO3−) + 3c(H2CO3) + 2c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NA为阿伏加德罗常数的值。下列有关说法正确的是
| A.室温下,22. 4L乙烷中含有的碳原子数小于2NA |
B.1L 0.1mol/L NH4Cl溶液中 的数目为0.1NA 的数目为0.1NA |
| C.标准状况下,11. 2L CHCl3中所含的氯原子数为1. 5NA |
| D.室温下,27g Al与足量浓硫酸反应,转移的电子数为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列各组离子在相应的条件下可能大量共存的是
| A.0.1 mol/LNaHSO4溶液中:Al3+、[Ag(NH3)2]+、Cl- |
B.由水电离产生的c水(OH-)=1×10-10 mol/L的溶液中:ClO-、Mg2+、Na+、 |
C.在 =1×1012的溶液中: =1×1012的溶液中: 、Fe2+、Cl-、 、Fe2+、Cl-、 |
| D.0.1 mol/LBa(OH)2溶液:Na+、K+、Cl-、ClO- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,用 NaOH溶液滴定20.00 mL
NaOH溶液滴定20.00 mL 
 溶液的滴定曲线如图所示。下列说法错误的是
溶液的滴定曲线如图所示。下列说法错误的是

 NaOH溶液滴定20.00 mL
NaOH溶液滴定20.00 mL 
 溶液的滴定曲线如图所示。下列说法错误的是
溶液的滴定曲线如图所示。下列说法错误的是
| A.点①、②、③所示溶液中,水的电离程度最大的为③ |
B.点③所示溶液,加水稀释, 不变 不变 |
C.点③所示溶液中: |
D.点①所示溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1的HA溶液和HB溶液,所得滴定曲线如图。下列说法正确的是
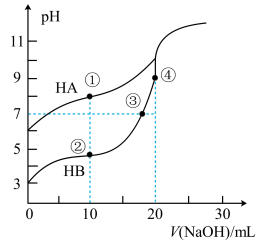

| A.HA和HB均为弱酸,且酸性HA>HB |
| B.点①和②所示溶液中:c(B-)-c(A-)=c(HA)-c(HB) |
| C.点③所示溶液中:c(B-)<c(Na+) |
| D.点④所示溶液中:c(Na+)>c(OH-)>c(B-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,向10mL0.10mol/L的一元弱酸HA(Ka=1.0×10-3)中逐滴加入0.10mol/LNaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。下列说法不正确的是
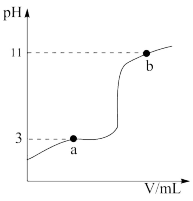

| A.V=10mL时,c(OH-)=c(HA)+c(H+) |
| B.b点时,c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.溶液在a点和b点时水的电离程度相同 |
| D.a点时,c(HA)+c(OH-)=c(Na+)+c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,向10.00mL0.1000mol·L-1HX中滴加0.1000mol·L-1NaOH溶液。溶液的pH随NaOH溶液体积的变化如图。下列说法错误的是( )


| A.滴定时选用甲基橙作指示剂 |
| B.HX的电离平衡常数的数量级为10-3 |
| C.a点溶液中存在c(Na+)=c(X-) |
| D.滴定至a点时消耗NaOH溶液的体积V1<10mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】Na2C2O4可用作抗凝血剂。室温下,通过下列实验探究Na2C2O4溶液的性质。
下列有关说法不 正确的是
| 实验 | 实验操作和现象 |
| 1 | 测得0.1mol·L-1Na2C2O4溶液的pH≈8.4 |
| 2 | 向0.2mol·L-1Na2C2O4溶液中加入等体积0.2mol·L-1盐酸,测得混合后溶液的pH≈5.5 |
| 3 | 向0.1mol·L-1Na2C2O4溶液中滴加几滴酸性KMnO4溶液,振荡,溶液仍为无色 |
| 4 | 向0.1mol·L-1Na2C2O4溶液中加入等体积0.1mol·L-1CaCl2溶液,产生白色沉淀 |
A.0.1mol·L-1Na2C2O4溶液中存在c(OH-)=c(H+)+2c(H2C2O4)+c( ) ) |
B.实验2得到的溶液中有c(Cl-)>c( )>c(H2C2O4) )>c(H2C2O4) |
C.实验3中 被还原成Mn2+,则反应的离子方程式为2 被还原成Mn2+,则反应的离子方程式为2 +5 +5 +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
D.实验4中c(Na+)=2c(H2C2O4)+2c( )+2c( )+2c( ) ) |
您最近一年使用:0次

 数等于0.1NA
数等于0.1NA

