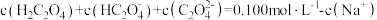常温下,浓度均为0.1mol·L-1的三种溶液:①醋酸溶液②醋酸钠溶液③碳酸钠溶液。已知醋酸的电离平衡常数为K=1.8×10-5。下列说法正确的是
| A.溶液中c(CH3COO-):①>② |
| B.溶液的pH:②<③<① |
| C.水的电离程度:①<②<③ |
| D.①与②等体积混合溶液中:c(CH3COO-)>c(CH3COOH) |
20-21高二上·河北石家庄·阶段练习 查看更多[2]
河北正定中学2020-2021学年高二上学期第一次半月考化学试题(已下线)3.3.4 溶液中粒子浓度的关系(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
更新时间:2021-09-16 11:06:05
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将铁粉和活性炭的混合物用NaCl溶液湿润后,置于试管中,5min后测得试管内压强变小 | 说明铁粉发生了吸氧腐蚀 |
| B | 室温下,向0.1mol·L-1HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | CH3COOH电离出H+的能力比HNO2弱 |
| D | 向CH3COONa溶液中滴加酚酞,加热(忽略水的蒸发)溶液红色加深 | CH3COONa水解是一个放热过程 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
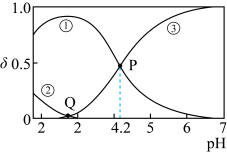
【推荐2】20℃时,在c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol·L-1的H2C2O4、NaOH混合溶液中,含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。下列说法正确的是( )

| A.0.100 mol·L-1NaHC2O4溶液中:c(OH-)=c(H+)-2c(C2O42-)+c(H2C2O4) |
| B.Q点:c(H2C2O4)+c(C2O42-)>c(HC2O4-) |
| C.P点:c(Na+)+c(H2C2O4)<0.100mol·L-1+c(C2O42-) |
| D.该温度下H2C2O4的电离常数Ka2=1×10-4.2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下向10mL 0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的
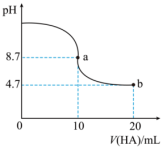

A.a点所示溶液中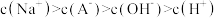 |
B.a、b两点所示溶液中水的电离程度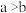 |
C. 时, 时,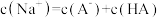 |
D.b点所示溶液中 |
您最近一年使用:0次
【推荐2】用精炼铜漂浮阳极泥(主要成分为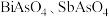 ,含有少量
,含有少量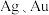 )制备
)制备 的工艺流程如下:
的工艺流程如下:
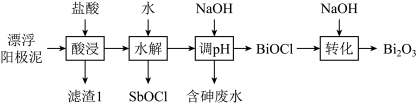
已知:①“转化”分两步进行,其第一步 转化为
转化为 。
。
②常温下, ,
,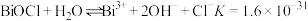 。
。
下列说法错误的是
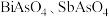 ,含有少量
,含有少量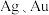 )制备
)制备 的工艺流程如下:
的工艺流程如下:
已知:①“转化”分两步进行,其第一步
 转化为
转化为 。
。②常温下,
 ,
,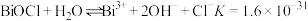 。
。下列说法错误的是
A.“滤渣1”的主要成分是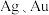 ,含砷废水主要成分是 ,含砷废水主要成分是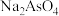 |
B.“水解”分离 和 和 的原理是 的原理是 的水解 的水解 高于 高于 水解的 水解的 |
C.“转化”的总反应方程式为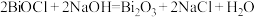 |
D.当 恰好完全转化成 恰好完全转化成 时,溶液 时,溶液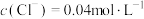 ,此时溶液 ,此时溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】向x mL 0.1 mol•L-1的氨水中滴加等浓度的高氯酸溶液,测得混合溶液的温度和pOH[pOH=-lgc(OH-)]随着加入稀高氯酸的体积变化如图所示(图中实线为温度变化,虚线为pOH变化)。下列说法正确的是
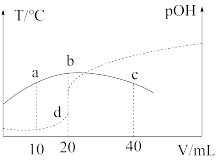

| A.b点溶液:pH>pOH |
| B.b、c两点由水电离出的c(H+):b>c |
C.a点时溶液中微粒浓度存在关系:c(NH3•H2O)+2c(OH-)=2c(H+)+c(NH ) ) |
| D.a、d两点对应的NH3•H2O电离常数:K(d)<K(a) |
您最近一年使用:0次

 )是一种二元弱酸。常温下,用
)是一种二元弱酸。常温下,用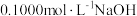 溶液滴定
溶液滴定 溶液(忽略滴定过程中溶液体积变化),得到
溶液(忽略滴定过程中溶液体积变化),得到 和
和 三种粒子的分布分数
三种粒子的分布分数 (平衡时某种含碳微粒浓度占各种含碳微粒浓度之和的分数)随溶液pH变化的曲线如图所示。下列说法正确的是
(平衡时某种含碳微粒浓度占各种含碳微粒浓度之和的分数)随溶液pH变化的曲线如图所示。下列说法正确的是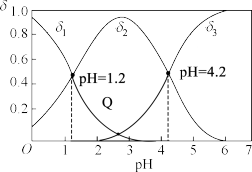
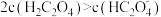
 时,混合溶液中
时,混合溶液中