常温下,下列叙述正确的是
| A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B.pH=8.3的NaHS溶液:c(Na+)>c(HS-)>c(S2-)>c(H2S) |
C.CH3COOH溶液加水稀释后,溶液中 的值减小 的值减小 |
D.等物质的量的NaClO、Na2CO3混合溶液中:c(HClO)+c(ClO-)=c(HCO )+c(H2CO3)+c(CO )+c(H2CO3)+c(CO ) ) |
2021高三·全国·专题练习 查看更多[1]
(已下线)第23讲 盐类水解(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-10-20 14:38:05
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】水合肼(N2H4·H2O)有弱碱性和强还原性,因其产物无污染,故广泛用于金属的回收。 某小组利用N2H4·H2O 处理碱性含铜废液{主要成分为[Cu(NH3)4]Cl2、NH4Cl、氨水}回收铜。已知在相同时间和温度下,溶液 pH 的变化对铜回收率影响如图所示。
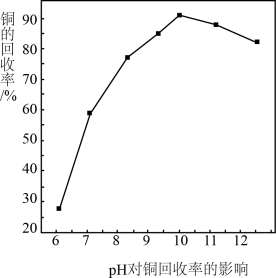
下列说法正确的是

下列说法正确的是
| A.反应的离子方程式为8OH-十N2H4·H2O+4[Cu(NH3)4]2+=2NO↑+4Cu ↓ +16NH3↑十7H2O |
| B.pH>10 时,随着 pH 值的增大铜回收率下降的原因可能是溶液碱性增强,铜废液中生成了 Cu(OH)2沉淀 |
| C.pH=10 时,若制得 2 mol Cu 单质,理论上消耗水合肼的物质的量为 1 mol |
| D.检验回收 Cu 后废液中 Cl-的实验操作:取少量样品, 滴加AgNO3观察是否有白色沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用含硫酸锰(MnSO4)的废锰矿渣制备碳酸锰的某种工艺如图所示。下列说法错误的是

①溶解时采取40~50℃,是为了加快废锰矿渣的溶解
②抽滤属于加压过滤,比常压过滤压强更大
③抽滤与常压过滤相比速度更快,固体和液体分离更彻底
④沉锰的离子方程式为:Mn2++2HCO =MnCO3↓+CO2↑+H2O
=MnCO3↓+CO2↑+H2O
⑤采用高温烘干,可得到纯净干燥的产品

①溶解时采取40~50℃,是为了加快废锰矿渣的溶解
②抽滤属于加压过滤,比常压过滤压强更大
③抽滤与常压过滤相比速度更快,固体和液体分离更彻底
④沉锰的离子方程式为:Mn2++2HCO
 =MnCO3↓+CO2↑+H2O
=MnCO3↓+CO2↑+H2O⑤采用高温烘干,可得到纯净干燥的产品
| A.②④ | B.①③⑤ | C.②⑤ | D.②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下,向冰醋酸中加水进行稀释,稀释过程中溶液的导电能力随加水量(即加入水的体积)变化如图所示(不考虑稀释过程中的温度变化)。下列说法正确的是


| A.醋酸的电离度在原点时为零,b点时最大 |
| B.在溶液处于b点时,加入适量稀硫酸,醋酸的电离度增大 |
| C.稀释过程溶液中c(CH3COO-)的关系:b>a>c |
| D.稀释过程中醋酸的电离平衡常数逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
①0.1mol·L-1 氨水中,c(OH-)=c(NH 4+)
②10mL 0.02mol·L-1 HCl 溶液与 10mL0.02mol·L-1Ba(OH)2 溶液充分混合,若混合后溶液的体积为 20mL,则溶液的 pH=12
③在 0.1mol·L-1 CH COONa 溶液中,c(OH-)=c(CH COOH)+c(H+)
④0.1mol·L-1 某二元弱酸酸式盐 NaHA 溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H A)
①0.1mol·L-1 氨水中,c(OH-)=c(NH 4+)
②10mL 0.02mol·L-1 HCl 溶液与 10mL0.02mol·L-1Ba(OH)2 溶液充分混合,若混合后溶液的体积为 20mL,则溶液的 pH=12
③在 0.1mol·L-1 CH COONa 溶液中,c(OH-)=c(CH COOH)+c(H+)
④0.1mol·L-1 某二元弱酸酸式盐 NaHA 溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H A)
| A.①② | B.②③ | C.③④ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙醇胺为一元弱碱(25℃时,电离常数 ),其电离方程式为
),其电离方程式为 。用
。用 的盐酸滴定20 mL
的盐酸滴定20 mL  乙醇胺溶液,温度恒定在25℃时,滴定过程中由水电离出的
乙醇胺溶液,温度恒定在25℃时,滴定过程中由水电离出的 与滴加盐酸体积的关系如图所示(已知:
与滴加盐酸体积的关系如图所示(已知: )。下列说法中错误的是
)。下列说法中错误的是

 ),其电离方程式为
),其电离方程式为 。用
。用 的盐酸滴定20 mL
的盐酸滴定20 mL  乙醇胺溶液,温度恒定在25℃时,滴定过程中由水电离出的
乙醇胺溶液,温度恒定在25℃时,滴定过程中由水电离出的 与滴加盐酸体积的关系如图所示(已知:
与滴加盐酸体积的关系如图所示(已知: )。下列说法中错误的是
)。下列说法中错误的是
A.a点溶液中: |
B.b点溶液中: |
C.c点两侧溶液均存在由水电离出的 |
D.d点溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】25℃时,分别向25mL浓度均为1.0mol·L-1的HA、NaA溶液中逐滴加入浓度均为1.0mol·L-1的NaOH、HCl溶液VmL。溶液的pH与lgY[Y=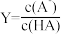 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
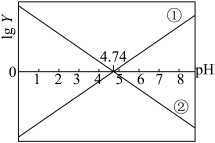
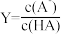 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
A.曲线①中的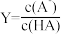 |
| B.当pH=4.74时,一定存在c(H+)+c(Na+)=c(OH-)+c(A-) |
| C.当滴入体积V=12.5mL时,溶液pH>4.74 |
| D.25℃时,1.0mol·L-1的NaA溶液的pH=9.37 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知: Ag+ +NH3 [Ag(NH3)]+ K1=103.32
[Ag(NH3)]+ K1=103.32
[Ag(NH3)]++NH3 [Ag(NH3)2]+ K2
[Ag(NH3)2]+ K2
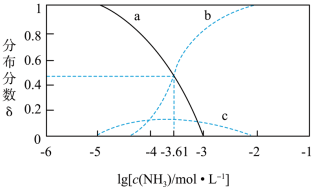
Ag+、[Ag(NH3)]+、 [Ag(NH3)2]+ 的分布分数δ与lgc(NH3 )关系如下图所示,下列说法正确的是{例如:分布分数δ(Ag+)= }
}
 [Ag(NH3)]+ K1=103.32
[Ag(NH3)]+ K1=103.32[Ag(NH3)]++NH3
 [Ag(NH3)2]+ K2
[Ag(NH3)2]+ K2Ag+、[Ag(NH3)]+、 [Ag(NH3)2]+ 的分布分数δ与lgc(NH3 )关系如下图所示,下列说法正确的是{例如:分布分数δ(Ag+)=
 }
}
| A.曲线c代表[Ag(NH3)2]+ |
| B.K2=10-3.61 |
C.[Ag(NH3)2]+ Ag++ 2NH3平衡常数K' =10-7.22 Ag++ 2NH3平衡常数K' =10-7.22 |
| D.当c(NH3 )<0.01 mol/L时,c [Ag(NH3)2]+> c [Ag(NH3)]+>c(Ag+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向一定浓度的亚磷酸( )溶液中滴加NaOH溶液,测得溶液的pH 与溶液中离子浓度变化的关系如图所示,下列说法错误的是
)溶液中滴加NaOH溶液,测得溶液的pH 与溶液中离子浓度变化的关系如图所示,下列说法错误的是

A.表示溶液pH与 变化的关系是曲线I 变化的关系是曲线I |
| B.NaH2PO3溶液显酸性 |
C.0.1mol·L-1 Na2HPO3溶液中,各离子浓度大小关系为:c(Na+)>c( )>c( )>c(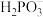 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
D.若HF的电离常数Ka=3.6×10-4,则足量NaF溶液和H3PO3溶液反应的离子方程式为:F- + H3PO3 = HF +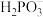 |
您最近一年使用:0次

 的比值减小
的比值减小 的
的 、
、 混合溶液中:
混合溶液中: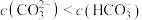 ,且
,且
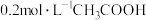 溶液与
溶液与 溶液等体积混合后:
溶液等体积混合后:
 、②
、② :①<②<③[已知:
:①<②<③[已知: ]
]

