当今,世界各国相继规划了碳达峰、碳中和的时间节点。因此,研发CO2利用技术、降低CO2含量成为研究热点。某化学实验小组采用CO2催化加氢制甲醇来减少CO2对环境造成的影响。在容积为4L的恒容密闭容器中,充入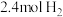 和
和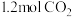 ,发生反应:
,发生反应: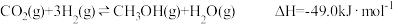 。回答下列问题:
。回答下列问题:
(1)每消耗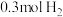 ,该反应放出的热量为
,该反应放出的热量为___________ kJ。
(2)下列能用来判断该反应达到平衡状态的标志是___________(填标号)。
(3)3min后,反应达到平衡状态,此时测得反应前后的总压强之比为5∶4。
①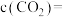
___________ mol/L, 的转化率为
的转化率为___________ %。
②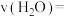
___________  。
。
③该反应达到平衡时的平衡常数K=___________ (列出计算式即可)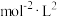 。
。
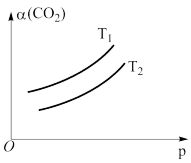
(4)在一定条件下,体系中的CO2的平衡转化率( )与温度(T)和压强(p)的关系如图所示。则T1
)与温度(T)和压强(p)的关系如图所示。则T1___________ (填“>”或“<”)T2,判断的理由是___________ 。
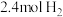 和
和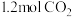 ,发生反应:
,发生反应: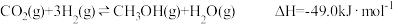 。回答下列问题:
。回答下列问题:(1)每消耗
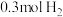 ,该反应放出的热量为
,该反应放出的热量为(2)下列能用来判断该反应达到平衡状态的标志是___________(填标号)。
| A.混合气体的密度不再随时间改变 | B.混合气体的平均相对分子质量不再随时间改变 |
C.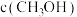 不再随时间改变 不再随时间改变 | D.混合气体的质量不再随时间改变 |
①
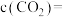
 的转化率为
的转化率为②
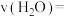
 。
。③该反应达到平衡时的平衡常数K=
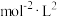 。
。(4)在一定条件下,体系中的CO2的平衡转化率(
 )与温度(T)和压强(p)的关系如图所示。则T1
)与温度(T)和压强(p)的关系如图所示。则T1
更新时间:2021/11/21 20:55:11
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)已知丙烷完全燃烧生成CO2和1 mol H2O(l)放出553.75kJ的热量,写出表示丙烷燃烧热的热化学方程式:_______ 。
(2)在25℃、101kPa下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_______ 。
(3)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是_______ 。
(4)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。已知:E(H—H)=436kJ•mol-1,E(Cl—Cl)=243kJ•mol-1,E(H—Cl)=432kJ•mol-1。则H2(g)+Cl2(g) =2HCl(g) ΔH=_______ 。
(5)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化的示意图,请计算每生成1molNH3(g)放出热量为_______ 。

(1)已知丙烷完全燃烧生成CO2和1 mol H2O(l)放出553.75kJ的热量,写出表示丙烷燃烧热的热化学方程式:
(2)在25℃、101kPa下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为
(3)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是
(4)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。已知:E(H—H)=436kJ•mol-1,E(Cl—Cl)=243kJ•mol-1,E(H—Cl)=432kJ•mol-1。则H2(g)+Cl2(g) =2HCl(g) ΔH=
(5)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化的示意图,请计算每生成1molNH3(g)放出热量为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
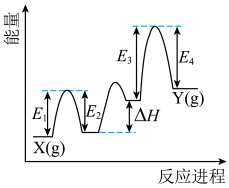
【推荐2】Cr2O3催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的焓变为___________ (列式表示)。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在一固定容积的密闭容器中,进行如下反应:C(s)+H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。
(1)若容器体积为2 L,反应10秒后氢气的质量增加0.4 g,则该时间内一氧化碳的反应速率为___ mol/(L•s)。
(2)该反应达到平衡状态的标志是___ (选填编号)。
A.压强不变 B.v正(H2)=v正(H2O)
C.c(CO)不变 D.c(H2O)=c(CO)
(3)若增加炭的量,则正反应速率___ (选填“增大”、“减小”、不变);若增大压强,化学平衡向___ 移动(选填“正向”、“逆向”或“不”)。
(4)若升高温度,平衡向正向移动,则正反应方向为___ 反应。(填“吸热”或“放热”)
 CO(g)+H2(g)。
CO(g)+H2(g)。(1)若容器体积为2 L,反应10秒后氢气的质量增加0.4 g,则该时间内一氧化碳的反应速率为
(2)该反应达到平衡状态的标志是
A.压强不变 B.v正(H2)=v正(H2O)
C.c(CO)不变 D.c(H2O)=c(CO)
(3)若增加炭的量,则正反应速率
(4)若升高温度,平衡向正向移动,则正反应方向为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】994 K,当H2缓慢通过过量的块状固体CoO时,部分CoO被还原为固体Co。在流出的平衡气体中H2的物质的量分数为2.50%; 在同一温度,若用CO还原固体CoO时平衡气体中CO的物质的量分数为1.92%。 如果994 K时物质的量比为1:2的一氧化碳和水蒸气的混合物在一定条件下反应,问:
(1)一氧化碳的平衡转化率大约是多少___________ ?
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施___________ 。
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化___________ ?为什么___________ ?
(1)一氧化碳的平衡转化率大约是多少
(2)欲获得较纯的H2,请简要说明在生产工艺上应采取的措施
(3)994 K,当H2缓慢通过过量的纳米CoO固体粉末时,部分CoO被还原为固体Co。在相同的反应时间内,与块状固体CoO相比,采用纳米固体CoO时流出的平衡气体中H2的物质的量分数将怎样变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氨催化氧化是硝酸工业的基础,氨气在Pt催化剂作用下发生主反应I和副反应II:
I.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ∆H1=-905 kJ/mol
II.4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ∆H2=-1265KJ/mol
(1)2NO(g)⇌N2(g) + O2(g) ∆H3=____ 。
(2)以Pt为催化剂,在1L密闭容器中充入1mol NH3和2mol O2, 测得有关物质的量与温度的关系如图:
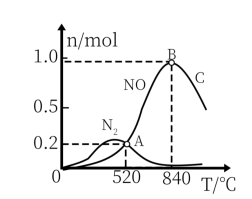
①该催化剂在高温时对反应___ 更有利(填“I”或“II”)。
②520℃时,NH3的转化率为___ 。(提示:多平衡问题一定以多平衡后最终结果计算)
③520℃时,反应II的平衡常数K=___ (写出平衡常数数字表达式,不用计算结果)。
④下列说法正确的是__ (填标号)。
A.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
B.增大NH3与O2的初始投料比,可以提高NH3生成NO的平衡转化率
C.投料比不变,增加反应物的浓度,可以提高NH3生成NO的平衡转化率
D.使用催化剂时,可降低反应的活化能,加快其反应速率
⑤温度高于840℃时,NO的物质的量减少的原因可能是___ (回答任意一条)
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1mol N2时,转移的电子数用分数表示为___ mol。
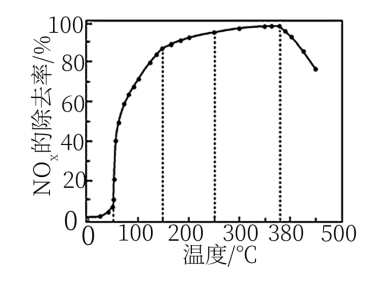
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂的反应器中反应。反应相同时间NOx的去除率随反应温度的变化曲线如下图所示,在50-250℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢,先迅速上升的主要原因是___ 。
I.4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ∆H1=-905 kJ/mol
II.4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ∆H2=-1265KJ/mol
(1)2NO(g)⇌N2(g) + O2(g) ∆H3=
(2)以Pt为催化剂,在1L密闭容器中充入1mol NH3和2mol O2, 测得有关物质的量与温度的关系如图:

①该催化剂在高温时对反应
②520℃时,NH3的转化率为
③520℃时,反应II的平衡常数K=
④下列说法正确的是
A.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
B.增大NH3与O2的初始投料比,可以提高NH3生成NO的平衡转化率
C.投料比不变,增加反应物的浓度,可以提高NH3生成NO的平衡转化率
D.使用催化剂时,可降低反应的活化能,加快其反应速率
⑤温度高于840℃时,NO的物质的量减少的原因可能是
(3)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1mol N2时,转移的电子数用分数表示为
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂的反应器中反应。反应相同时间NOx的去除率随反应温度的变化曲线如下图所示,在50-250℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢,先迅速上升的主要原因是

您最近一年使用:0次
【推荐1】氨气是重要的化工原料,工业上合成氨的反应: 。回答下列问题:
。回答下列问题:
(1)已知键能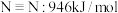 ,
,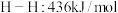 ,
,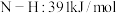 。工业上合成氨反应的
。工业上合成氨反应的
___________ 。
(2)工业合成氨在合成塔中进行,下列事实能说明反应已达化学平衡状态的有___________ (填字母标号)。
a.密闭的合成塔中气体密度不再变化 b.合成塔中混合气体的平均摩尔质量不再变化
c.氮气的百分含量保持不变 d.氮气、氢气、氨气物质的量之比为
(3)氨是一种极易溶于水的气体。氨气极易溶于水的主要原因是___________ 。
(4)将稀氨水逐滴滴加到 溶液中,出现蓝色沉淀,滴加一定量氨水后蓝色沉淀溶解,得深蓝色溶液,沉淀溶解的化学方程式为
溶液中,出现蓝色沉淀,滴加一定量氨水后蓝色沉淀溶解,得深蓝色溶液,沉淀溶解的化学方程式为___________ ;向深蓝色溶液中加入无水乙醇有深蓝色晶体析出,该晶体中阴离子的空间结构为___________ 。
(5)稀氨水也能用于配制银氨溶液。
①下列有关银氨溶液的相关描述正确的有___________ (填字母标号)。
a.向盛有1mL 2% 溶液的试管中,边振荡边逐滴滴入2%氨水,使最初产生的沉淀恰好溶解,制得银氨溶液
溶液的试管中,边振荡边逐滴滴入2%氨水,使最初产生的沉淀恰好溶解,制得银氨溶液
b. 是配位化合物,配位原子是N,中心离子的配位数是2
是配位化合物,配位原子是N,中心离子的配位数是2
c.将几滴银氨溶液滴入2mL乙醛中,用酒精灯的外焰给试管底部加热可产生银镜
d.能发生银镜反应的物质一定属醛类物质
②若用0.05mol乙醛与足量的银氨溶液发生银镜反应,理论上可生成银___________ g。
 。回答下列问题:
。回答下列问题:(1)已知键能
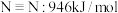 ,
,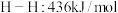 ,
,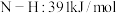 。工业上合成氨反应的
。工业上合成氨反应的
(2)工业合成氨在合成塔中进行,下列事实能说明反应已达化学平衡状态的有
a.密闭的合成塔中气体密度不再变化 b.合成塔中混合气体的平均摩尔质量不再变化
c.氮气的百分含量保持不变 d.氮气、氢气、氨气物质的量之比为

(3)氨是一种极易溶于水的气体。氨气极易溶于水的主要原因是
(4)将稀氨水逐滴滴加到
 溶液中,出现蓝色沉淀,滴加一定量氨水后蓝色沉淀溶解,得深蓝色溶液,沉淀溶解的化学方程式为
溶液中,出现蓝色沉淀,滴加一定量氨水后蓝色沉淀溶解,得深蓝色溶液,沉淀溶解的化学方程式为(5)稀氨水也能用于配制银氨溶液。
①下列有关银氨溶液的相关描述正确的有
a.向盛有1mL 2%
 溶液的试管中,边振荡边逐滴滴入2%氨水,使最初产生的沉淀恰好溶解,制得银氨溶液
溶液的试管中,边振荡边逐滴滴入2%氨水,使最初产生的沉淀恰好溶解,制得银氨溶液b.
 是配位化合物,配位原子是N,中心离子的配位数是2
是配位化合物,配位原子是N,中心离子的配位数是2c.将几滴银氨溶液滴入2mL乙醛中,用酒精灯的外焰给试管底部加热可产生银镜
d.能发生银镜反应的物质一定属醛类物质
②若用0.05mol乙醛与足量的银氨溶液发生银镜反应,理论上可生成银
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】恒温下在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

(1)该反应的化学方程式为_____ 。
(2)从开始至5min,Y的平均反应速率为_____ ;X的转化率为_____ 。
(3)反应达平衡时体系的压强是开始时的_____ 倍。
(4)下列描述中能表明反应已达到平衡状态的是_____ 。(填序号)
①混合气体的压强不变
②混合气体的密度不变
③Z(g)的物质的量浓度不变
④混合气体的平均相对分子质量不变
⑤单位时间内生成2n mol Z,同时生成3n mol X
⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻v(X)=3v(Y)且不等于零
(5)在某一时刻采取下列措施能加快反应速率的是 。

(1)该反应的化学方程式为
(2)从开始至5min,Y的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列描述中能表明反应已达到平衡状态的是
①混合气体的压强不变
②混合气体的密度不变
③Z(g)的物质的量浓度不变
④混合气体的平均相对分子质量不变
⑤单位时间内生成2n mol Z,同时生成3n mol X
⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻v(X)=3v(Y)且不等于零
(5)在某一时刻采取下列措施能加快反应速率的是 。
| A.加催化剂 | B.降低温度 |
| C.体积不变,充入X | D.体积不变,从容器中分离出Y |
您最近一年使用:0次
【推荐3】我国力争于2030年前实现“碳达峰”,2060年前实现“碳中和”。世界各地科学家寻求将CO2转化为甲烷,实现资源的循环利用。二氧化碳甲烷化的反应为: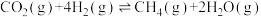 结合相关信息,回答下列问题:
结合相关信息,回答下列问题:
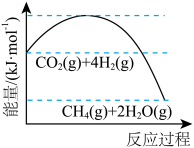
(1)下图表示该反应过程中能量变化,在恒容绝热的容器中,该反应进行一段时间后,容器内的温度___________ (填“升高”或“降低”)。
①5min内该反应的平均反应速率v(CO2)=___________ 。
②平衡时,H2的转化率为___________ 。
③下列情况可以说明该反应达到平衡状态的是___________ (填字母)。
a.生成1mol CH4的同时消耗1molCO2 b.CO2的体积分数不再变化
c.容器内气体的压强不再变化 d.容器内气体的密度不再变化
④其它条件相同时,只改变一个条件,能增大CH4的生成速率的是___________ (填字母)。
a.降低温度 b.充入CO2 c.充入He
(3)燃料电池的能量转化率可以超过80%,还具有清洁、安全等特点,某新型甲烷燃料电池的工作原理如图所示,放电时,氧化产物为K2CO3。___________ 。
②电池放电转移16mol电子时,至少消耗燃料甲烷___________ g。
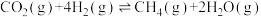 结合相关信息,回答下列问题:
结合相关信息,回答下列问题:(1)下图表示该反应过程中能量变化,在恒容绝热的容器中,该反应进行一段时间后,容器内的温度
| 时间/min | 5 | 10 | 13 |
| n(CO2)/mol | 0.35 | 0.30 | 0.30 |
②平衡时,H2的转化率为
③下列情况可以说明该反应达到平衡状态的是
a.生成1mol CH4的同时消耗1molCO2 b.CO2的体积分数不再变化
c.容器内气体的压强不再变化 d.容器内气体的密度不再变化
④其它条件相同时,只改变一个条件,能增大CH4的生成速率的是
a.降低温度 b.充入CO2 c.充入He
(3)燃料电池的能量转化率可以超过80%,还具有清洁、安全等特点,某新型甲烷燃料电池的工作原理如图所示,放电时,氧化产物为K2CO3。
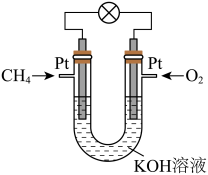
②电池放电转移16mol电子时,至少消耗燃料甲烷
您最近一年使用:0次
【推荐1】高炉炼铁中发生的基本反应如下:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0。
Fe(s)+CO2(g) △H>0。
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是___________ 。
a.高炉内压强不变
b.CO2的生成速率和CO的生成速率相等
c.混合气体中CO2的浓度不变
d.c(CO2)=c(CO)
(2)此反应的平衡常数表达式为K=___________ 。
(3)温度升高平衡常数K值__________ (填“增大”“减小”、或“不变”)。
(4)已知1100℃时,K=0.263,此时测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态____________ (填“是”或“否”),此时化学反应速率是
___________  (填“<”、“>”或“=”),其原因是
(填“<”、“>”或“=”),其原因是___________ 。
 Fe(s)+CO2(g) △H>0。
Fe(s)+CO2(g) △H>0。(1)下列可以作为判断该反应已经达到化学平衡状态依据的是
a.高炉内压强不变
b.CO2的生成速率和CO的生成速率相等
c.混合气体中CO2的浓度不变
d.c(CO2)=c(CO)
(2)此反应的平衡常数表达式为K=
(3)温度升高平衡常数K值
(4)已知1100℃时,K=0.263,此时测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态

 (填“<”、“>”或“=”),其原因是
(填“<”、“>”或“=”),其原因是
您最近一年使用:0次
【推荐2】合成氨工业对国民经济和社会发展具有重要的意义。
其原理为:
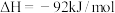 ;据此回答以下问题:
;据此回答以下问题:
实验室中模拟合成氨反应,在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
(1)实验1中,50 min时向容器中充入一定量He,则正反应速率____ (域“增大”、“减小”或“不变”)
(2)实验2中,前20min内以 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为_____ 。
(3)比较实验1和2,说明实验2隐含的条件是______ 。
(4)上述三组实验的化学平衡常数分别为 、
、 、
、 ,三者大小关系是
,三者大小关系是______ 。
(5)某温度下,若把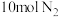 ,与
,与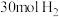 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
_______ 。(用百分数表示)。能说明该反应达到化学平衡状态的是_____ (填字母)。
a.容器内压强保持不变。
b.容器内的密度保持不变
c.混合气体中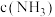 不变
不变
d.
(6)对于合成氨反应而言,下列有关图象一定正确的是_____ (选填序号)。
A、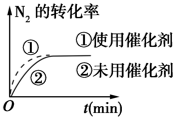 B、
B、 C、
C、 
其原理为:

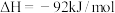 ;据此回答以下问题:
;据此回答以下问题:实验室中模拟合成氨反应,在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
| 实验序号 | 温度(℃) |  浓度(mol/L) 浓度(mol/L) | ||||||
| 0 min | 10 min | 20 min | 30 min | 40min | 50min | 60 min | ||
| 1 | 300 | 2.00 | 1.70 | 1.50 | L36 | 1.25 | 1.20 | 1.20 |
| 2 | 300 | 2.00 | 1.50 | 1.28 | 1.20 | 1.20 | 1.20 | 1.20 |
| 3 | 200 | 2.00 | 1.60 | 1.39 | 1.29 | 1.27 | 1.27 | 1.27 |
(1)实验1中,50 min时向容器中充入一定量He,则正反应速率
(2)实验2中,前20min内以
 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为(3)比较实验1和2,说明实验2隐含的条件是
(4)上述三组实验的化学平衡常数分别为
 、
、 、
、 ,三者大小关系是
,三者大小关系是(5)某温度下,若把
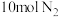 ,与
,与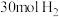 置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
置于体积为10 L的密闭容器内,反应达到平衡状态时,测得混合气体的压强弯为开始时的0.8,则平衡时氢气的转化率
a.容器内压强保持不变。
b.容器内的密度保持不变
c.混合气体中
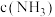 不变
不变d.

(6)对于合成氨反应而言,下列有关图象一定正确的是
A、
 B、
B、 C、
C、 
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】马来酸二丁酯(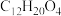 )是粘接剂行业的一种优良增塑剂,也在很多有机合成中用作添加剂和中间体。研究者用离子交换树脂AmberliteIR-120作为催化剂,催化顺丁烯二酸酐(
)是粘接剂行业的一种优良增塑剂,也在很多有机合成中用作添加剂和中间体。研究者用离子交换树脂AmberliteIR-120作为催化剂,催化顺丁烯二酸酐(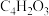 ,记为A)与正丁醇(
,记为A)与正丁醇(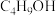 ,记为B)的酯化反应来合成马来酸二丁酯。实验获得如下动力学数据:
,记为B)的酯化反应来合成马来酸二丁酯。实验获得如下动力学数据:
已知速率方程式为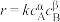 。
。
(1)试导出 、
、 的值。
的值。 =
=________ , =
=________ ,
(2)计算反应的速率常数k及反应的活化能 。k=
。k=________ ,
________ ,
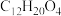 )是粘接剂行业的一种优良增塑剂,也在很多有机合成中用作添加剂和中间体。研究者用离子交换树脂AmberliteIR-120作为催化剂,催化顺丁烯二酸酐(
)是粘接剂行业的一种优良增塑剂,也在很多有机合成中用作添加剂和中间体。研究者用离子交换树脂AmberliteIR-120作为催化剂,催化顺丁烯二酸酐(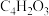 ,记为A)与正丁醇(
,记为A)与正丁醇(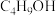 ,记为B)的酯化反应来合成马来酸二丁酯。实验获得如下动力学数据:
,记为B)的酯化反应来合成马来酸二丁酯。实验获得如下动力学数据:| 序号 | 反应温度/℃ |  |  | 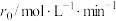 |
| 1 | 115 | 0.303 | 0.606 | 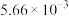 |
| 2 | 115 | 0.454 | 0.606 | 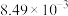 |
| 3 | 115 | 0.303 | 0.910 | 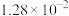 |
| 4 | 110 | 0.454 | 0.606 | 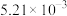 |
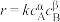 。
。(1)试导出
 、
、 的值。
的值。 =
= =
=(2)计算反应的速率常数k及反应的活化能
 。k=
。k=
您最近一年使用:0次

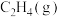 与适量
与适量 反应,生成
反应,生成 和
和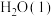 ,放出1411kJ的热量
,放出1411kJ的热量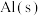 与适量
与适量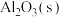 ,放出834.9kJ的热量
,放出834.9kJ的热量

