在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知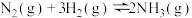
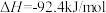 ;)
;)
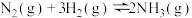
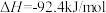 ;)
;)容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol | 2mol | 4mol |
平衡时 |
|
|
|
反应的能量变化 | 放出aKJ | 吸收bKJ | 吸收cKJ |
平衡压强 |
|
|
|
反应物转化率 |
|
|
|
A.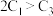 | B. | C.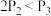 | D.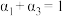 |
更新时间:2021-12-10 21:38:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】现将 2 mol 气体A 与 1 mol 气体B 充入一个体积不变的容器内,发生反应:2A+B ⇌ C+3D+4E,达到平衡后气体A 的浓度减少一半,发现有液体生成,在相同的温度下测得反应 前后压强分别为 6.06×106 Pa 和 8.08×106 Pa,又测得反应共放出热量 Q kJ,下列说法正确的是
| A.该反应在任何温度下都可自发进行 |
| B.在上述平衡体系中再加入 1 mol A 和 0.5 mol B,平衡正向移动,A 的转化率增大 |
| C.该反应的热化学方程式为 2A(g)+B(g) ⇌ C(g)+3D(l)+4E(g) ΔH= -Q kJ/mol |
| D.上述反应达到平衡后,其他的条件不变的情况下,升高温度,压强一定增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】反应N2O4(g)  2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g);△H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.a、c两点的反应速率:a>c |
| B.b、c两点气体的颜色:一样深 |
| C.b、c两点的转化率:b>c |
| D.由b点到a点,可以用加热的方法 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】密闭容器进行如下反应: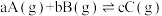 △H,A、C的质量分数(ω)、压强(p)、温度(T)和时间(t)的关系如图甲(恒温)和图乙(恒压)所示。下列说法正确的是
△H,A、C的质量分数(ω)、压强(p)、温度(T)和时间(t)的关系如图甲(恒温)和图乙(恒压)所示。下列说法正确的是
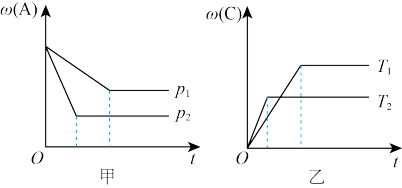
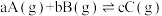 △H,A、C的质量分数(ω)、压强(p)、温度(T)和时间(t)的关系如图甲(恒温)和图乙(恒压)所示。下列说法正确的是
△H,A、C的质量分数(ω)、压强(p)、温度(T)和时间(t)的关系如图甲(恒温)和图乙(恒压)所示。下列说法正确的是
A. , , |
B.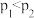 , ,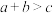 |
C.平衡常数K: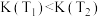 , ,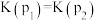 |
D.若只改变压强 ,B的转化率减小 ,B的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】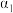 和
和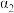 、
、 和
和 分别为两个恒容容器中平衡体系
分别为两个恒容容器中平衡体系 和
和 的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量。下列判断正确的是( )
的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量。下列判断正确的是( )
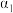 和
和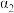 、
、 和
和 分别为两个恒容容器中平衡体系
分别为两个恒容容器中平衡体系 和
和 的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量。下列判断正确的是( )
的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量。下列判断正确的是( )A.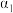 减小、 减小、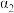 增大, 增大, 、 、 均增大 均增大 |
B.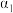 、 、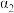 均增大, 均增大, 、 、 均增大 均增大 |
C.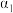 增大、 增大、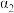 减小, 减小, 、 、 均增大 均增大 |
D.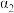 减小、 减小、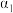 增大, 增大, 增大、 增大、 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知常温下,N2(气)和H2(气)生成2mol NH3(气)放出92.4 kJ热量。现有甲、乙两个容积相同的密闭容器,在常温下:①向密闭容器甲中通入1 molN2和3 mol H2,达到平衡时放出热量Q1kJ。②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2kJ。则下列关系式正确的是
| A.Q1=2Q2=92.4 | B.Ql>2Q2 | C.Q1<2Q2 | D.Q1=2Q2≠92.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:

下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
| A.v1< v2,c2< 2c1 | B.K1> K3,p2> 2p3 |
| C.v1< v3,α1(SO2 ) >α3(SO2 ) | D.c2> 2c3,α2(SO3 )+α3(SO2 )=1 |
您最近一年使用:0次
【推荐3】700℃时, H2(g) + CO2(g) H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时, (H2O)为 0.025 mol·L-1·min-1,下列判断错误的是
(H2O)为 0.025 mol·L-1·min-1,下列判断错误的是
 H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时, (H2O)为 0.025 mol·L-1·min-1,下列判断错误的是
(H2O)为 0.025 mol·L-1·min-1,下列判断错误的是| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)mol·L-1 | 0.10 | 0.20 | 0.20 |
| c(CO2)mol·L-1 | 0.10 | 0.10 | 0.20 |
| A.平衡时,甲中CO2的转化率等于50% |
| B.当反应平衡时,丙中c(CO2)是甲中的2倍 |
C.温度升至800℃,上述反应平衡常数为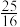 ,则正反应为吸热反应 ,则正反应为吸热反应 |
| D.其他条件不变,若起始时向容器乙中充入0.10 mol·L-1 H2 和0.20 mol·L-1CO2,到达平衡时c (CO)与乙不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:
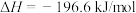 。现在一容积为2L的密闭容器中充入2molSO2、1molO2,加入固体催化剂,保持温度在450℃使之发生反应,5min时测得体系的压强减小了30%。下列说法正确的是
。现在一容积为2L的密闭容器中充入2molSO2、1molO2,加入固体催化剂,保持温度在450℃使之发生反应,5min时测得体系的压强减小了30%。下列说法正确的是

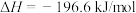 。现在一容积为2L的密闭容器中充入2molSO2、1molO2,加入固体催化剂,保持温度在450℃使之发生反应,5min时测得体系的压强减小了30%。下列说法正确的是
。现在一容积为2L的密闭容器中充入2molSO2、1molO2,加入固体催化剂,保持温度在450℃使之发生反应,5min时测得体系的压强减小了30%。下列说法正确的是| A.5min时SO2的转化率为30% |
| B.5min时反应共放出了137.62kJ的热量 |
C.用O2表示的5min内的平均反应速率为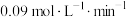 |
| D.若将反应起始温度提高到500℃,反应达到此状态的时间小于5min,其本质原因是反应体系中活化分子的数量和百分数均增加,增加了有效碰撞几率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应 的
的 ,在恒容密闭容器中反应达到平衡时,下列说法正确的是
,在恒容密闭容器中反应达到平衡时,下列说法正确的是
 的
的 ,在恒容密闭容器中反应达到平衡时,下列说法正确的是
,在恒容密闭容器中反应达到平衡时,下列说法正确的是A. 的正反应速率是 的正反应速率是 的逆反应速率的3倍 的逆反应速率的3倍 |
| B.通入稀有气体使压强增大,平衡将向正反应方移动 |
| C.降低温度,混合气体的平均相对分子质量变大 |
D.若平衡时 、 、 的转化率相等,说明反应开始时 的转化率相等,说明反应开始时 的物质的量是 的物质的量是 的物质的量的3倍 的物质的量的3倍 |
您最近一年使用:0次

 和3mol
和3mol



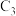






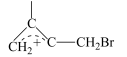 互相转化,反应历程及能量变化如图所示:
互相转化,反应历程及能量变化如图所示: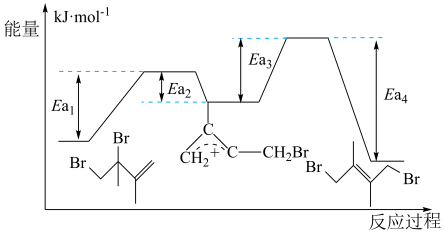
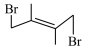 比
比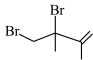 稳定,因此任意条件下主产物均为
稳定,因此任意条件下主产物均为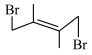
 小于
小于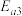 可知,升温有利于
可知,升温有利于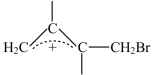

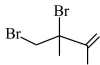
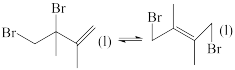
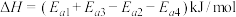
 CH3COOH(l)
CH3COOH(l)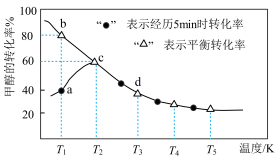

 在低温时分两步完成:
在低温时分两步完成: (慢反应)、
(慢反应)、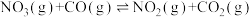 (快反应),依据该过程,下列说法错误的是:
(快反应),依据该过程,下列说法错误的是:

