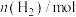一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气进行回收。涉及的反应为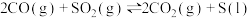
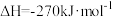 ,
,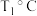 时,在容积为1 L且体积不变的密闭容器中,1 mol CO和0.5 mol SO2,达到平衡时时,测得CO2的浓度为0.5 mol/L。下列说法错误的是
时,在容积为1 L且体积不变的密闭容器中,1 mol CO和0.5 mol SO2,达到平衡时时,测得CO2的浓度为0.5 mol/L。下列说法错误的是
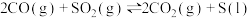
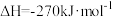 ,
,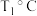 时,在容积为1 L且体积不变的密闭容器中,1 mol CO和0.5 mol SO2,达到平衡时时,测得CO2的浓度为0.5 mol/L。下列说法错误的是
时,在容积为1 L且体积不变的密闭容器中,1 mol CO和0.5 mol SO2,达到平衡时时,测得CO2的浓度为0.5 mol/L。下列说法错误的是| A.该温度下的K=4 |
| B.温度不变,在1 L密闭容器中加入1 mol CO2和0.3 mol S,平衡时CO2的浓度为0.5 mol/L |
| C.温度不变,在1 L密闭容器中加入1 mol CO,0.5 mol SO2,1 mol CO2和0.5 mol S。此时v正>v逆 |
| D.该过程中放出的热量135 kJ |
更新时间:2021-11-08 21:01:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】400℃时,向容积为2L的密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据见下表:
。反应过程中测得的部分数据见下表:
下列说法中,正确的是
 ,发生如下反应:
,发生如下反应: 。反应过程中测得的部分数据见下表:
。反应过程中测得的部分数据见下表:
| 0 | 10 | 20 | 30 |
| 0.10 | 0.04 | 0.02 | |
| 0.20 | 0.04 |
A.反应在前10min内的平均速率为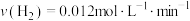 |
B.保持其他条件不变,再向平衡体系中同时通入物质的量均为0.08mol的CO、 和 和 ,则达到新平衡前 ,则达到新平衡前 |
C.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
D.保持其他条件不变,起始时向容器中充入0.05molCO和 ,达到平衡时, ,达到平衡时,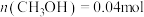 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)⇌pC(g)+qD(g)(m、n、p、q为任意整数)。下列不能作为达到平衡状态的标志的是
| A.单位时间内有m mol A消耗,同时有p mol C生成 |
| B.体系的温度不再改变 |
| C.各组分的浓度不再改变 |
| D.各组分的质量分数不再改变 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列解释实验事实的方程式不正确的是
| A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN-⇌ Fe(SCN)3 |
| B.“NO2球”浸泡在冷水中,颜色变浅:2 NO2(g)⇌N2O4 (g) ∆H>0 |
| C.氢氧化铜沉淀中滴加氨水,形成深蓝色溶液: Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- |
D.I2的CCl4溶液中加入浓KI溶液,紫色变浅:I2+I-= I |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用平衡移动原理解释的是
A. 左右比室温更有利于合成 左右比室温更有利于合成 的反应 的反应 |
B.密闭烧瓶内 和 和 的混合气体,受热后颜色加深 的混合气体,受热后颜色加深 |
C.加压有利于 与 与 生成 生成 的反应 的反应 |
| D.浓硫酸的使用有利于乙醇的酯化反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
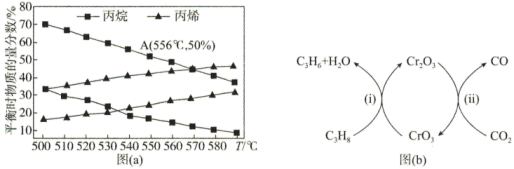
【推荐1】近年来,全球丙烯需求快速增长,研究丙烷制丙烯有着重要的意义。用丙烷直接催化脱氢容易造成积碳,降低催化剂的稳定性,该反应在不同压强(0.1MPa、0.01MPa)下,丙烷和丙烯的物质的量分数随温度变化的关系如图(a)所示;科学家最新研究用 氧化
氧化 脱氢,机理如图(b)所示。下列说法错误的是
脱氢,机理如图(b)所示。下列说法错误的是
 氧化
氧化 脱氢,机理如图(b)所示。下列说法错误的是
脱氢,机理如图(b)所示。下列说法错误的是
| A.丙烷直接催化脱氢的反应条件:高温低压 |
B.A点的平衡常数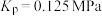 |
C.与直接脱氢相比,用 氧化 氧化 脱氢制丙烯的优点之一是消除积碳 脱氢制丙烯的优点之一是消除积碳 |
D. 直接脱氢与 直接脱氢与 氧化 氧化 脱氢制得等量的丙烯转移电子数相同 脱氢制得等量的丙烯转移电子数相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为探究外界条件对可逆反应A(g)+B(g) C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1molB,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为II、III、IV。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1molB,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为II、III、IV。
针对上述系列实验,下列结论中错误 的是
 C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1molB,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为II、III、IV。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1molB,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为II、III、IV。A | B | C | |
| I | 0.050mol·L-1 | 0.050mol·L-1 | 0.050mol·L-1 |
| II | 0.070mol·L-1 | 0.070mol·L-1 | 0.098mol·L-1 |
| III | 0.060mol·L-1 | 0.060mol·L-1 | 0.040mol·L-1 |
| IV | 0.080mol·L-1 | 0.080mol·L-1 | 0.12mol·L-1 |
| A.由I中数据可计算出该温度下反应的平衡常数K=20 |
| B.II可能是通过增大C的浓度实现的 |
| C.若III只是升高温度,则与I比较,可以判断出正反应一定是放热反应 |
| D.第IV组实验数据的得出,通过压缩容器的体积就可以实现 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】科研工作者利用生物无水乙醇脱水制备乙烯,有关反应在不同温度下的化学平衡常数如表所示,下列说法正确的是
| 温度(K) | 化学平衡常数 | |
I.C2H5OH(g) C2H4(g)+H2O(g) C2H4(g)+H2O(g) | II.2C2H5OH(g) C2H5OC2H5(g)+H2O(g) C2H5OC2H5(g)+H2O(g) | |
| 500 | 3.2 | 0.80 |
| 700 | 7.7 | 0.14 |
| 900 | 12.3 | 0.12 |
| A.升高温度反应I的速率加快,反应II的速率减慢 |
| B.反应I的△H>0 |
| C.由信息可知相同条件下反应I比反应II更易发生 |
D.500K时,C2H5OC2H5(g) 2C2H4(g)+H2O(g)的平衡常数为5.6 2C2H4(g)+H2O(g)的平衡常数为5.6 |
您最近半年使用:0次