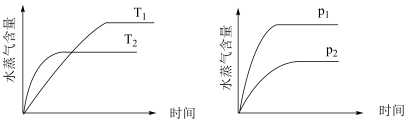
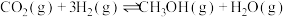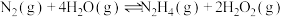下列事实不能 用勒夏特列原理解释的是
| A.加水稀释0.1 mol∙L−1CH3COOH溶液,其电离程度增大 |
| B.NO2和N2O4的混合气体升温后红棕色加深 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D.向水中加入少量NaOH(s)后恢复至常温,溶液的pH增大 |
更新时间:2021-11-12 10:14:33
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】20世纪初,德国化学家哈伯首次利用氨气和氢气合成了氨气N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1,以氨气为原料可制得各种氮肥,大大提高了粮食产量。下列有关合成氨反应说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1,以氨气为原料可制得各种氮肥,大大提高了粮食产量。下列有关合成氨反应说法正确的是
 2NH3(g) ΔH=-92.4kJ·mol-1,以氨气为原料可制得各种氮肥,大大提高了粮食产量。下列有关合成氨反应说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1,以氨气为原料可制得各种氮肥,大大提高了粮食产量。下列有关合成氨反应说法正确的是| A.使用催化剂能改变反应途径,提高反应的活化能 |
| B.及时液化分离出氨气,有利于提高反应物的转化率 |
| C.用E总表示物质能量之和,E总(反应物)<E总(生成物) |
| D.向合成塔中充入1molN2和3molH2,充分反应后放出92.4kJ 的热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】铜氨法可用于测定气体中氧气浓度。该方法是以Cu作为还原剂,用一定量 和氨水的混合液作为吸收液吸收
和氨水的混合液作为吸收液吸收 ,其原理如图所示。
,其原理如图所示。 为蓝色,
为蓝色, 为无色。
为无色。
下列说法错误的是
 和氨水的混合液作为吸收液吸收
和氨水的混合液作为吸收液吸收 ,其原理如图所示。
,其原理如图所示。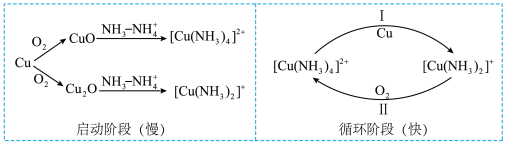
 为蓝色,
为蓝色, 为无色。
为无色。下列说法错误的是
A. 的作用是抑制氨水的电离,防止生成 的作用是抑制氨水的电离,防止生成 沉淀 沉淀 |
B.吸收过程中, 、 、 、 、 是中间产物 是中间产物 |
| C.启动阶段,氨气的加入加快铜氧化物溶于铵盐的速率 |
| D.随着吸收过程不断进行,当吸收液由蓝色变为无色时,表明吸收液已失效 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】合成氨反应为:N2(g)+3H2(g) 2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
 2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是
2NH3(g) △H=−92.4 kJ∙mol−1。对于合成氨反应,下列有关说法正确的是| A.反应的ΔS>0 |
| B.反应的ΔH=6E(N−H) −E(N≡N) −3E(H−H)(E表示键能) |
| C.使用催化剂能改变反应途径,降低反应的活化能 |
| D.升高温度,正反应速率减小,逆反应速率增大,反应逆向进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】对于反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
 CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是
CH3OH(g)+H2O(g) △H<0,有利于提高平衡时CO2转化率的措施是| A.使用催化剂 | B.加压 |
| C.增大CO2和H2的初始投料比 | D.升高温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】利用CH4能消除有害气体NO,其反应原理为CH4(g)+4NO(g) CO2(g)+2N2(g)+2H2O(l)
CO2(g)+2N2(g)+2H2O(l) ,一定温度下,该反应在密闭容器中达到平衡状态。下列说法正确的是
,一定温度下,该反应在密闭容器中达到平衡状态。下列说法正确的是
 CO2(g)+2N2(g)+2H2O(l)
CO2(g)+2N2(g)+2H2O(l) ,一定温度下,该反应在密闭容器中达到平衡状态。下列说法正确的是
,一定温度下,该反应在密闭容器中达到平衡状态。下列说法正确的是| A.加入催化剂,可使反应物的平衡转化率变大 |
| B.恒压下,通入惰性气体He,CH4的平衡转化率减小 |
| C.升高温度,逆反应速率增大,正反应速率减小 |
| D.适当增大压强,化学平衡常数增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】如图是可逆反应A+2B⇌2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断下列说法正确的是


| A.C、D均不是气体 | B.D可能是气体 |
| C.逆反应是放热反应 | D.A、B、C均为气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中,不能用勒夏特列原理解释的是
| A.高压比常压有利于SO2与O2合成SO3的反应 |
| B.加入催化剂有利于N2与H2合成NH3的反应 |
| C.向橙色K2Cr2O7溶液中加入一定浓度的NaOH溶液后,溶液变为黄色 |
| D.工业制取金属钾Na(1)+KCl(l)⇌NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X (g) +Y (g) 2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:

下列说法正确的是
 2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
下列说法正确的是
| A.反应前2 min的平均速率v(Z) =2.0×l0—3mol.L—l·min—l |
| B.其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正) |
| C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,C (Z) =0.24 mol·L—l |
| D.该温度下此反应的平衡常数:K=l. 44 |
您最近一年使用:0次

 反应热:盖斯定律
反应热:盖斯定律 完全燃烧消耗2体积
完全燃烧消耗2体积 溶液中加入少量KSCN固体,溶液颜色加深:勒夏特列原理
溶液中加入少量KSCN固体,溶液颜色加深:勒夏特列原理