电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。用0.100 mol/L的KOH溶液分别滴定体积均为20.00 mL、浓度均为0.100 mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是


| A.相同温度下,C点水的电离程度大于A点 |
| B.由PA段电导率变化趋势可知,K+的导电能力强于H+ |
| C.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1 |
| D.B点溶液中:c(K+)>c(OH-)>c(CH3COO-)>c(H+) |
2021·云南·一模 查看更多[2]
更新时间:2022-01-03 23:49:47
|
相似题推荐
单选题
|
适中
(0.65)
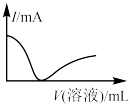
【推荐1】向一定量的CuSO4溶液中逐滴加入Ba(OH)2溶液至沉淀刚好不再增加,然后再逐滴加入稀盐酸至过量,下列各项中的曲线可近似表示整个过程中混合溶液的导电能力(用电流强度I表示)变化的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化的曲线如图所示,下列说法正确的是
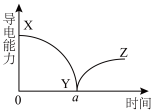

A.XY段溶液中的离子方程式为Ba2++OH-+H++ =BaSO4↓+H2O =BaSO4↓+H2O |
| B.a时刻溶液的导电能力约为0,说明BaSO4不是电解质 |
| C.将稀硫酸换成稀盐酸滴入,测得混合溶液的导电能力随时间变化曲线一样 |
| D.YZ段溶液的导电能力不断增大,主要是由于过量的稀H2SO4电离出的离子导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是


| A.a、b、c、d四个点中,水的电离程度最大的是d |
| B.a点溶液中:c(NH3·H2O)+c(H+)=c(OH-) |
C.b点溶液中:c(Na+)+c(NH4+)=c(SO ) ) |
D.c点溶液中:4c(Na+)= 3[c(SO ) +c(NH4+)+ c(NH3·H2O)] ) +c(NH4+)+ c(NH3·H2O)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子在指定条件下一定能大量共存的是
A.使甲基橙变红的溶液中: 、 、 、 、 、 、 |
B. 溶液中: 溶液中: 、 、 、 、 、 、 |
C.透明溶液中: 、 、 、 、 、 、 |
D. 下,由水电离的 下,由水电离的 溶液中: 溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,浓度均为0.1mol/L的下列四种盐溶液,其pH测定如下表所示:
下列说法正确的是
| 序号 | ① | ② | ③ | ④ |
| 溶液 |  |  |  | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
| A.四种溶液中,水的电离程度:①>②>④>③ |
B. 和 和 溶液中,粒子种类不相同 溶液中,粒子种类不相同 |
C.常温下,等浓度的 和HClO溶液相比较,pH小的是 和HClO溶液相比较,pH小的是 |
D. 溶液中: 溶液中: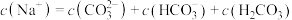 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】问某 和
和 的混合溶液中逐滴加入某浓度的
的混合溶液中逐滴加入某浓度的 溶液,测得溶液中离子浓度的关系如图所示,下列说法不正确的是
溶液,测得溶液中离子浓度的关系如图所示,下列说法不正确的是

 和
和 的混合溶液中逐滴加入某浓度的
的混合溶液中逐滴加入某浓度的 溶液,测得溶液中离子浓度的关系如图所示,下列说法不正确的是
溶液,测得溶液中离子浓度的关系如图所示,下列说法不正确的是
A.溶液中pH由小到大的顺序是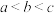 |
B.b点溶液中存在:  |
| C.向b点溶液中加入NaOH可使b点溶液向c点溶液转化 |
D.滴加过程中溶液存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
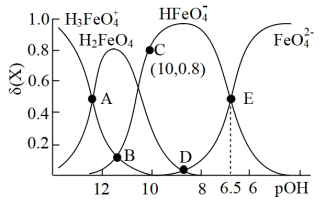
【推荐1】高铁酸盐是一种绿色净水剂,溶于水后, 与水分子结合发生质子化,并存在平衡
与水分子结合发生质子化,并存在平衡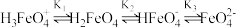 。常温下;0.1mol/L的高铁酸盐溶液中,含铁粒子的物质的量分数
。常温下;0.1mol/L的高铁酸盐溶液中,含铁粒子的物质的量分数 随pOH的变化如图所示[
随pOH的变化如图所示[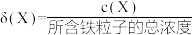 ]。下列说法错误的是
]。下列说法错误的是
 与水分子结合发生质子化,并存在平衡
与水分子结合发生质子化,并存在平衡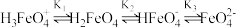 。常温下;0.1mol/L的高铁酸盐溶液中,含铁粒子的物质的量分数
。常温下;0.1mol/L的高铁酸盐溶液中,含铁粒子的物质的量分数 随pOH的变化如图所示[
随pOH的变化如图所示[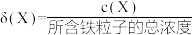 ]。下列说法错误的是
]。下列说法错误的是
A.pH=4时, |
B.B点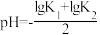 |
C.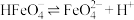 的平衡常数为 的平衡常数为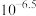 |
| D.溶液中水的电离程度由E点到A点减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】10 mL 0.1 mol/L NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是
A.x=10时,溶液中有 、Al3+、 、Al3+、 ,且 ,且 |
B.x=15时,溶液中有 、 、 ,且 ,且 |
C.x=20时,溶液中有 、Al3+、OH-,且 、Al3+、OH-,且 |
D.x=30时,溶液中有Ba2+、 、OH-,且 、OH-,且 |
您最近一年使用:0次




 的溶液中:
的溶液中: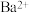 、
、 、
、
 、
、 、
、 、
、 的溶液中:
的溶液中: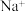 、
、
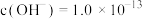
 的溶液中:
的溶液中:

 ) = c(OH-)
) = c(OH-) 溶液:
溶液: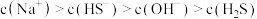
 溶液:
溶液:
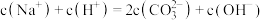
 混合溶液:
混合溶液:


