工业上利用生产磷肥的副产品高磷镍铁制备硫酸镍晶体NiSO4·6H2O。
(1)制备含Ni2+溶液
高磷镍铁 镍铁合金
镍铁合金 含Ni2+溶液
含Ni2+溶液
已知:i.高磷镍铁和镍铁合金中元素的百分含量:
ii.金属活动性:Fe>Co>Ni>H
①依据数据,“转炉吹炼”的主要目的是:富集镍元素,除去部分___________ 。
②“电解造液”时,用镍铁合金作阳极,H2SO4溶液作电解质溶液。电解过程中阴极产生的气体是___________ 。电解一段时间后,有少量Ni在阴极析出,为防止Ni析出降低NiSO4·6H2O的产率,可向电解质溶液中加入___________ (填试剂)。
(2)制备NiSO4·6H2O
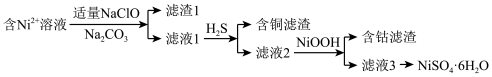
已知:常温下,金属离子完全转化为氢氧化物沉淀的pH:
①在酸性条件下,NaClO和Fe2+反应生成Fe3+和Cl—的离子方程式是___________ 。
②已知Ni(OH)2的Ksp为5.48×10-16,滤液1中c(Ni2+)=1.37mol/L。结合数据说明不能通过调节溶液的pH除去Cu2+的原因:___________ 。(已知:lg5=0.7)
③从滤液3中获取NiSO4·6H2O的操作是___________ 、洗涤、干燥。
(1)制备含Ni2+溶液
高磷镍铁
 镍铁合金
镍铁合金 含Ni2+溶液
含Ni2+溶液已知:i.高磷镍铁和镍铁合金中元素的百分含量:
| 元素/% | Ni/% | Fe/% | P/% | Co/% | Cu/% |
| 高磷镍铁 | 4.58 | 70.40 | 16.12 | 0.22 | 0.34 |
| 镍铁合金 | 52.49 | 38.30 | 5.58 | 1.73 | 1.52 |
①依据数据,“转炉吹炼”的主要目的是:富集镍元素,除去部分
②“电解造液”时,用镍铁合金作阳极,H2SO4溶液作电解质溶液。电解过程中阴极产生的气体是
(2)制备NiSO4·6H2O

已知:常温下,金属离子完全转化为氢氧化物沉淀的pH:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | Co2+ | Ni2+ |
| 完全沉淀的pH | 2.8 | 8.3 | 6.7 | 9.4 | 8.9 |
②已知Ni(OH)2的Ksp为5.48×10-16,滤液1中c(Ni2+)=1.37mol/L。结合数据说明不能通过调节溶液的pH除去Cu2+的原因:
③从滤液3中获取NiSO4·6H2O的操作是
21-22高三上·北京西城·期末 查看更多[6]
北京师范大学第二附属中学2023-2024学年高二上学期12月月考化学试题 北京市第八中学2022-2023学年高二上学期期末考试化学试题北京市第一六六中学2022届高三下学期三模化学试题北京市第一六六中学2022届高三下学期三模化学试题(已下线)一轮巩固卷5-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)北京市西城区2021~2022学年高三上学期期末考试化学试题
更新时间:2022-01-14 20:51:06
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】 是实验室中常用的化学药品之一,可以利用
是实验室中常用的化学药品之一,可以利用 氧化
氧化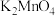 制备
制备 ,设计了如图所示的实验装置(加热及夹持仪器已略去)。回答下列问题:
,设计了如图所示的实验装置(加热及夹持仪器已略去)。回答下列问题:
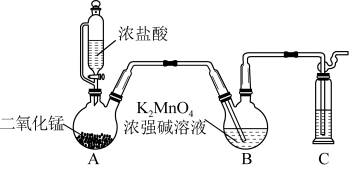
(1)装置A中制备 的化学反应方程式为
的化学反应方程式为_______ ,装置B中生成 的离子反应方程式为
的离子反应方程式为_______ 。
(2) 常作氧化还原滴定的氧化剂,滴定时应将
常作氧化还原滴定的氧化剂,滴定时应将 溶液装入
溶液装入_______ (填“酸式”或“碱式”)滴定管中。现有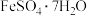 的样品,采用
的样品,采用 滴定法测定该样品的组成(设杂质都不与
滴定法测定该样品的组成(设杂质都不与 反应),实验步骤如下:
反应),实验步骤如下:
(ⅰ)配制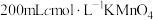 溶液;
溶液;
(ⅱ)洗涤并润洗滴定管,装入高锰酸钾溶液,排气泡,调节液面到0刻度线或以下,记录读数为 ;
;
(ⅲ)准确称取 样品于锥形瓶中,加入稀
样品于锥形瓶中,加入稀 至刚好完全溶解,用
至刚好完全溶解,用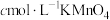 溶液滴定至
溶液滴定至_______ (填现象),记录读数为 。
。
①由以上数据可计算样品中所含 的质量分数,计算表达式为
的质量分数,计算表达式为_______ ;
②下列关于样品误差分析的说法,正确的是_______ (填正确答案标号)。
A.配制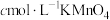 溶液定容时仰视,样品含量测定值偏高
溶液定容时仰视,样品含量测定值偏高
B.未润洗滴定管便装入 溶液,样品含量测定值偏低
溶液,样品含量测定值偏低
C.滴定结束时俯视读数,样品含量测定值偏低
D.滴定前滴定管尖嘴处无气泡,滴定后有气泡,样品含量测定值偏高
 是实验室中常用的化学药品之一,可以利用
是实验室中常用的化学药品之一,可以利用 氧化
氧化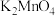 制备
制备 ,设计了如图所示的实验装置(加热及夹持仪器已略去)。回答下列问题:
,设计了如图所示的实验装置(加热及夹持仪器已略去)。回答下列问题:
(1)装置A中制备
 的化学反应方程式为
的化学反应方程式为 的离子反应方程式为
的离子反应方程式为(2)
 常作氧化还原滴定的氧化剂,滴定时应将
常作氧化还原滴定的氧化剂,滴定时应将 溶液装入
溶液装入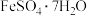 的样品,采用
的样品,采用 滴定法测定该样品的组成(设杂质都不与
滴定法测定该样品的组成(设杂质都不与 反应),实验步骤如下:
反应),实验步骤如下:(ⅰ)配制
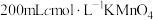 溶液;
溶液;(ⅱ)洗涤并润洗滴定管,装入高锰酸钾溶液,排气泡,调节液面到0刻度线或以下,记录读数为
 ;
;(ⅲ)准确称取
 样品于锥形瓶中,加入稀
样品于锥形瓶中,加入稀 至刚好完全溶解,用
至刚好完全溶解,用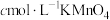 溶液滴定至
溶液滴定至 。
。①由以上数据可计算样品中所含
 的质量分数,计算表达式为
的质量分数,计算表达式为②下列关于样品误差分析的说法,正确的是
A.配制
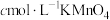 溶液定容时仰视,样品含量测定值偏高
溶液定容时仰视,样品含量测定值偏高B.未润洗滴定管便装入
 溶液,样品含量测定值偏低
溶液,样品含量测定值偏低C.滴定结束时俯视读数,样品含量测定值偏低
D.滴定前滴定管尖嘴处无气泡,滴定后有气泡,样品含量测定值偏高
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾 (K2Cr2O7),其工艺流程及相关物质溶解度曲线如下图所示。
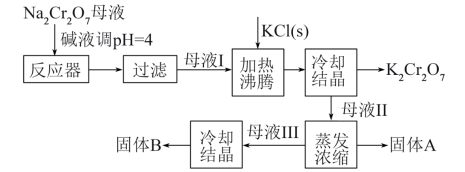
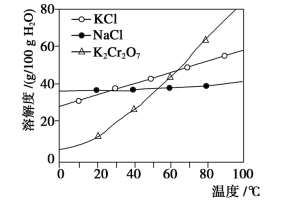
(1)向Na2Cr2O7母液中加碱液调pH的目的是_____________________ 。
(2)通过冷却结晶析出大量K2Cr2O7的原因是________________________________ 。
(3)固体A的主要成分为__________ (填化学式),用热水洗涤固体A,回收的洗涤液转移到母液___________ (填“I”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗降低。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 与K2Cr2O7反应的离子方程式为_____________________________ 。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为__________ %( 保留2 位小数,设整个过程中其他杂质不参与反应)。


(1)向Na2Cr2O7母液中加碱液调pH的目的是
(2)通过冷却结晶析出大量K2Cr2O7的原因是
(3)固体A的主要成分为
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。
①酸性溶液中KI 与K2Cr2O7反应的离子方程式为
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】国家规定,排放的废水中氟的含量不得超过10.0mg/L,砷的含量不得超过0.5mg/L。硫酸工厂废水中除含有稀硫酸外,还含有H3AsO3、H2SiF6等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO4)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:___________ 。
②充分沉淀后测得废水中F的含量为9.5mg/L,此时 的浓度为
的浓度为___________ 。[已知:Ksp(CaSO4)=5.0×10-5、Ksp(CaF2)=5.0×10-9]
(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(II)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电你越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
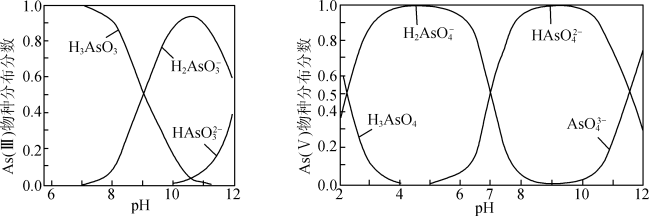
①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:___________ 。
②其它条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。
方式I:先加NaClO溶液,再加FeSO4溶液;
方式II:先加FeSO4溶液,再加NaClO溶液。
反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是___________ 。
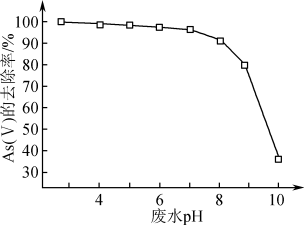
③废水的pH对As(V)的去除率的影响如图所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是___________ 。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO4)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:
②充分沉淀后测得废水中F的含量为9.5mg/L,此时
 的浓度为
的浓度为(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(II)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电你越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:
②其它条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。
方式I:先加NaClO溶液,再加FeSO4溶液;
方式II:先加FeSO4溶液,再加NaClO溶液。
反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是
③废水的pH对As(V)的去除率的影响如图所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是

您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】从镍矿石尾矿中提取NiSO4是解决我国镍资源匮乏的一条重要途径,已知该过程如下:
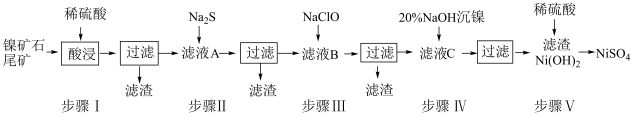
表1:各物质的Ksp数据如下表:
表2:滤液A中各金属离子的含量如下表:
根据以上信息,回答下列问题:
(1)步骤I酸浸之前需将矿石粉碎,目的是____________ 。
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤Ⅱ中当Pb2+“恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=_____________ ;此时Ni2+是否已开始沉淀____ (填“是”或“否”)。
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ ClO - +5H2O=2Fe( OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式______________ 。
(4)为测定滤液A中Fe2+离子的含量,(每升溶液中含有的亚铁离子的质量,以g/L表示)每次移取20.00 mL待测液,并用0.02 mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18. 00mL,则x的值为________ (精确到小数点后两位)。
(5)所得Ni(OH)2是制造镍镉电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH) +2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
则随着放电的进行,正极区pH______ (填“增大”、“减小”或“不变”);充电时阴极电极反应式为______ 。

表1:各物质的Ksp数据如下表:
物质 | MnS | NiS | PbS | CuS | Ni(OH)2 |
Ksp | 2.5×10-13 | 1.1×10-21 | 8.0×10-28 | 6.3×10-36 | 2.0×10-15 |
成分 | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | …… |
3.80 | 4.80 | x | 0. 20 | 0.15 | <0.001 | …… |
根据以上信息,回答下列问题:
(1)步骤I酸浸之前需将矿石粉碎,目的是
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤Ⅱ中当Pb2+“恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ ClO - +5H2O=2Fe( OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式
(4)为测定滤液A中Fe2+离子的含量,(每升溶液中含有的亚铁离子的质量,以g/L表示)每次移取20.00 mL待测液,并用0.02 mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18. 00mL,则x的值为
(5)所得Ni(OH)2是制造镍镉电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH) +2H2O
 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2则随着放电的进行,正极区pH
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】国家规定,排放的废水中氟的含量不得超过10.0mg·L-1,砷的含量不得超过0.5mg·L-1。硫酸工厂废水中除含有稀硫酸外,还含有H3AsO3、H2SiF6等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:____ 。
②充分沉淀后测得废水中F-的含量为9.5mg·L-1,此时SO 的浓度为
的浓度为____ mol·L-1。[已知:Ksp(CaSO4)=5.0×10-5,Ksp(CaF2)=5.0×10-9]
(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电荷越多。
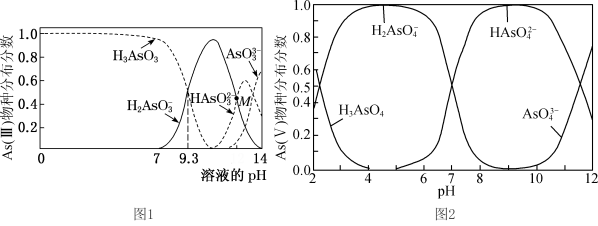
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:____ 。
②H3AsO3第一步电离的电离常数为Ka1,则pKa1=____ (pKa1=-lgKa1)。
③如图1为向0.1mol/LH3AsO3溶液逐滴加入KOH溶液,含砷物种的分布分数图,下列说法正确的是____ 。
A.当n(H3AsO3):n(H2AsO )=1:1时,溶液呈碱性
)=1:1时,溶液呈碱性
B.pH在8.0~10.0时,反应的离子方程式为:H3AsO3+OH-=H2AsO +H2O
+H2O
C.M点对应的溶液中:c(H2AsO )+c(HAsO
)+c(HAsO )+c(AsO
)+c(AsO )+c(H3AsO3)=0.1mol·L-1
)+c(H3AsO3)=0.1mol·L-1
D.pH=12时,溶液中:c(H2AsO )+2c(HAsO
)+2c(HAsO )+3c(AsO
)+3c(AsO )+c(H3AsO3)>c(H+)+c(K+)
)+c(H3AsO3)>c(H+)+c(K+)
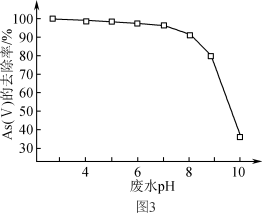
④废水的pH对As(V)的去除率的影响如图3所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是____ 。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主]、过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO3)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:
②充分沉淀后测得废水中F-的含量为9.5mg·L-1,此时SO
 的浓度为
的浓度为(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(III)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电荷越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:
②H3AsO3第一步电离的电离常数为Ka1,则pKa1=
③如图1为向0.1mol/LH3AsO3溶液逐滴加入KOH溶液,含砷物种的分布分数图,下列说法正确的是
A.当n(H3AsO3):n(H2AsO
 )=1:1时,溶液呈碱性
)=1:1时,溶液呈碱性B.pH在8.0~10.0时,反应的离子方程式为:H3AsO3+OH-=H2AsO
 +H2O
+H2OC.M点对应的溶液中:c(H2AsO
 )+c(HAsO
)+c(HAsO )+c(AsO
)+c(AsO )+c(H3AsO3)=0.1mol·L-1
)+c(H3AsO3)=0.1mol·L-1D.pH=12时,溶液中:c(H2AsO
 )+2c(HAsO
)+2c(HAsO )+3c(AsO
)+3c(AsO )+c(H3AsO3)>c(H+)+c(K+)
)+c(H3AsO3)>c(H+)+c(K+)④废水的pH对As(V)的去除率的影响如图3所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是

您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】利用含钴废料(主要成分为 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: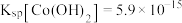 ;
;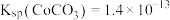 。
。
请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为 和
和___________ 。“酸浸”时 发生反应的总离子方程式为
发生反应的总离子方程式为___________ 。
(2)“萃取”时 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)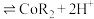 ,若萃取剂的量一定时,
,若萃取剂的量一定时,___________ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。若“酸浸”后浸出液的 ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为___________ (结果保留一位小数,溶液体积变化忽略不计)。
(3)“沉锰”时, 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为___________ 。
(4)可以通过电解 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是___________ 。若Ⅱ室溶液中溶质的质量增加了 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为___________ 。
 、
、 、
、 、
、 以及
以及 、
、 等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示:
等)制备碳酸钴和硫酸镍晶体的一种工艺流程如图所示: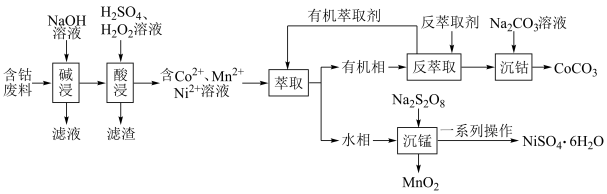
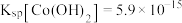 ;
;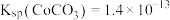 。
。请回答下列问题:
(1)“碱浸”时所得滤液中溶质的主要成分为
 和
和 发生反应的总离子方程式为
发生反应的总离子方程式为(2)“萃取”时
 萃取的反应原理如下:
萃取的反应原理如下: (有机层)
(有机层)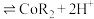 ,若萃取剂的量一定时,
,若萃取剂的量一定时, ,
, ,萃取完成后水相中
,萃取完成后水相中 为
为 ,则钴的萃取率为
,则钴的萃取率为(3)“沉锰”时,
 转化为
转化为 ,则“沉锰”时发生反应的离子方程式为
,则“沉锰”时发生反应的离子方程式为(4)可以通过电解
 溶液获得单质
溶液获得单质 和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是
和较浓的盐酸,其工作原理如图所示,其中膜a和膜b中,属于阳离子交换膜的是 ,则理论上获得的单质
,则理论上获得的单质 的质量为
的质量为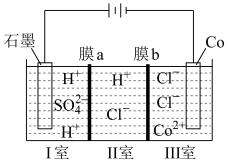
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】工业上用含锰废料(主要成分 ,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备
,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备 的流程如下:
的流程如下:
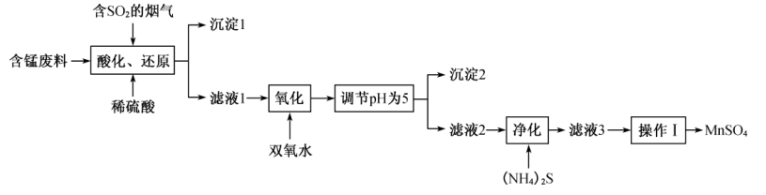
已知:25℃时,部分物质的溶度积常数( )如下表所示。
)如下表所示。
(1)Mn的原子序数为25,请写出其价电子的核外电子排布式_______ 。
(2)沉淀1为_______ 。
(3)室温下,若滤液1中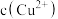 为
为 ,当pH调节到5时,
,当pH调节到5时,_______ (填“能”或“不能”)产生 沉淀。
沉淀。
(4)室温下,调节pH到5时,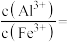
_______ 。
(5)“净化”时,加入 的作用为
的作用为_______ ;加入 的量不宜过多,原因是
的量不宜过多,原因是_______ 。
(6)在“酸化、还原”过程中,主要发生的氧化还原反应的离子方程式为_______ 。
(7)工业上可用电解酸性 溶液的方法制备
溶液的方法制备 ,其阳极反应式为
,其阳极反应式为_______ 。
 ,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备
,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备 的流程如下:
的流程如下:
已知:25℃时,部分物质的溶度积常数(
 )如下表所示。
)如下表所示。 |  |  |  | |
 | 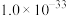 |  | 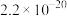 |  |
| CuS | MnS |  | ||
 |  | 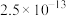 | 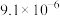 |
(1)Mn的原子序数为25,请写出其价电子的核外电子排布式
(2)沉淀1为
(3)室温下,若滤液1中
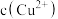 为
为 ,当pH调节到5时,
,当pH调节到5时, 沉淀。
沉淀。(4)室温下,调节pH到5时,
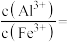
(5)“净化”时,加入
 的作用为
的作用为 的量不宜过多,原因是
的量不宜过多,原因是(6)在“酸化、还原”过程中,主要发生的氧化还原反应的离子方程式为
(7)工业上可用电解酸性
 溶液的方法制备
溶液的方法制备 ,其阳极反应式为
,其阳极反应式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】工业用黄铜矿【主要成分CuFeS2(Fe化合价+2),含少量锌、铅的硫化物】冶炼铜的一种方法如图:
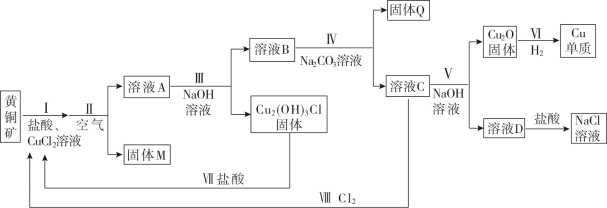
(1)从流程图可以看出,第III步的分离操作是__ 。
(2)完成Ⅰ中发生反应的离子方程式。___ 。
CuFeS2+____Cu2++____ =____CuCl
=____CuCl +Fe2++____S
+Fe2++____S
(3)固体M是S和FeOOH的混合物,写出Ⅱ中通入空气,将FeCl2转化FeOOH沉淀的化学方程式是___ 。
(4)溶液B中含金属元素的离子有:Zn2+、Pb2+和CuCl ,下列说法正确的是
,下列说法正确的是____ 。
(5)反应Ⅵ中用H2将57.6kgCu2O完全还原,若H2的利用率是80%,则需要提供H2的体积是__ m3(标准状况)。
(6)从物质循环利用的角度看,电解NaCl溶液能够很好的服务于该冶炼铜的工艺,分析图(a),结合化学用语说明骤Ⅲ所需原料的生成原理:___ 。
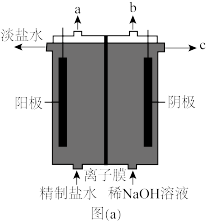

(1)从流程图可以看出,第III步的分离操作是
(2)完成Ⅰ中发生反应的离子方程式。
CuFeS2+____Cu2++____
 =____CuCl
=____CuCl +Fe2++____S
+Fe2++____S(3)固体M是S和FeOOH的混合物,写出Ⅱ中通入空气,将FeCl2转化FeOOH沉淀的化学方程式是
(4)溶液B中含金属元素的离子有:Zn2+、Pb2+和CuCl
 ,下列说法正确的是
,下列说法正确的是| A.Ⅲ中需控制NaOH溶液的用量 |
| B.Ⅳ中加入Na2CO3溶液的目的是除去Zn2+、Pb2+ |
| C.反应Ⅴ发生了氧化还原反应 |
(6)从物质循环利用的角度看,电解NaCl溶液能够很好的服务于该冶炼铜的工艺,分析图(a),结合化学用语说明骤Ⅲ所需原料的生成原理:

您最近半年使用:0次
【推荐3】高锰酸钾常用作消毒杀菌剂、水质净化剂等。某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题:
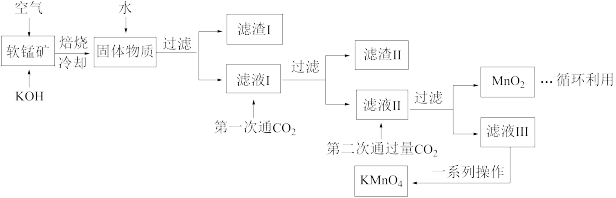
(1)配平焙烧时发生的化学反应方程式:_____ MnO2+_____ ______ +________ O2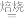
________ K2MnO4+________ H2O;
(2)滤渣Ⅱ的成分有________ (化学式);第一次通CO2不能用稀盐酸代替的原因是_______ 。
(3)第二次通入过量CO2生成MnO2的离子方程式为______________ 。
(4)将滤液Ⅲ进行一系列操作得KMnO4。由图像可知,从滤液Ⅲ得到KMnO4需经过______ 、________ 、洗涤等操作。
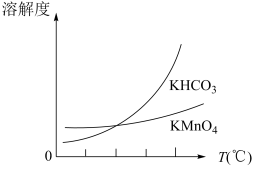
(5)工业上按上述流程连续生产。用含a%MnO2的软锰矿1吨,理论上最多可制KMnO4________ 吨。(保留2位有效数字)
(6)利用电解法可得到更纯的KMnO4。用惰性电极电解滤液Ⅱ。
①电解槽阳极反应式为________________ 。
②阳极还可能有气体产生,该气体是________ 。

(1)配平焙烧时发生的化学反应方程式:
(2)滤渣Ⅱ的成分有
(3)第二次通入过量CO2生成MnO2的离子方程式为
(4)将滤液Ⅲ进行一系列操作得KMnO4。由图像可知,从滤液Ⅲ得到KMnO4需经过

(5)工业上按上述流程连续生产。用含a%MnO2的软锰矿1吨,理论上最多可制KMnO4
(6)利用电解法可得到更纯的KMnO4。用惰性电极电解滤液Ⅱ。
①电解槽阳极反应式为
②阳极还可能有气体产生,该气体是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】在金属冶炼产生的废弃物中,常含有砷元素(与磷同主族),由于有毒需检测与处理。
Ⅰ.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
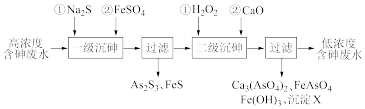
已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为___ ;砷酸的第一步电离方程式为__ 。
(2)“一级沉砷”中FeSO4的作用是___ 。
(3)“二级沉砷”中H2O2与含砷物质反应的化学方程式为___ 。沉淀X为___ (填化学式)。
Ⅱ.强阴离子交换柱可以吸附以阴离子形态存在的As(V)达到去除As的目的。采用该方法去除水体中的砷时,可选用NaClO将As(Ⅲ)转化为As(V)。

已知:一定条件下,As(V)的存在形式如表所示:
(4)pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是___ 。
Ⅲ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成(即未能检出)。
(5)请写出步骤2的离子方程式____ 。
Ⅰ.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq)
 2AsS33-(aq);
2AsS33-(aq);②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为
(2)“一级沉砷”中FeSO4的作用是
(3)“二级沉砷”中H2O2与含砷物质反应的化学方程式为
Ⅱ.强阴离子交换柱可以吸附以阴离子形态存在的As(V)达到去除As的目的。采用该方法去除水体中的砷时,可选用NaClO将As(Ⅲ)转化为As(V)。

已知:一定条件下,As(V)的存在形式如表所示:
| pH | <2 | 2~7 | 7~11 | 11~14 |
| 存在形式 | H3AsO4 | H2AsO4− | HAsO42− | HAsO42−、AsO43− |
(4)pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是
Ⅲ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成(即未能检出)。
(5)请写出步骤2的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】氯化亚铜(CuCl)是一种见光易分解的白色固体,难溶于水,在潮湿的环境中易被氧气氧化为碱式氯化铜。实验室用SOCl2与CuCl2溶液混合制取CuCl的装置如图所示。
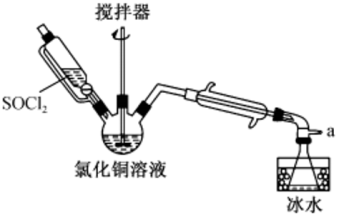
已知:
①SOCl2是一种易发烟的液体,遇水剧烈水解生成SO2和HCl气体;
②CuCl在溶液中存在如下平衡:CuCl(s)+3Cl-(aq) [CuCl4]3-(aq)(无色)。
[CuCl4]3-(aq)(无色)。
回答下列问题:
(1)配制CuCl2溶液所需的蒸馏水需要去氧气,最简单的去氧操作是_______ 。
(2)当三颈烧瓶的溶液由_____ 时(填实验现象),则说明反应已经完成,可以停止实验。
(3)实验结束后需要先向三颈烧瓶中加入去氧水,然后再进行过滤得到CuCl。加水的作用是____ ,过滤时需要在避光的条件下进行,原因是_____ 。
(4)经过滤得到的CuCl沉淀,先用无水乙醇洗涤,然后在真空干燥机内于70℃下干燥2小时,冷却,密封保存。“70℃真空干燥”的目的是_____ 。
(5)久置在空气中的CuCl可完全变质为碱式氯化铜[xCuCl2·yCu(OH)2,其x、y为整数],为探究该碱式氯化铜的组成,设计如下实验步骤:
①准确称取4.216g样品,溶于足量乙酸中,加蒸馏水配制成100mL溶液;
②取25mL溶液,向其中加入足量的AgNO3溶液,充分反应后过滤、洗涤、干燥,所得白色固体质量为0.574g;
③另取25mL溶液,向其中加入过量的KI溶液,再用0.400mol·L-1的Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知滴定过程涉及如下反应:2Cu2++4I-=2CuI↓+I2、2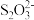 +I2=2I-+
+I2=2I-+ 。
。
计算碱式氯化铜中x=_____ ;y=____ 。

已知:
①SOCl2是一种易发烟的液体,遇水剧烈水解生成SO2和HCl气体;
②CuCl在溶液中存在如下平衡:CuCl(s)+3Cl-(aq)
 [CuCl4]3-(aq)(无色)。
[CuCl4]3-(aq)(无色)。回答下列问题:
(1)配制CuCl2溶液所需的蒸馏水需要去氧气,最简单的去氧操作是
(2)当三颈烧瓶的溶液由
(3)实验结束后需要先向三颈烧瓶中加入去氧水,然后再进行过滤得到CuCl。加水的作用是
(4)经过滤得到的CuCl沉淀,先用无水乙醇洗涤,然后在真空干燥机内于70℃下干燥2小时,冷却,密封保存。“70℃真空干燥”的目的是
(5)久置在空气中的CuCl可完全变质为碱式氯化铜[xCuCl2·yCu(OH)2,其x、y为整数],为探究该碱式氯化铜的组成,设计如下实验步骤:
①准确称取4.216g样品,溶于足量乙酸中,加蒸馏水配制成100mL溶液;
②取25mL溶液,向其中加入足量的AgNO3溶液,充分反应后过滤、洗涤、干燥,所得白色固体质量为0.574g;
③另取25mL溶液,向其中加入过量的KI溶液,再用0.400mol·L-1的Na2S2O3标准溶液滴定至终点,消耗标准溶液25.00mL。已知滴定过程涉及如下反应:2Cu2++4I-=2CuI↓+I2、2
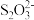 +I2=2I-+
+I2=2I-+ 。
。计算碱式氯化铜中x=
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】连二亚硫酸钠(Na2S2O4)是无机精细化学品,在造纸、印染等行业应用广泛。某科研小组通过以下方案制备Na2S2O4并测定其纯度。
已知:①Na2S2O4在空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定。
②低于52℃时Na2S2O4在水溶液中以Na2S2O4·2H2O形态结晶,高于52℃时Na2S2O4·2H2O在碱性溶液中脱水成无水盐。
请回答下列问题:
I.Na2S2O4的制备
其制备过程如下:
步骤1:安装好整套装置(夹持装置省略),并检查装置的气密性;
步骤2:在三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
步骤3:打开仪器a的活塞,向装置C中先通入一段时间SO2;
步骤4:打开仪器c的活塞滴加稍过量NaOH溶液使装置C中溶液的pH在8.2~10.5之间;
步骤5:过滤,将滤液经“一系列操作”可获得Na2S2O4。
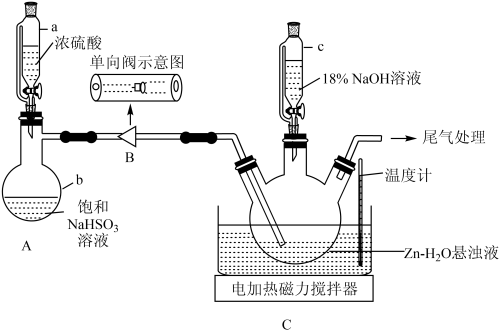
(1)仪器b的名称是____ 。
(2)写出装置A中发生反应的化学方程式:____ 。
(3)装置B(单向阀)的作用是防倒吸,下列装置能代替它的是____ (填字母)。
a.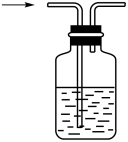 b.
b.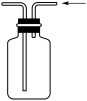 c.
c. d.
d.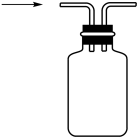
(4)步骤3中生成物为ZnS2O4,该反应需控制温度在35~45℃进行,其原因为____ 。
(5)步骤4中,需控制溶液的pH在8.2~10.5之间,其原因为:
①pH太大Zn(OH)2会溶解;
②pH太小Zn2+沉淀不完全;
③____ 。
(6)“一系列操作”包括:
a.搅拌下用水蒸气加热至60℃左右;
b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;
c.趁热过滤;
d.用乙醇洗涤。
上述操作的合理顺序为____ →干燥(填字母)。
II.Na2S2O4含量的测定
实验装置:
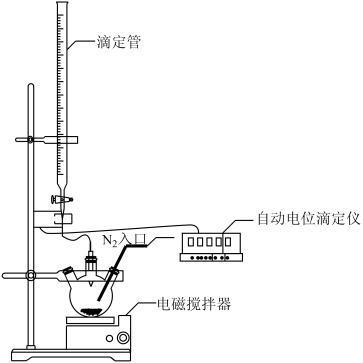
实验原理:[Fe(CN)6]3-+S2O +OH-——SO
+OH-——SO +[Fe(CN)6]4-+H2O(未配平)。
+[Fe(CN)6]4-+H2O(未配平)。
实验过程:称取0.25g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.10mol·L-1,K3[Fe(CN)6]标准溶液,达到滴定终点时消耗24.00mL标准溶液。
(7)样品中Na2S2O4的质量分数为____ %(假设杂质不参与反应);若实验过程中忘记通入N2,对测定Na2S2O4含量的影响是____ (填“偏低”“偏高”或“无影响”)。
已知:①Na2S2O4在空气中极易被氧化,易溶于水且随温度的升高溶解度增大,不溶于乙醇,在碱性介质中较稳定。
②低于52℃时Na2S2O4在水溶液中以Na2S2O4·2H2O形态结晶,高于52℃时Na2S2O4·2H2O在碱性溶液中脱水成无水盐。
请回答下列问题:
I.Na2S2O4的制备
其制备过程如下:
步骤1:安装好整套装置(夹持装置省略),并检查装置的气密性;
步骤2:在三颈烧瓶中依次加入Zn粉和水,电磁搅拌形成悬浊液;
步骤3:打开仪器a的活塞,向装置C中先通入一段时间SO2;
步骤4:打开仪器c的活塞滴加稍过量NaOH溶液使装置C中溶液的pH在8.2~10.5之间;
步骤5:过滤,将滤液经“一系列操作”可获得Na2S2O4。

(1)仪器b的名称是
(2)写出装置A中发生反应的化学方程式:
(3)装置B(单向阀)的作用是防倒吸,下列装置能代替它的是
a.
 b.
b. c.
c. d.
d.
(4)步骤3中生成物为ZnS2O4,该反应需控制温度在35~45℃进行,其原因为
(5)步骤4中,需控制溶液的pH在8.2~10.5之间,其原因为:
①pH太大Zn(OH)2会溶解;
②pH太小Zn2+沉淀不完全;
③
(6)“一系列操作”包括:
a.搅拌下用水蒸气加热至60℃左右;
b.分批逐步加入细食盐粉,搅拌使其结晶,用倾析法除去上层溶液,余少量母液;
c.趁热过滤;
d.用乙醇洗涤。
上述操作的合理顺序为
II.Na2S2O4含量的测定
实验装置:

实验原理:[Fe(CN)6]3-+S2O
 +OH-——SO
+OH-——SO +[Fe(CN)6]4-+H2O(未配平)。
+[Fe(CN)6]4-+H2O(未配平)。实验过程:称取0.25g样品加入三颈烧瓶中,加入适量NaOH溶液,打开电磁搅拌器,通过滴定仪控制滴定管向三颈烧瓶中快速滴加0.10mol·L-1,K3[Fe(CN)6]标准溶液,达到滴定终点时消耗24.00mL标准溶液。
(7)样品中Na2S2O4的质量分数为
您最近半年使用:0次



