下列有关反应 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是A.反应中每消耗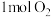 转移的电子数目约等于 转移的电子数目约等于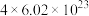 |
B. 和 和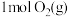 所含化学键的键能总和高于 所含化学键的键能总和高于 的键能 的键能 |
C.每 和过量 和过量 通过接触室,可放出 通过接触室,可放出 热量 热量 |
D.使用催化剂能加快化学反应速率,提高 的平衡转化率 的平衡转化率 |
更新时间:2022-01-23 18:56:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,2H2(g)+O2(g) 2H2O(l)+566kJ。下列说法错误的是
2H2O(l)+566kJ。下列说法错误的是
 2H2O(l)+566kJ。下列说法错误的是
2H2O(l)+566kJ。下列说法错误的是A.H2 H+H的过程需要吸热 H+H的过程需要吸热 |
| B.若生成2mol水蒸气,则放出的热量大于566kJ |
| C.2g氢气完全燃烧生成液态水所释放的能量为283kJ |
| D.2mol氢气与1mol氧气的能量之和大于2mol液态水的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在反应CH4(g)=C(s)+2H2(g) △H中,1molC(s)成键释放的热量为709.6kJ,C-H的键能为414kJ•mol-1,则H-H的键能为
已知:反应①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ•mol-1;
反应②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205.9kJ•mol-1。
已知:反应①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ•mol-1;
反应②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205.9kJ•mol-1。
| A.872kJ | B.436kJ | C.872kJ•mol-1 | D.436kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在PdCl2-CuCl2做催化剂和适宜的温度条件下,用O2将HCl氧化为Cl2:4HCl(g)+O2(g)=2H2O(g)+2Cl2(g) ΔH<0,下列有关说法不正确的是
| A.降低温度,可提高Cl2产率 |
B.提高 ,该反应的平衡常数增大 ,该反应的平衡常数增大 |
| C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态 |
D.该反应的平衡常数表达式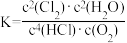 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用无机离子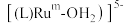 和
和 (如图可简写为
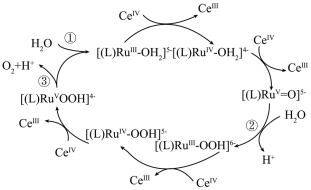
(如图可简写为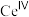 ,可以实现水在催化剂作用下制氧气。其相关机理如图所示,下列说法
,可以实现水在催化剂作用下制氧气。其相关机理如图所示,下列说法不正确 的是
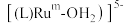 和
和 (如图可简写为
(如图可简写为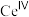 ,可以实现水在催化剂作用下制氧气。其相关机理如图所示,下列说法
,可以实现水在催化剂作用下制氧气。其相关机理如图所示,下列说法
A.若反应①中为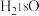 ,反应②中为 ,反应②中为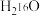 ,则产生 ,则产生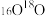 |
| B.反应机理整个过程涉及非氧化还原反应 |
C.催化氧化水的反应为:  |
D.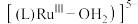 在反应中做催化剂 在反应中做催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】有反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
 CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下| A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.增大反应物浓度,反应的ΔH也随之改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对一个可逆反应来说,升高温度下列物理量一定增大的是
| A.反应速率 | B.平衡常数 | C.催化剂的活性 | D.反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】图中a曲线表示一定条件下的可逆反应:X(g)+Y(g) 2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
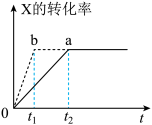
 2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
2Z(g)+W(g);△H=QkJ/mol的反应过程。若使a曲线变为b曲线,可采取的措施是( )
| A.降低温度 | B.增大Y的浓度 |
| C.加入催化剂 | D.增大体系压强 |
您最近一年使用:0次

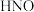 自由基与
自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是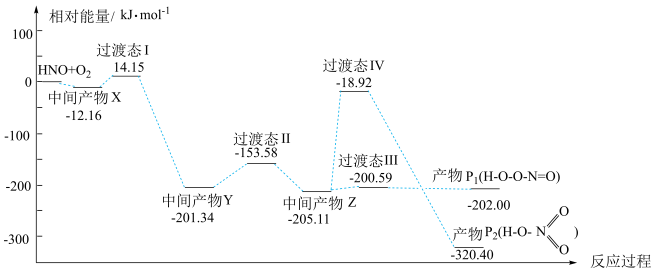
 的键能总和大于产物
的键能总和大于产物 的键能总和
的键能总和 转化为产物的速率:
转化为产物的速率:



