反应 在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
在有、无催化剂条件下的能量变化如图所示。下列说法正确的是

 在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
在有、无催化剂条件下的能量变化如图所示。下列说法正确的是
A. 催化时,该反应的速率取决于步骤① 催化时,该反应的速率取决于步骤① |
B.使用 作催化剂同时降低了正、逆反应的活化能 作催化剂同时降低了正、逆反应的活化能 |
| C.升高温度,正反应的平衡常数增大 |
D.其他条件相同,增大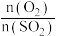 , , 的转化率下降 的转化率下降 |
更新时间:2022-01-23 18:56:38
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】计算机模拟研究反应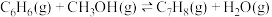 在固体酸(HB)催化剂表面进行的反应历程如图所示(其中吸附在固体酸(HB)表面的物种用*标注)。下列说法
在固体酸(HB)催化剂表面进行的反应历程如图所示(其中吸附在固体酸(HB)表面的物种用*标注)。下列说法不正确 的是

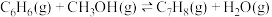 在固体酸(HB)催化剂表面进行的反应历程如图所示(其中吸附在固体酸(HB)表面的物种用*标注)。下列说法
在固体酸(HB)催化剂表面进行的反应历程如图所示(其中吸附在固体酸(HB)表面的物种用*标注)。下列说法
A.该反应的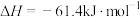 |
B.反应历程中最大的能垒 |
C.C6H6*在催化剂表面转化为C7H8*的反应方程式为 |
| D.将固体酸(HB)催化剂更换为固体活性催化剂(MN)能有效提高C6H6(g)的平衡转化率 |
您最近一年使用:0次
【推荐2】CO2氧化含氮焦炭的反应历程中某一路径的能量变化如图所示,TS表示过渡态,IM表示中间产物,下列说法错误的是


| A.d-TS2到d-IM2的过程中C=O键断裂 |
| B.该反应是吸热反应 |
| C.该反应历程中C、N化合价均发生了变化 |
| D.该反应的最大能垒为598.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知:气态分子中 化学键解离成气态原子所吸收的能量叫键能。在催化剂作用下,发生反应:
化学键解离成气态原子所吸收的能量叫键能。在催化剂作用下,发生反应: 。有关数据如下:
。有关数据如下:
下列叙述正确的是
 化学键解离成气态原子所吸收的能量叫键能。在催化剂作用下,发生反应:
化学键解离成气态原子所吸收的能量叫键能。在催化剂作用下,发生反应: 。有关数据如下:
。有关数据如下:| 化学键 |  |  |  |
键能 | 436 | 391 | 946 |
A. |
B. |
| C.合成氨反应必须是在高温下才能自发进行 |
D.平衡后,增大 浓度, 浓度, 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】向某一恒容密闭容器中充入一定量的X(g)、Y(g),发生反应X(g)+Y(g) 2Z(g) ΔH<0,下列说法正确的是
2Z(g) ΔH<0,下列说法正确的是
 2Z(g) ΔH<0,下列说法正确的是
2Z(g) ΔH<0,下列说法正确的是| A.反应达到平衡后,仅升高温度,该反应的平衡常数增大 |
| B.加入合适的催化剂,可提高Z的产率 |
| C.仅增大Y的物质的量浓度,X的平衡转化率增大 |
| D.当n(X):n(Y):n(Z)=1:1:2时,该反应一定达到平衡 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】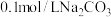 溶液的
溶液的 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是

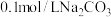 溶液的
溶液的 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是
A.温度高于 时, 时, 变化主要受水的电离平衡移动的影响 变化主要受水的电离平衡移动的影响 |
B.常温下: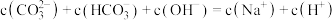 |
C.常温下: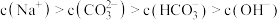 |
| D.升高温度,溶液中的水解平衡逆向移动,导致溶液pH减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】CoCl2可溶。将 溶解于盐酸中可形成
溶解于盐酸中可形成 ,在溶液中存在下面的化学平衡:
,在溶液中存在下面的化学平衡: 。下列说法不正确的是
。下列说法不正确的是
 溶解于盐酸中可形成
溶解于盐酸中可形成 ,在溶液中存在下面的化学平衡:
,在溶液中存在下面的化学平衡: 。下列说法不正确的是
。下列说法不正确的是| A.升高温度,正反应速率、逆反应速率都增大 |
B.该反应的平衡常数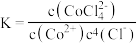 |
C.将盛有 和盐酸混合液的试管置于热水中,试管内溶液为蓝色 和盐酸混合液的试管置于热水中,试管内溶液为蓝色 |
| D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某温度下,反应mA(g)+nB(g)⇌pC(g)+qD(g)的平衡常数为K,下列说法正确的是( )
| A.K越大,达到平衡时,反应物的转化率越大 | B.K越小,达到平衡时,反应物的转化率越大 |
| C.K随反应物浓度改变而改变 | D.K随温度的改变而改变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】煤燃烧排放的烟气含有 和
和 ,对烟气进行脱硫、脱硝,对环境保护有着重要意义。在脱硫实验中发生反应:
,对烟气进行脱硫、脱硝,对环境保护有着重要意义。在脱硫实验中发生反应: ,在体积为
,在体积为 的恒容密闭容器中,通入
的恒容密闭容器中,通入 和
和 ,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法正确的是
,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法正确的是

 和
和 ,对烟气进行脱硫、脱硝,对环境保护有着重要意义。在脱硫实验中发生反应:
,对烟气进行脱硫、脱硝,对环境保护有着重要意义。在脱硫实验中发生反应: ,在体积为
,在体积为 的恒容密闭容器中,通入
的恒容密闭容器中,通入 和
和 ,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法正确的是
,在不同条件下进行反应时体系的总压强随时间的变化如图所示。下列说法正确的是
A.若采用 处理烟气,可以脱硫,不能脱硝 处理烟气,可以脱硫,不能脱硝 |
B. 的化学平衡常数大于 的化学平衡常数大于 |
C. 对应 对应 达到平衡,则在 达到平衡,则在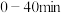 内用 内用 表示的平均反应速率为 表示的平均反应速率为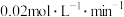 |
D.a达到平衡时, 的转化率小于 的转化率小于 的转化率 的转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】一定温度下,向10L恒容密闭容器中分别充入①1mol X气体和2mol Y气体、②2mol X气体和4mol Y气体,均发生反应X(g)+Y(g) nZ(?),实验过程中测得的数据如下表所示,下列说法错误的是
nZ(?),实验过程中测得的数据如下表所示,下列说法错误的是
 nZ(?),实验过程中测得的数据如下表所示,下列说法错误的是
nZ(?),实验过程中测得的数据如下表所示,下列说法错误的是时间/min Z的物质的量/mol 实验序号 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| ① | 0 | 0.40 | 0.70 | 0.95 | 1.10 | 1.20 | 1.20 |
| ② | 0 | 0.95 | 1.65 | 2.18 | 2.40 | 2.40 | 2.40 |
| A.n=2 |
| B.Z可能为液体 |
| C.实验①中X的平衡转化率等于实验② |
| D.实验①和实验②的平衡常数相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】一定条件下,在一个容积为 的密闭容器中加入
的密闭容器中加入 气体和
气体和 气体,反应达到平衡时生成
气体,反应达到平衡时生成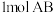 气体并释放出能量:反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是( )
气体并释放出能量:反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是( )

 的密闭容器中加入
的密闭容器中加入 气体和
气体和 气体,反应达到平衡时生成
气体,反应达到平衡时生成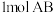 气体并释放出能量:反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是( )
气体并释放出能量:反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是( )
A.图中a的值为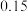 | B.该反应的平衡常数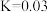 |
C.平衡时 物质的量为 物质的量为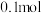 | D.平衡时 的转化率为 的转化率为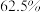 |
您最近一年使用:0次

 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是 ( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是 ( )

