2021年11月2日,第四届世界顶尖科学家碳大会——通往“双碳目标”的科技之路论坛在上海召开。我国科学家刘科提到了绿色甲醇技术,将CO2转化为甲醇是实现碳达峰、碳中和的一种非常重要的路径。回答下列问题:
(1)已知H2(g)和CH3OH(l)的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应生成液态甲醇和液态水的热化学方程式为_____ 。
(2)最近科学家采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,反应历程如图所示:
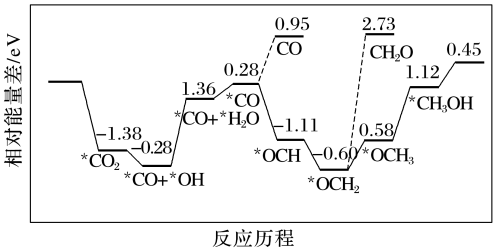
①反应容易得到的副产物有CO和CH2O,其中相对较少的副产物为_____ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_____ (填字母)的能量变化。
A.*CO+*OH→*CO+*H2O B.*CO+*H2O→*CO
C.*OCH2→*OCH3 D.*OCH3→*CH3OH
(3)一定条件下,在1L恒容密闭容器中充入1molCO2和3molH2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
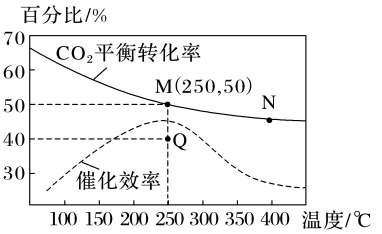
①下列说法能说明该反应达到化学平衡状态的是_____ (填字母)。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
D.H2O(g)和CO2(g)的生成速率之比为1∶1
②反应速率:v正(M)_____ (填“大于”“小于”“等于”或“无法判断”,下同)v逆(N),化学平衡常数:KM_____ KN。
③M点甲醇的体积分数为_____ ,该温度下,反应的平衡常数K=_____ 。
④已知:反应速率v=v正-v逆=k正c(CO2)·c3(H2)-k逆c(CH3OH)·c(H2O),k正、k逆分别为正、逆反应速率常数,则Q点时 =
=_____ (保留2位小数)。
(1)已知H2(g)和CH3OH(l)的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应生成液态甲醇和液态水的热化学方程式为
(2)最近科学家采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,反应历程如图所示:

①反应容易得到的副产物有CO和CH2O,其中相对较少的副产物为
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.*CO+*OH→*CO+*H2O B.*CO+*H2O→*CO
C.*OCH2→*OCH3 D.*OCH3→*CH3OH
(3)一定条件下,在1L恒容密闭容器中充入1molCO2和3molH2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
①下列说法能说明该反应达到化学平衡状态的是
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
D.H2O(g)和CO2(g)的生成速率之比为1∶1
②反应速率:v正(M)
③M点甲醇的体积分数为
④已知:反应速率v=v正-v逆=k正c(CO2)·c3(H2)-k逆c(CH3OH)·c(H2O),k正、k逆分别为正、逆反应速率常数,则Q点时
 =
=
更新时间:2022-02-08 17:59:26
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
【推荐1】“雾疆”成为人们越来越关心的环境问题。雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质。回答下列问题:
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质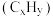 催化还原尾气中的NO气体,该过程的化学方程式为
催化还原尾气中的NO气体,该过程的化学方程式为________ 。
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。经研究发现将煤炭在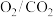 的气氛下燃烧,能够降低煤炭燃烧时NO的排放,主要反应为
的气氛下燃烧,能够降低煤炭燃烧时NO的排放,主要反应为 。
。
已知:①
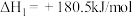
②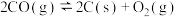
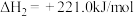
③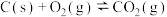
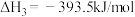
则反应 的
的
________ 。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的 溶液进行电解,其中阴、阳膜组合电解装置如图所示,电极材料为石墨。
溶液进行电解,其中阴、阳膜组合电解装置如图所示,电极材料为石墨。
① 表示
表示________  填“阴离子”或“阳离子”
填“阴离子”或“阳离子” 交换膜。
交换膜。 分别代表生产中的原料或产品,其中C为硫酸溶液,则A表示
分别代表生产中的原料或产品,其中C为硫酸溶液,则A表示________ ,E表示________ 。
②阳极的电极反应式为________ 。
(4)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中 发生催化氧化的反应为
发生催化氧化的反应为 。若在
。若在 、
、 条件下,往一恒容密闭容器中通入
条件下,往一恒容密闭容器中通入 和
和 的混合气体
的混合气体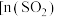 :
: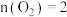 :
: ,测得容器内总压强与反应时间的关系如图所示。
,测得容器内总压强与反应时间的关系如图所示。
①图中A点时, 的转化率为
的转化率为________ 。
②在其他条件不变的情况下,测得 时压强的变化曲线如图2所示,则C点的正反应速率
时压强的变化曲线如图2所示,则C点的正反应速率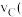 正
正 与A点的逆反应速率
与A点的逆反应速率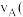 逆
逆 的大小关系为
的大小关系为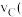 正
正
________  填“
填“ ”“
”“ ”或“
”或“ ”
”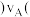 逆
逆 。
。
③图中B点的压强平衡常数
________ 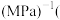 用平衡分压代表平衡浓度计算,分压
用平衡分压代表平衡浓度计算,分压 总压
总压 物质的量分数
物质的量分数 。
。
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质
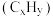 催化还原尾气中的NO气体,该过程的化学方程式为
催化还原尾气中的NO气体,该过程的化学方程式为(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。经研究发现将煤炭在
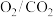 的气氛下燃烧,能够降低煤炭燃烧时NO的排放,主要反应为
的气氛下燃烧,能够降低煤炭燃烧时NO的排放,主要反应为 。
。已知:①

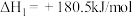
②
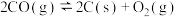
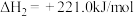
③
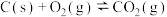
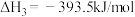
则反应
 的
的
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的
 溶液进行电解,其中阴、阳膜组合电解装置如图所示,电极材料为石墨。
溶液进行电解,其中阴、阳膜组合电解装置如图所示,电极材料为石墨。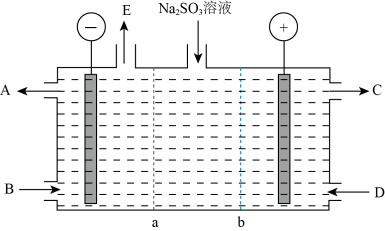
①
 表示
表示 填“阴离子”或“阳离子”
填“阴离子”或“阳离子” 交换膜。
交换膜。 分别代表生产中的原料或产品,其中C为硫酸溶液,则A表示
分别代表生产中的原料或产品,其中C为硫酸溶液,则A表示②阳极的电极反应式为
(4)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中
 发生催化氧化的反应为
发生催化氧化的反应为 。若在
。若在 、
、 条件下,往一恒容密闭容器中通入
条件下,往一恒容密闭容器中通入 和
和 的混合气体
的混合气体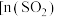 :
: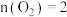 :
: ,测得容器内总压强与反应时间的关系如图所示。
,测得容器内总压强与反应时间的关系如图所示。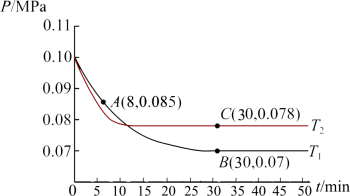
①图中A点时,
 的转化率为
的转化率为②在其他条件不变的情况下,测得
 时压强的变化曲线如图2所示,则C点的正反应速率
时压强的变化曲线如图2所示,则C点的正反应速率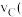 正
正 与A点的逆反应速率
与A点的逆反应速率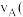 逆
逆 的大小关系为
的大小关系为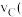 正
正
 填“
填“ ”“
”“ ”或“
”或“ ”
”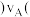 逆
逆 。
。③图中B点的压强平衡常数

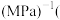 用平衡分压代表平衡浓度计算,分压
用平衡分压代表平衡浓度计算,分压 总压
总压 物质的量分数
物质的量分数 。
。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为: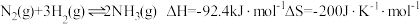
回答下列问题:
(1)合成氨反应在常温下___________ (填“能”或“不能”)自发。
(2)___________ 温(填“高”或“低”,下同)有利于提高反应速率,___________ 温有利于提高平衡转化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用 。
。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
(3)方案二: 复合催化剂。
复合催化剂。
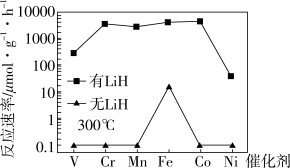
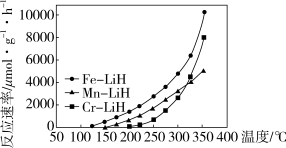
下列说法正确的是___________ 。
a. 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高
b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为: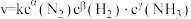 ,根据表中数据,
,根据表中数据,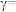
___________ ;
在合成氨过程中,需要不断分离出氨的原因为___________ 。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
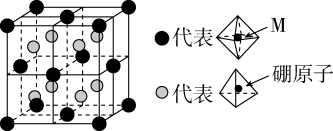
(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为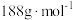 ,则M元素为
,则M元素为___________ (填元素符号);在该化合物中,M离子的价电子排布式为___________ 。
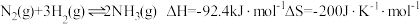
回答下列问题:
(1)合成氨反应在常温下
(2)
 。
。针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
(3)方案二:
 复合催化剂。
复合催化剂。

下列说法正确的是
a.
 时,复合催化剂比单一催化剂效率更高
时,复合催化剂比单一催化剂效率更高b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为:
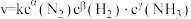 ,根据表中数据,
,根据表中数据,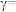
| 实验 | 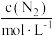 | 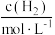 |  | 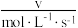 |
| 1 | m | n | p | q |
| 2 | 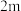 | n | p |  |
| 3 | m | n |  | 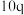 |
| 4 | m |  | p | 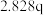 |
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为
 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为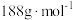 ,则M元素为
,则M元素为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】以活性炭为催化剂,可以将工业废气中的SO2催化氧化变为硫酸,进而制得各种硫酸盐,如硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]等。
(1)研究表明,SO2在活性炭上催化氧化的反应机理可以表示为(*标记的为吸附状态)
Ⅰ.二氧化硫的吸附:SO2(g) SO2* ΔH1=a kJ·mol-1
SO2* ΔH1=a kJ·mol-1
Ⅱ.氧气的吸附:O2(g) 2O* ΔH2=b kJ·mol-1
2O* ΔH2=b kJ·mol-1
Ⅲ.三氧化硫的氧化:SO2*+O*=SO3* ΔH3=c kJ·mol-1
Ⅳ.三氧化硫的脱附:SO3* SO3(g) ΔH4=d kJ·mol-1
SO3(g) ΔH4=d kJ·mol-1
根据上述反应机理,写出SO2在活性炭上催化氧化的热化学方程式____ 。
(2)以硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为原料通过下列流程可以制备晶体A。

①已知25 ℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq) [Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16。某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol·L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:
[Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16。某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol·L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:____ 。
②某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.910 0 g,干燥脱水至恒重,残留物质量为4.370 0 g;
步骤2:准确称取A样品4.910 0 g置于锥形瓶中,加入足量的3.000 mol·L-1 H2SO4溶液和适量蒸馏水,用0.500 0 mol·L-1 KMnO4溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为24.00 mL;(C2O42-+MnO4-+H+→CO2↑+Mn2++H2O)
步骤3:将步骤1所得固体溶于水,加入铁粉0.280 0 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程)。_____________
(1)研究表明,SO2在活性炭上催化氧化的反应机理可以表示为(*标记的为吸附状态)
Ⅰ.二氧化硫的吸附:SO2(g)
 SO2* ΔH1=a kJ·mol-1
SO2* ΔH1=a kJ·mol-1Ⅱ.氧气的吸附:O2(g)
 2O* ΔH2=b kJ·mol-1
2O* ΔH2=b kJ·mol-1Ⅲ.三氧化硫的氧化:SO2*+O*=SO3* ΔH3=c kJ·mol-1
Ⅳ.三氧化硫的脱附:SO3*
 SO3(g) ΔH4=d kJ·mol-1
SO3(g) ΔH4=d kJ·mol-1根据上述反应机理,写出SO2在活性炭上催化氧化的热化学方程式
(2)以硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为原料通过下列流程可以制备晶体A。

①已知25 ℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)
 [Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16。某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol·L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:
[Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16。某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol·L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:②某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.910 0 g,干燥脱水至恒重,残留物质量为4.370 0 g;
步骤2:准确称取A样品4.910 0 g置于锥形瓶中,加入足量的3.000 mol·L-1 H2SO4溶液和适量蒸馏水,用0.500 0 mol·L-1 KMnO4溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为24.00 mL;(C2O42-+MnO4-+H+→CO2↑+Mn2++H2O)
步骤3:将步骤1所得固体溶于水,加入铁粉0.280 0 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程)。
您最近一年使用:0次
【推荐1】NO的治理是当前生态环境保护中的重要课题之一。
I.电化学技术
(1)利用固体氧化物电解池可将NO直接转化为N2,实际应用中常将若干个电化学还原器结构单元组装在一起,形成电堆,以提高NO的去除效率。
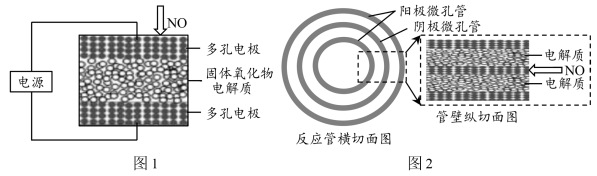
①纽扣式电化学还原器结构单元(其装置如图1所示)可叠加组装成电堆使用。电解时,阴极发生的电极反应式为_______ 。
②长管式电化学还原器结构单元(其剖面结构如图2所示)采用阴极微孔管作支撑,在管内外壁各设置一个对称的阳极微孔管,阴阳极管壁之间填充有固体氧化物电解质,使用时常将该结构单元组装成蜂窝状电堆。当电堆体积一定时,相比于纽扣式反应器,长管式反应器的优点是_______ 。
II.NH3-SCR技术
(2)Cu基催化剂是NH3-SCR技术脱除NO中性能较为优异的新型催化剂,但烟气中的SO2会造成Cu基催化剂的催化性能下降。加入CeO2(基态Ce原子核外电子排布式为[Xe]4f15d16s2)可抑制SO2对Cu基催化剂的影响,其作用机理如图3所示(含Ce化合物的比例系数均未标定)。
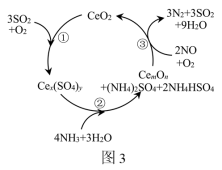
①从整个反应机理来看,总反应中起还原作用的物质是_______ (填化学式)。
②在上述反应机理图中,CemOn的化学式为_______ 。
(3)将3%NO、6%NH3、21%O2和70%N2的混合气体(N2为平衡气)以一定流速通过装有Cu基催化剂的反应器,NO去除率随反应温度的变化曲线如图4所示。
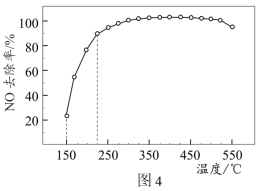
①在150-225°C范围内,NO去除率随温度的升高而迅速上升的原因是_______ 。
②燃煤烟气中伴有一定浓度的HCl气体,它会造成NO去除率下降,其原因可能是_______ 。
I.电化学技术
(1)利用固体氧化物电解池可将NO直接转化为N2,实际应用中常将若干个电化学还原器结构单元组装在一起,形成电堆,以提高NO的去除效率。

①纽扣式电化学还原器结构单元(其装置如图1所示)可叠加组装成电堆使用。电解时,阴极发生的电极反应式为
②长管式电化学还原器结构单元(其剖面结构如图2所示)采用阴极微孔管作支撑,在管内外壁各设置一个对称的阳极微孔管,阴阳极管壁之间填充有固体氧化物电解质,使用时常将该结构单元组装成蜂窝状电堆。当电堆体积一定时,相比于纽扣式反应器,长管式反应器的优点是
II.NH3-SCR技术
(2)Cu基催化剂是NH3-SCR技术脱除NO中性能较为优异的新型催化剂,但烟气中的SO2会造成Cu基催化剂的催化性能下降。加入CeO2(基态Ce原子核外电子排布式为[Xe]4f15d16s2)可抑制SO2对Cu基催化剂的影响,其作用机理如图3所示(含Ce化合物的比例系数均未标定)。

①从整个反应机理来看,总反应中起还原作用的物质是
②在上述反应机理图中,CemOn的化学式为
(3)将3%NO、6%NH3、21%O2和70%N2的混合气体(N2为平衡气)以一定流速通过装有Cu基催化剂的反应器,NO去除率随反应温度的变化曲线如图4所示。

①在150-225°C范围内,NO去除率随温度的升高而迅速上升的原因是
②燃煤烟气中伴有一定浓度的HCl气体,它会造成NO去除率下降,其原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】近年来,全球丙烯需求快速增长,研究丙烷制丙烯有着重要的意义。相关反应有:
反应Ⅰ(直接脱氢):
反应Ⅱ(氧化脱氢):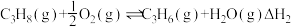
反应Ⅲ( 催化氧化
催化氧化 脱氢)机理:
脱氢)机理: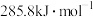 ,
,
 (l)蒸发吸热
(l)蒸发吸热 ;丙烷直接催化脱氢容易造成积碳,降低催化剂的稳定性,回答下列问题:
;丙烷直接催化脱氢容易造成积碳,降低催化剂的稳定性,回答下列问题:
(1)反应Ⅱ的焓变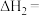
_______  。
。
(2)反应Ⅲ的化学方程式为_______ ;与直接脱氢相比,用 氧化
氧化 脱氢制丙烯的优点是
脱氢制丙烯的优点是_______ 。
(3)在 、
、 反应条件下,将气体物质的量比为
反应条件下,将气体物质的量比为 的混合气进行直接脱氢反应(反应Ⅰ)。
的混合气进行直接脱氢反应(反应Ⅰ)。
①从平衡移动的角度判断,x越小,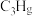 平衡转化率
平衡转化率_______ (填“越大”“越小”或“不变”),原因是_______ 。
②当 时,反应经过
时,反应经过 达到平衡,此时混合气中
达到平衡,此时混合气中 与
与 的分压相等,生成
的分压相等,生成 的平均速率为
的平均速率为_______  ,
, 平衡转化率为
平衡转化率为_______ 。
③ ,该反应平衡常数
,该反应平衡常数
_______  (以分压表示,分压
(以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
(4)我国学者结合实验与计算机模拟结果,研究了反应Ⅱ丙烷在含六方氮化硼固体催化剂的表面氧化脱氢的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用*号表示,反应历程中决速步骤能垒为_______  ,图示反应历程之后可能发生的反应为
,图示反应历程之后可能发生的反应为_______ 。 ,在含六方氮化硼固体催化剂的刚性密闭容器中依次通入
,在含六方氮化硼固体催化剂的刚性密闭容器中依次通入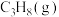 和
和 ,固定
,固定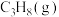 的分压恒定为
的分压恒定为 不变,实验测得氧气分压对反应速率的影响如图所示,随氧气分压增大,反应速率的增加程度明显减小,可能的原因为
不变,实验测得氧气分压对反应速率的影响如图所示,随氧气分压增大,反应速率的增加程度明显减小,可能的原因为_______ 。
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):
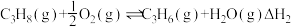
反应Ⅲ(
 催化氧化
催化氧化 脱氢)机理:
脱氢)机理: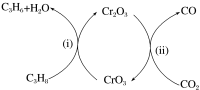
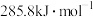 ,
,
 (l)蒸发吸热
(l)蒸发吸热 ;丙烷直接催化脱氢容易造成积碳,降低催化剂的稳定性,回答下列问题:
;丙烷直接催化脱氢容易造成积碳,降低催化剂的稳定性,回答下列问题:(1)反应Ⅱ的焓变
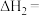
 。
。(2)反应Ⅲ的化学方程式为
 氧化
氧化 脱氢制丙烯的优点是
脱氢制丙烯的优点是(3)在
 、
、 反应条件下,将气体物质的量比为
反应条件下,将气体物质的量比为 的混合气进行直接脱氢反应(反应Ⅰ)。
的混合气进行直接脱氢反应(反应Ⅰ)。①从平衡移动的角度判断,x越小,
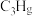 平衡转化率
平衡转化率②当
 时,反应经过
时,反应经过 达到平衡,此时混合气中
达到平衡,此时混合气中 与
与 的分压相等,生成
的分压相等,生成 的平均速率为
的平均速率为 ,
, 平衡转化率为
平衡转化率为③
 ,该反应平衡常数
,该反应平衡常数
 (以分压表示,分压
(以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。(4)我国学者结合实验与计算机模拟结果,研究了反应Ⅱ丙烷在含六方氮化硼固体催化剂的表面氧化脱氢的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用*号表示,反应历程中决速步骤能垒为
 ,图示反应历程之后可能发生的反应为
,图示反应历程之后可能发生的反应为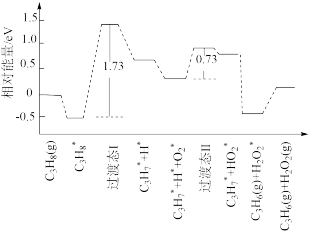
 ,在含六方氮化硼固体催化剂的刚性密闭容器中依次通入
,在含六方氮化硼固体催化剂的刚性密闭容器中依次通入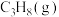 和
和 ,固定
,固定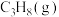 的分压恒定为
的分压恒定为 不变,实验测得氧气分压对反应速率的影响如图所示,随氧气分压增大,反应速率的增加程度明显减小,可能的原因为
不变,实验测得氧气分压对反应速率的影响如图所示,随氧气分压增大,反应速率的增加程度明显减小,可能的原因为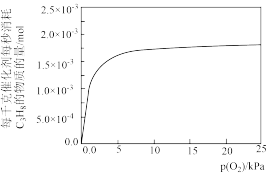
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一
已知: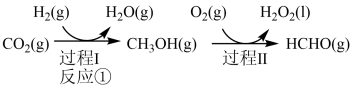
反应②: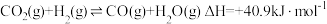
反应③:
(1)反应①: 的
的
_______ 。
(2)反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
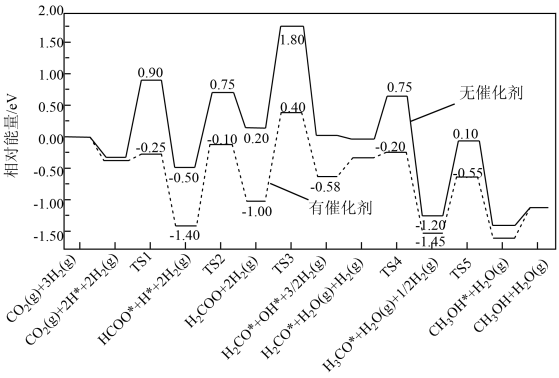
该反应历程中,使用催化剂条件下的决速步骤的反应方程式为:_______ 。
(3)某研究小组将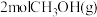 通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,
通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,
_______ ; 的转化率为:
的转化率为:_______ 。
(4)某研究小组采用上述催化剂,向密闭容器中通入 和
和 ,只发生反应①和反应②,在不同条件下达到平衡。其中,在
,只发生反应①和反应②,在不同条件下达到平衡。其中,在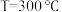 下甲醇的物质的量分数
下甲醇的物质的量分数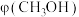 随压强P的变化、在
随压强P的变化、在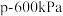 下
下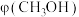 随温度T的变化,如图所示。
随温度T的变化,如图所示。
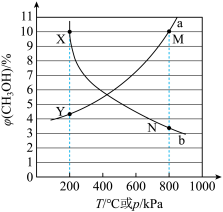
①Y点对应的温度和压强为_______ ℃、_______ kPa。
②M点时容器中 为
为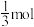 ,CO为
,CO为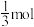 ,反应①的压强平衡常数
,反应①的压强平衡常数
_______  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
③图中M点的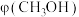 高于N点的原因是
高于N点的原因是_______ 。
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一
人工合成淀粉(节选途径见图)中的重要反应之一已知:
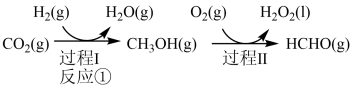
反应②:
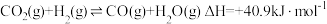
反应③:

(1)反应①:
 的
的
(2)反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。

该反应历程中,使用催化剂条件下的决速步骤的反应方程式为:
(3)某研究小组将
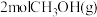 通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,
通入2L的刚性密闭容器内,只发生反应③,5分钟后容器压强变为原来的2.5倍,则这段时间内,
 的转化率为:
的转化率为:(4)某研究小组采用上述催化剂,向密闭容器中通入
 和
和 ,只发生反应①和反应②,在不同条件下达到平衡。其中,在
,只发生反应①和反应②,在不同条件下达到平衡。其中,在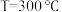 下甲醇的物质的量分数
下甲醇的物质的量分数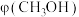 随压强P的变化、在
随压强P的变化、在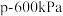 下
下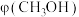 随温度T的变化,如图所示。
随温度T的变化,如图所示。
①Y点对应的温度和压强为
②M点时容器中
 为
为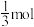 ,CO为
,CO为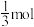 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。③图中M点的
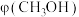 高于N点的原因是
高于N点的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】气态烯烃广泛用于塑料、纤维、洗涤剂等的合成。中科院某研究所在丙烷脱氢反应制备丙烯的条件控制方面进行了深入地研究。
(1)已知:H2(g)、C3H6(g)、C3H8(g)的燃烧热(∆H)分别为-285.8kJ·mol-1、-2058kJ·mol-1、-2219.9kJ·mol-1。计算:C3H8(g)⇌C3H6(g)+H2(g) ∆H=____ kJ·mol-1,常温下该反应的∆S=+0.1kJ·mol-1·K-1,则常温下该反应____ (填“能”或“不能”)自发进行。
(2)某种氧化硼催化剂(BOS)催化丙烷脱氢制丙烯的反应路径如图一,反应结果测定如图二。
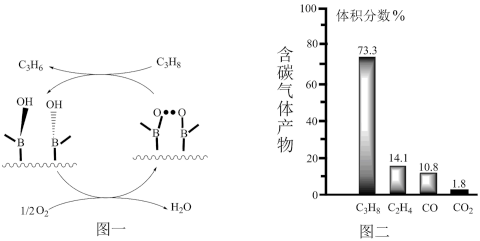
写出该路径主反应的化学方程式:__ ;结合图二,该反应路径可以提高丙烯产率的原因是___ 。
(3)在体积可变的密闭容器中充入由3mol丙烷分别在3.0×104Pa、1.2×105Pa时发生脱氢反应。测得不同温度下的平衡态中,丙烷、丙烯的物质的量分数变化关系如图所示:
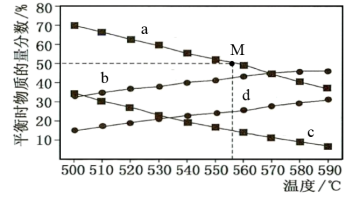
①1.2×105Pa时丙烯的物质的量分数随温度变化的关系曲线是____ 。
②下列叙述能说明此反应已达平衡状态的是____ 。
a.混合气体密度保持不变
b.C3H6和H2的浓度相等
c.相同时间断开和形成的碳氢键数目相同
d.混合气体的摩尔质量不再改变
③计算M点的平衡常数Kp=__ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知:H2(g)、C3H6(g)、C3H8(g)的燃烧热(∆H)分别为-285.8kJ·mol-1、-2058kJ·mol-1、-2219.9kJ·mol-1。计算:C3H8(g)⇌C3H6(g)+H2(g) ∆H=
(2)某种氧化硼催化剂(BOS)催化丙烷脱氢制丙烯的反应路径如图一,反应结果测定如图二。

写出该路径主反应的化学方程式:
(3)在体积可变的密闭容器中充入由3mol丙烷分别在3.0×104Pa、1.2×105Pa时发生脱氢反应。测得不同温度下的平衡态中,丙烷、丙烯的物质的量分数变化关系如图所示:

①1.2×105Pa时丙烯的物质的量分数随温度变化的关系曲线是
②下列叙述能说明此反应已达平衡状态的是
a.混合气体密度保持不变
b.C3H6和H2的浓度相等
c.相同时间断开和形成的碳氢键数目相同
d.混合气体的摩尔质量不再改变
③计算M点的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途,回答下列问题:
(1)写出砷的原子序数______________
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H2AsO4和单质硫,写出发生反应的化学方程式_____________________________________________ ;该反应需要在加压下进行,原因是 _______________________________________
(3)已知:As(s)+3/2H2(g)+2O2(g)=H3AsO4 (s) △H1
H2(g)+1/2O2(g)=H2O(l) △H2
2As(s)+5/2O2(g)=As2O5(s) △H3
则反应As2O5(s)+3H2O(l)=2H3AsO4 (s)的△H=________________________
(4)298K时,将20mL 3xmol·L-1Na3AsO3、20mL 3xmol·L-1I2和20mL NaOH溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-
(aq)+I2(aq)+2OH- AsO
AsO (aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
(aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
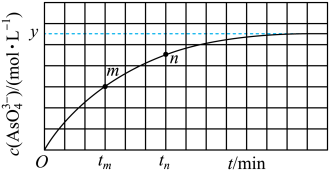
①下列可判断反应达到平衡的是______ (填标号).
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c. c(AsO )/c(AsO
)/c(AsO )不再变化 d.c(I-)=ymol·L-1
)不再变化 d.c(I-)=ymol·L-1
②tm时,v正______ v逆 ( 填“大于”“小于”或“等于”)
③tm时,v逆______ tn时v逆(填“大于”“小于”或“等于”),理由是 ____________________
④若平衡时溶液pH=14,则该反应的平衡常数K为______________
(1)写出砷的原子序数
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H2AsO4和单质硫,写出发生反应的化学方程式
(3)已知:As(s)+3/2H2(g)+2O2(g)=H3AsO4 (s) △H1
H2(g)+1/2O2(g)=H2O(l) △H2
2As(s)+5/2O2(g)=As2O5(s) △H3
则反应As2O5(s)+3H2O(l)=2H3AsO4 (s)的△H=
(4)298K时,将20mL 3xmol·L-1Na3AsO3、20mL 3xmol·L-1I2和20mL NaOH溶液混合,发生反应:AsO
 (aq)+I2(aq)+2OH-
(aq)+I2(aq)+2OH- AsO
AsO (aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
(aq)+2I-(aq)+H2O(l)溶液中c(AsO43-)与反应时间(t)的关系如图所示.
①下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c. c(AsO
 )/c(AsO
)/c(AsO )不再变化 d.c(I-)=ymol·L-1
)不再变化 d.c(I-)=ymol·L-1②tm时,v正
③tm时,v逆
④若平衡时溶液pH=14,则该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】已知在催化剂存在条件下,能发生如下反应:CO+H2O H2 +CO2 +Q
H2 +CO2 +Q
(1)该反应的平衡常数表达式为:___ 。在5L盛有固体催化剂(其体积可忽略不计)的密闭容器中,通入反应物,10s后,生成了氢气0.4g,则此10s内CO的平均反应速率为v(CO)=__ 。
(2)在该密闭容器中,下列叙述可以说明反应已经达到平衡状态的是__ 。
A.若容器体积不变,在一定温度下压强达到恒定
B.CO2的生成速率与H2O蒸气的生成速率之比为1:1
C.CO、H2O、H2、CO在容器中的物质的量浓度保持不变
D.反应体系中混合物的平均摩尔质量保持不变
(3)在上述反应达平衡状态后,分别改变条件,请完成下列两张图:
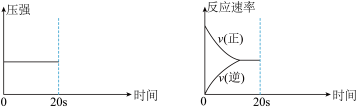
A.在第20s时将容器体积缩小至原来的一半后压强变化图___
B.在第20s时,向容器中注入少量的CO气体后正逆反应速率变化图___
(4)某化学小组在做澄清石灰水导电性实验时,发现石墨两极产生气体,溶液出现白色浑浊,请根据已有知识推测,两极产生的气体可能是__ ,白色浑浊是___ 。为验证白色浑浊物的成分,该同学向白色浑浊液体中加入盐酸,没有观察到气泡产生。他们继续实验,将浑浊的液体倒入密闭容器,通过注射器注入稀盐酸,并用二氧化碳传感器来测定装置中二氧化碳含量的变化,装置和图象如图所示:
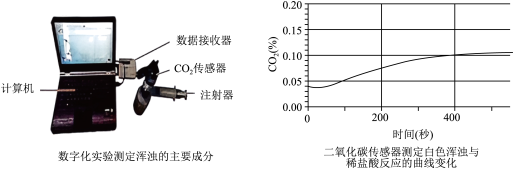
请解释上述现象并分析产生白色浑浊可能的原因___ 。
 H2 +CO2 +Q
H2 +CO2 +Q(1)该反应的平衡常数表达式为:
(2)在该密闭容器中,下列叙述可以说明反应已经达到平衡状态的是
A.若容器体积不变,在一定温度下压强达到恒定
B.CO2的生成速率与H2O蒸气的生成速率之比为1:1
C.CO、H2O、H2、CO在容器中的物质的量浓度保持不变
D.反应体系中混合物的平均摩尔质量保持不变
(3)在上述反应达平衡状态后,分别改变条件,请完成下列两张图:

A.在第20s时将容器体积缩小至原来的一半后压强变化图
B.在第20s时,向容器中注入少量的CO气体后正逆反应速率变化图
(4)某化学小组在做澄清石灰水导电性实验时,发现石墨两极产生气体,溶液出现白色浑浊,请根据已有知识推测,两极产生的气体可能是

请解释上述现象并分析产生白色浑浊可能的原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】为了缓解温空效应,科学家提出了多种回收和利用CO2的方案。
(1)方案1: 利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 =+113. 4kJ/mol
请写出由FeO制备H2的热化学方程式_________________ 。
方案2: 利用CO2制备CH4
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应: CO2(g)+4H2(g) CH4(g)+ 2H2O(g) ΔH4,混合气体中CH4的浓度与反应时间的关系如图所示。
CH4(g)+ 2H2O(g) ΔH4,混合气体中CH4的浓度与反应时间的关系如图所示。
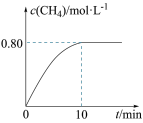
(2)① 从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=_________________ 。
② 300℃时,反应的平衡常数K=_______________ 。
③ 300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g)。则v正____________ v逆(填“>”“<”或“=" )
(3)下列有关说法正确的是(填序号)_______________ 。
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.300℃时,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度等于1.6mo/L
D.每断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
E.达到平衡后,分离出水蒸气,既能加快反应速率又能使平衡正方向移动
(4)已知200℃时,该反应的平衡常数K=64.8(L/mol)2。则ΔH4________ 0(填“>”“<”或“=”)。
方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:(假设开始时两极的质量相等)
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:(假设开始时两极的质量相等)

(5)①放电时,正极的电极反应式为_______________ 。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mole-时,两极的质量差为_____ g。
(1)方案1: 利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ΔH1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) ΔH2 =+113. 4kJ/mol
请写出由FeO制备H2的热化学方程式
方案2: 利用CO2制备CH4
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2发生反应: CO2(g)+4H2(g)
 CH4(g)+ 2H2O(g) ΔH4,混合气体中CH4的浓度与反应时间的关系如图所示。
CH4(g)+ 2H2O(g) ΔH4,混合气体中CH4的浓度与反应时间的关系如图所示。
(2)① 从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=
② 300℃时,反应的平衡常数K=
③ 300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g)。则v正
(3)下列有关说法正确的是(填序号)
A.容器内密度不变,说明反应达到平衡状态
B.容器内压强不变,说明反应达到平衡状态
C.300℃时,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度等于1.6mo/L
D.每断开2molC=O键的同时断开4molC-H键,说明反应达到平衡状态
E.达到平衡后,分离出水蒸气,既能加快反应速率又能使平衡正方向移动
(4)已知200℃时,该反应的平衡常数K=64.8(L/mol)2。则ΔH4
方案3:利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:(假设开始时两极的质量相等)
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:(假设开始时两极的质量相等)
(5)①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mole-时,两极的质量差为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】科学家一直致力于“人工固氮”的新方法研究。
I.目前合成氨技术原理为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。
(1)在一定体积的容器中发生上述反应,下列描述中能说明该反应已达平衡的是_______ 。
(2)673K、30MPa下,向容积为2.0L的恒容密闭容器中充入080molN2和1.60molH2,反应3分钟达到平衡时,NH3的体积分数为20%。
①该条件下反应:N2(g)+3H2(g) 2NH3(g)的平衡常数K=
2NH3(g)的平衡常数K=_____ (精确到小数点后一位);K值越大,表明反应达到平衡时_______ 。
A. H2的转化率一定越高
B.NH3的浓度一定越大
C.正反应进行得越完全
D.化学反应速率越大
②若达平衡后再向该容器中充入0.40molN2和0.40molNH3,该平衡将______ (填“向正反应方向移动”、“向逆反应方向移动”或“不移动”)。
Ⅱ.根据“人工固氮”的最新研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2(g)+6H2O(1) 4NH3(g)+3O2(g) △H=akJ/mol。进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如表:
4NH3(g)+3O2(g) △H=akJ/mol。进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如表:
(3)此合成反应的a______ 0;△S______ 0,(填“>”、“<”或“=”)。
(4)已知(K为平衡常数):N2(g)+3H2(g) 2NH3(g) K1,2H2(g)+O2(g)=2H2O(1) K2,则N2(g)+3H2O(1)=2NH3(g)+
2NH3(g) K1,2H2(g)+O2(g)=2H2O(1) K2,则N2(g)+3H2O(1)=2NH3(g)+ O2(g)的K=
O2(g)的K=______ (用K1、K2表示)。
I.目前合成氨技术原理为:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。(1)在一定体积的容器中发生上述反应,下列描述中能说明该反应已达平衡的是
| A.容器内气体的平均摩尔质量保持不变 |
| B.2v(NH3)正=v(N2)逆 |
| C.容器中气体的压强保持不变 |
| D.N2、H2、NH3的物质的量之比为1∶3∶2 |
(2)673K、30MPa下,向容积为2.0L的恒容密闭容器中充入080molN2和1.60molH2,反应3分钟达到平衡时,NH3的体积分数为20%。
①该条件下反应:N2(g)+3H2(g)
 2NH3(g)的平衡常数K=
2NH3(g)的平衡常数K=A. H2的转化率一定越高
B.NH3的浓度一定越大
C.正反应进行得越完全
D.化学反应速率越大
②若达平衡后再向该容器中充入0.40molN2和0.40molNH3,该平衡将
Ⅱ.根据“人工固氮”的最新研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2(g)+6H2O(1)
 4NH3(g)+3O2(g) △H=akJ/mol。进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如表:
4NH3(g)+3O2(g) △H=akJ/mol。进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如表:| T/K | 303 | 313 | 323 |
| NH3的生成量/(10mol) | 4.8 | 5.9 | 6.0 |
(3)此合成反应的a
(4)已知(K为平衡常数):N2(g)+3H2(g)
 2NH3(g) K1,2H2(g)+O2(g)=2H2O(1) K2,则N2(g)+3H2O(1)=2NH3(g)+
2NH3(g) K1,2H2(g)+O2(g)=2H2O(1) K2,则N2(g)+3H2O(1)=2NH3(g)+ O2(g)的K=
O2(g)的K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。甲烷重整是提高甲烷利用率的重要方式。
回答下列问题:
(1)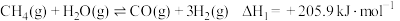 ①
①
 ②
②
写出 与
与 反应生成CO和
反应生成CO和 的热化学方程式:
的热化学方程式:_______ 。
(2)高温下,在1L密闭容器中通入1mol甲烷,发生如下反应: 。反应在初期阶段的速率方程为
。反应在初期阶段的速率方程为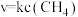 ,其中
,其中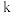 为反应速率常数。
为反应速率常数。
①设反应开始时的反应速率为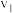 ,甲烷的转化率为
,甲烷的转化率为 时的反应速率为
时的反应速率为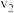 ,则
,则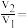
_______ 。
②对于处于初期阶段的该反应,下列说法正确的是_______ (填字母)。
A.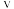 与甲烷浓度成正比
与甲烷浓度成正比
B.压强不变时,反应到达平衡状态
C.乙烷的生成速率逐渐增大
D.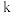 与温度无关
与温度无关
③平衡时,再通入1 mol甲烷,则反应的平衡常数K_______ (填“增大”“减小”或“不变”,下同),甲烷的转化率
_______ 。
(3) 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
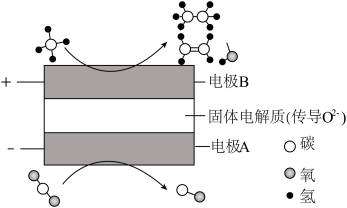
当在某电极上生成的两种有机物物质的量之比为1:1时,该电极上的电极反应式为_______ 。 和
和 的物质的量比为
的物质的量比为_______ 。
(4)我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步: 催化裂解生成
催化裂解生成 和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如
和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如 ;第二步:碳(或碳氢物种)和
;第二步:碳(或碳氢物种)和 反应生成
反应生成 和
和 ,如
,如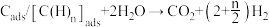 ,反应过程和能量变化残图如下:
,反应过程和能量变化残图如下:
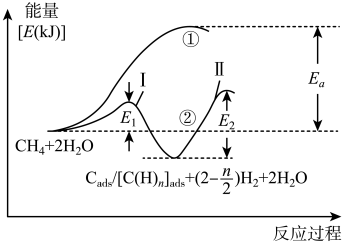
判断_______ (填序号)过程加入催化剂,原因是_______ 。控制整个过程②反应速率的是第Ⅱ步,其原因为_______ 。
回答下列问题:
(1)
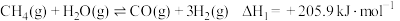 ①
① ②
②写出
 与
与 反应生成CO和
反应生成CO和 的热化学方程式:
的热化学方程式:(2)高温下,在1L密闭容器中通入1mol甲烷,发生如下反应:
 。反应在初期阶段的速率方程为
。反应在初期阶段的速率方程为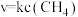 ,其中
,其中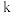 为反应速率常数。
为反应速率常数。①设反应开始时的反应速率为
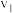 ,甲烷的转化率为
,甲烷的转化率为 时的反应速率为
时的反应速率为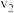 ,则
,则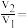
②对于处于初期阶段的该反应,下列说法正确的是
A.
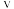 与甲烷浓度成正比
与甲烷浓度成正比B.压强不变时,反应到达平衡状态
C.乙烷的生成速率逐渐增大
D.
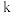 与温度无关
与温度无关③平衡时,再通入1 mol甲烷,则反应的平衡常数K

(3)
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
当在某电极上生成的两种有机物物质的量之比为1:1时,该电极上的电极反应式为
 和
和 的物质的量比为
的物质的量比为(4)我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步:
 催化裂解生成
催化裂解生成 和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如
和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如 ;第二步:碳(或碳氢物种)和
;第二步:碳(或碳氢物种)和 反应生成
反应生成 和
和 ,如
,如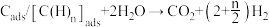 ,反应过程和能量变化残图如下:
,反应过程和能量变化残图如下:
判断
您最近一年使用:0次



