亚铁氰化钾{ }在医药工业用作凝聚剂,能达到理想的除杂工艺,提高药品质量。回答下列问题:
}在医药工业用作凝聚剂,能达到理想的除杂工艺,提高药品质量。回答下列问题:
(1)基态铁原子的价电子排布图为_______ ;与K同周期且基态原子最外层与基态K原子具有相同未成对电子数的元素有种_______ (不包括K元素)。
(2)已知反应 。
。
①化学方程式中涉及到的第二周期元素第一电离能由大到小的顺序为_______ (用元素符号表示)。
② 中N原子的杂化方式为
中N原子的杂化方式为_______ ; 的空间构型为
的空间构型为_______ 。
③写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_______ 。
④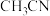 能与水混溶的原因为
能与水混溶的原因为_______ 。
(3)铁酸铋( )属于多铁材料的一种,具有铁电性和反铁磁性,并伴随弱的铁磁性。其晶胞结构如图所示。
)属于多铁材料的一种,具有铁电性和反铁磁性,并伴随弱的铁磁性。其晶胞结构如图所示。
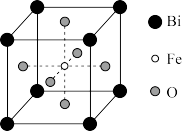
①距离O最近且等距离的Bi有_______ 个。
②若该晶胞的密度为 ,
, 为阿伏加德罗常数的值,则距离Fe最近的O构成的图形的边长为
为阿伏加德罗常数的值,则距离Fe最近的O构成的图形的边长为_______ pm(用含 、
、 的代数式表示)。
的代数式表示)。
 }在医药工业用作凝聚剂,能达到理想的除杂工艺,提高药品质量。回答下列问题:
}在医药工业用作凝聚剂,能达到理想的除杂工艺,提高药品质量。回答下列问题:(1)基态铁原子的价电子排布图为
(2)已知反应
 。
。①化学方程式中涉及到的第二周期元素第一电离能由大到小的顺序为
②
 中N原子的杂化方式为
中N原子的杂化方式为 的空间构型为
的空间构型为③写出一种与
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:④
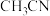 能与水混溶的原因为
能与水混溶的原因为(3)铁酸铋(
 )属于多铁材料的一种,具有铁电性和反铁磁性,并伴随弱的铁磁性。其晶胞结构如图所示。
)属于多铁材料的一种,具有铁电性和反铁磁性,并伴随弱的铁磁性。其晶胞结构如图所示。
①距离O最近且等距离的Bi有
②若该晶胞的密度为
 ,
, 为阿伏加德罗常数的值,则距离Fe最近的O构成的图形的边长为
为阿伏加德罗常数的值,则距离Fe最近的O构成的图形的边长为 、
、 的代数式表示)。
的代数式表示)。
2022·广东茂名·模拟预测 查看更多[5]
广东省茂名市五校联盟2021-2022学年高三下学期第三次联考化学试卷(已下线)专项17 物质结构与性质综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)押广东卷化学第20题 物质结构与性质综合题-备战2022年高考化学临考题号押题(广东卷)黑龙江省哈尔滨市第九中学校2022届高三考前理科综合压轴卷化学试题湖南省岳阳市岳阳县2021-2022学年高三上学期入学考试化学试题
更新时间:2022-03-02 18:44:30
|
相似题推荐
【推荐1】合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为_______ ,占据最高能级电子的电子云轮廓图为_______ 形。
② 分子中,与N原子相连的H显正电性,N、H电负性大小顺序为
分子中,与N原子相连的H显正电性,N、H电负性大小顺序为_______ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是_______ 。
②比较Mg、Ca第一电离能的大小:_______ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:_______ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为_______ ,铁在元素周期表中的位置_______ 。
②比较 与
与 的半径大小关系:
的半径大小关系: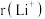
_______  (填“>”或“<”)。
(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②
 分子中,与N原子相连的H显正电性,N、H电负性大小顺序为
分子中,与N原子相连的H显正电性,N、H电负性大小顺序为(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较
 与
与 的半径大小关系:
的半径大小关系: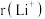
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】镍具有良好的导磁性和可塑性,主要用于制作合金及催化剂。请回答下列问题
(1)基态镍原子的价电子排布图为____ ,同周期元素中基态原子与镍具有相同未成对电子的还有____ 种。
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为___ 三种组成元素按电负性由大到小的顺序为____ 。
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为____ ,写出与SO42-互为等电子体的一种分子和一种离子的化学式____ ,____ ;[Ni(
NH3)4]SO4中H-N-H键之间的夹角___ (填“>”“<”或“=”)NH3分子中H-N-H键之间的夹角。
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的____ 体空隙中,其空隙的填充率为____ 。
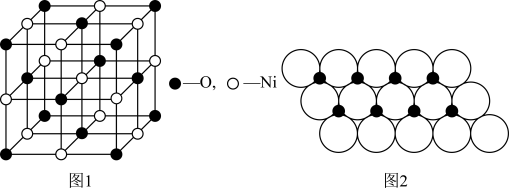
(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为___ g。(用a、NA表示)
(1)基态镍原子的价电子排布图为
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为
NH3)4]SO4中H-N-H键之间的夹角
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的

(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为
您最近一年使用:0次
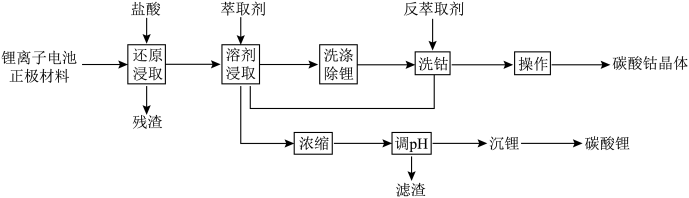
【推荐3】废旧锂离子电池的资源化利用是锂离子电池工业可持续发展的有效途径,一种废旧锂离子电池湿法回收钴和锂的工艺流程如图所示。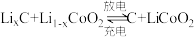 。
。
②25℃时,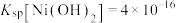 ;当溶液中离子浓度小于
;当溶液中离子浓度小于 时认为沉淀完全。
时认为沉淀完全。
③ 和
和 的溶解度如表所示。
的溶解度如表所示。
回答下列问题:
(1)基态Cu原子的价层电子排布图为___________ 。
(2)“还原浸取”时发生反应的化学方程式为___________ 。
(3)“溶剂浸取”的目的是将 、
、 与
与 、
、 分开(锂离子不与萃取剂作用),萃取原理为
分开(锂离子不与萃取剂作用),萃取原理为 ,参考下图判断应选择的萃取剂为
,参考下图判断应选择的萃取剂为___________ (填“P507”或“P204”),pH应控制在约___________ (“2~3”“4~5”或“6~7”)。___________ (填化学式);从溶液中获得硫酸钻晶体的操作为___________ 。
(5)25℃时,调
___________ 可以使 沉淀完全(已知:
沉淀完全(已知: )。
)。
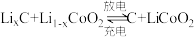 。
。②25℃时,
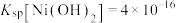 ;当溶液中离子浓度小于
;当溶液中离子浓度小于 时认为沉淀完全。
时认为沉淀完全。③
 和
和 的溶解度如表所示。
的溶解度如表所示。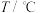 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
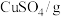 | 17.4 | 20.7 | 25.0 | 28.5 | 33.3 | 35.0 | 39.5 | 43.4 | 47.2 | 65.4 |
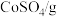 | 30.6 | 36.2 | 42.2 | 49.9 | 55.2 | 60.4 | 65.7 | 71.0 | 76.0 | 83.0 |
(1)基态Cu原子的价层电子排布图为
(2)“还原浸取”时发生反应的化学方程式为
(3)“溶剂浸取”的目的是将
 、
、 与
与 、
、 分开(锂离子不与萃取剂作用),萃取原理为
分开(锂离子不与萃取剂作用),萃取原理为 ,参考下图判断应选择的萃取剂为
,参考下图判断应选择的萃取剂为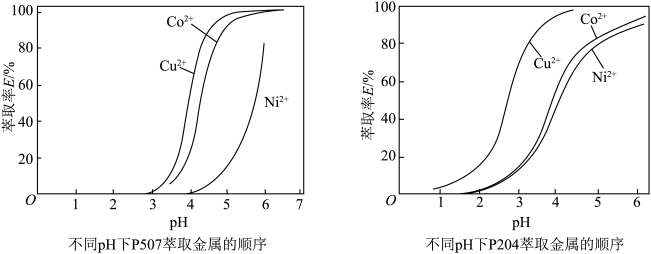
(5)25℃时,调

 沉淀完全(已知:
沉淀完全(已知: )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】选做[化学—物质结构与性质]氨是重要的化工原料,用途很广。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是____ (填元素名称)。
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有____ (填标号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有_______ 种(不含Cu)。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3= F3B—NH3。
①BF3和NH3分子的空间构型分别为_____ 、_____ 。
②晶体F3B—NH3中,B原子的杂化轨道类型为______ 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质易溶于水,在水溶液中以 和
和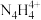 两种正四面体构型的离子存在。
两种正四面体构型的离子存在。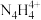 遇碱生成一种形似白磷的N4分子。
遇碱生成一种形似白磷的N4分子。

①下列相关说法中,正确的是_____ (填序号)。
a.N4是N2的同分异构体
b.1mol N4分解生成N2,形成了4mol π键
c.白磷的沸点比N4高,原因是P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键):___________ 。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3= F3B—NH3。
①BF3和NH3分子的空间构型分别为
②晶体F3B—NH3中,B原子的杂化轨道类型为
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质易溶于水,在水溶液中以
 和
和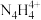 两种正四面体构型的离子存在。
两种正四面体构型的离子存在。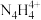 遇碱生成一种形似白磷的N4分子。
遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是
a.N4是N2的同分异构体
b.1mol N4分解生成N2,形成了4mol π键
c.白磷的沸点比N4高,原因是P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键):
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】Ⅰ.硫是一种重要的非金属元絭,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是___________ ,最高能级电子所在的原子轨道为___________ 形。
(2)①硫单质的一种结构为 ,S原子杂化方式为
,S原子杂化方式为___________ ; 分子的空间构型是
分子的空间构型是___________ 。
② 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是___________ 。
③比较沸点高低:
___________ (填“>”或“<”) ,并解释原因:
,并解释原因:___________ 。
(3) 晶胞如图所示:
晶胞如图所示:

①由图可知,每个 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有___________ 个。
②已知该晶胞密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为___________  。
。
Ⅱ.金属材料 、
、 、
、 等在工业生产和日常生活中有广泛的应用。某同学设计如下制备铜的配合物的实验,并对铜的化合物进行研究。已知铜离子的配位数通常为4。
等在工业生产和日常生活中有广泛的应用。某同学设计如下制备铜的配合物的实验,并对铜的化合物进行研究。已知铜离子的配位数通常为4。

(4) 试剂为
试剂为___________ 。
(5)目前,印刷电路板的腐蚀多采用碱氨蚀刻液(氯化铵和氨水的混合液),在空气中使电路板露出的铜以二氯四氨合铜的形式溶解下来,写出腐蚀的化学方程式___________ 。
(6)由上述实验能说明 、
、 与
与 形成蓝色配离子的稳定性强弱为:
形成蓝色配离子的稳定性强弱为:___________ >___________ (填配离子化学式)。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,S原子杂化方式为
,S原子杂化方式为 分子的空间构型是
分子的空间构型是②
 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是③比较沸点高低:

 ,并解释原因:
,并解释原因:(3)
 晶胞如图所示:
晶胞如图所示:
①由图可知,每个
 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有②已知该晶胞密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为 。
。Ⅱ.金属材料
 、
、 、
、 等在工业生产和日常生活中有广泛的应用。某同学设计如下制备铜的配合物的实验,并对铜的化合物进行研究。已知铜离子的配位数通常为4。
等在工业生产和日常生活中有广泛的应用。某同学设计如下制备铜的配合物的实验,并对铜的化合物进行研究。已知铜离子的配位数通常为4。
(4)
 试剂为
试剂为(5)目前,印刷电路板的腐蚀多采用碱氨蚀刻液(氯化铵和氨水的混合液),在空气中使电路板露出的铜以二氯四氨合铜的形式溶解下来,写出腐蚀的化学方程式
(6)由上述实验能说明
 、
、 与
与 形成蓝色配离子的稳定性强弱为:
形成蓝色配离子的稳定性强弱为:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】磷化硼是一种典型的超硬无机材料,常以BCl3、PH3为原料制备。回答下列问题:
(1)基态P原子与B原子中未成对电子数之比为___ 。
(2)与BC13分子互为等电子体的一种离子为___ (填化学式)。
(3)PH3分子的立体结构为___ ;PH3的沸点___ (填“高于”或“低于”)NH3,理由是___ 。
(4)BCl3、PCl3和PF3三种分子中键角由大到小的顺序为___ 。
(5)BCl3可转化为硼酸,硼酸为一元弱酸的原因是___ (用离子方程式表示)。
(6)磷化硼晶胞的示意图如图甲所示,其中实心球表示P原子,空心球表示B原子,晶胞中P原子空间堆积方式为___ 。已知磷化硼晶体的密度为ρg·cm-3,设阿伏加 德罗常数的值为NA,则晶胞中B原子与P原子间最短距离为___ pm。若磷化硼晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示P原子的投影),请在图乙中用实线圆圈画出B原子的投影位置___ (注意原子体积的相对大小)。

(1)基态P原子与B原子中未成对电子数之比为
(2)与BC13分子互为等电子体的一种离子为
(3)PH3分子的立体结构为
(4)BCl3、PCl3和PF3三种分子中键角由大到小的顺序为
(5)BCl3可转化为硼酸,硼酸为一元弱酸的原因是
(6)磷化硼晶胞的示意图如图甲所示,其中实心球表示P原子,空心球表示B原子,晶胞中P原子空间堆积方式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】硼元素的单质和化合物很多,我们可以利用所学知识认识和理解它们。
(1)硼元素位于元素周期表的__________ 区;硼元素的价电子排布式为_________ 。
(2)B、C、Si与H、O原子形成的单键和B、C、Si原子自成单键的键能如下表所示:
①自然界中硼主要以含氧化合物的形式存在的原因是_____________ 。
②类似于烷烃,B、Si也有一系列氢化物,但从物质数量角度看:硅烷<硼烷<烷烃。原因是_________ 。
③推测晶体B的晶体类型是__________ 。
(3)乙硼烷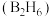 具有强还原性,它和氢化锂反应生成硼氢化锂
具有强还原性,它和氢化锂反应生成硼氢化锂 ,硼氢化锂常用于有机合成。
,硼氢化锂常用于有机合成。 由
由 和
和 构成。
构成。 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为_______ ; 中三种元素电负性由大到小的顺序是
中三种元素电负性由大到小的顺序是__________ (写元素符号)。
(4)氮化硼(BN)是一种重要的功能陶瓷材料。可通过下列反应得到:
①□内物质的空间构型为__________ 。
②在与石墨结构相似的六方氮化硼晶体中,晶体的层间距为a pm, 键键长为b pm,则六方氮化硼晶体的密度为
键键长为b pm,则六方氮化硼晶体的密度为__________  (用
(用 表示阿伏加 德罗常数的值)。
表示阿伏加 德罗常数的值)。

(1)硼元素位于元素周期表的
(2)B、C、Si与H、O原子形成的单键和B、C、Si原子自成单键的键能如下表所示:
| 化学键 |  |  | 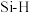 |  | 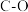 |  |  |  |  |
键能 | 389 | 411 | 318 | 561 | 358 | 452 | 293 | 346 | 222 |
②类似于烷烃,B、Si也有一系列氢化物,但从物质数量角度看:硅烷<硼烷<烷烃。原因是
③推测晶体B的晶体类型是
(3)乙硼烷
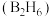 具有强还原性,它和氢化锂反应生成硼氢化锂
具有强还原性,它和氢化锂反应生成硼氢化锂 ,硼氢化锂常用于有机合成。
,硼氢化锂常用于有机合成。 由
由 和
和 构成。
构成。 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为 中三种元素电负性由大到小的顺序是
中三种元素电负性由大到小的顺序是(4)氮化硼(BN)是一种重要的功能陶瓷材料。可通过下列反应得到:

①□内物质的空间构型为
②在与石墨结构相似的六方氮化硼晶体中,晶体的层间距为a pm,
 键键长为b pm,则六方氮化硼晶体的密度为
键键长为b pm,则六方氮化硼晶体的密度为 (用
(用 表示阿伏加 德罗常数的值)。
表示阿伏加 德罗常数的值)。
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】3-氯靛红酸酐( )是重要的材料中间体,其制备流程图如下:
)是重要的材料中间体,其制备流程图如下:

已知:
(1)3-氯靛红酸酐的分子式为_____ ,苯环上碳原子的杂化方式为_____ ;
(2)有机物B的名称为_____ ,写出符合下列条件有机物B的所有同分异构体的结构简式_____ ;
a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
(3)该流程未采用甲苯直接硝化的方法制备有机物B,而是经由①、②、③三步反应进行制取,其目的是_____ ;
(4)⑥的反应类型是_____ ,⑥的主要目的是_____ ;
(5)⑧的反应试剂和条件为_____ ;F中含氧官能团的名称为_____ ;
(6)以有机物C为原料,在一定条件下制备含酰胺基聚合物的化学方程式_____ 。
 )是重要的材料中间体,其制备流程图如下:
)是重要的材料中间体,其制备流程图如下:
已知:

(1)3-氯靛红酸酐的分子式为
(2)有机物B的名称为
a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
(3)该流程未采用甲苯直接硝化的方法制备有机物B,而是经由①、②、③三步反应进行制取,其目的是
(4)⑥的反应类型是
(5)⑧的反应试剂和条件为
(6)以有机物C为原料,在一定条件下制备含酰胺基聚合物的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】铁、钴均为第四周期第Ⅷ族元素,它们的单质及化合物具有广泛用途。回答下列问题:
(1)基态Co2+中的未成对电子数为___ ;Fe和Co的第四电离能I4(Fe)___ I4(Co)(填“>”、“<”或“=”)。
(2)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为___ ;已知孤电子对与成键电子的排斥作用大于成键电子对与成键电子的排斥作用,试判断NH3分子与钴离子形成配合物后H—N—H键角___ (填“变大”、“变小”或“不变”)。
(3)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
①丙酮(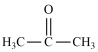 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是___ ,1mol丙酮分子中含有σ键的数目为___ 。
②C、H、O三种元素的电负性由小到大的顺序为___ 。
③乙醇的沸点高于丙酮,这是因为___ 。
(4)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示。
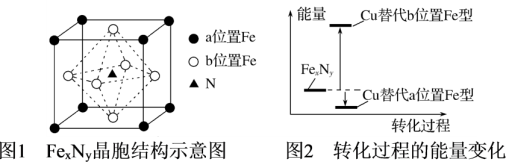
①该结构中单纯分析铁的堆积,其堆积方式为___ 。
②其中更稳定的Cu替代型产物的化学式为____ 。
③若更稳定的Cu替代型产物的密度为ρg/cm3,则该晶胞中相邻的两个Fe原子的距离为___ nm。
(1)基态Co2+中的未成对电子数为
(2)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为
(3)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
①丙酮(
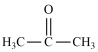 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是②C、H、O三种元素的电负性由小到大的顺序为
③乙醇的沸点高于丙酮,这是因为
(4)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示。

①该结构中单纯分析铁的堆积,其堆积方式为
②其中更稳定的Cu替代型产物的化学式为
③若更稳定的Cu替代型产物的密度为ρg/cm3,则该晶胞中相邻的两个Fe原子的距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】碳是地球上组成生命的最基本的元素之一, 易形成多种化合物及单质。石墨烯(单层石墨)与金刚石均为碳的同素异形体,二者的晶体结构如图所示。2020 年10月,在上海举行的中国国际石墨烯创新大会上超平铜镍合金单晶晶圆、8英寸石墨烯单晶晶圆、锗基石墨烯晶圆等新材料亮相,展示了我国在高质量石墨烯材料领域的创新成果。

回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______ 形象化描述,基态碳原子核外有_______ 种不同运动状态的电子。
(2)甲基负离子(CH )、甲基正离子(CH
)、甲基正离子(CH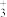 )是有机反应中重要的活性中间体,其空间构型分别为
)是有机反应中重要的活性中间体,其空间构型分别为____ 、______ ,碳原子的杂化方式分别为______ 、______ 。
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,第IIA族部分碳酸盐的相关数据如下表所示:
试解释,ⅡA族碳酸盐的分解温度随着阳离子半径的增大逐步升高的原因_______ 。
(4)在石墨烯晶体中,每个六元环占有_______ 个C 原子;在金刚石晶体中, C原子所连接的最小环也为六元环,每个六元环中最多有_______ 个C 原子在同一平面。
(5)已知金刚石晶体的晶胞参数为a nm,密度为ρg∙cm-3,则阿伏加德罗常数NA=_______ (用含a和ρ的代数式表示)。

回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)甲基负离子(CH
 )、甲基正离子(CH
)、甲基正离子(CH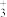 )是有机反应中重要的活性中间体,其空间构型分别为
)是有机反应中重要的活性中间体,其空间构型分别为(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,第IIA族部分碳酸盐的相关数据如下表所示:
碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
阳离子半径/pm | 66 | 99 | 112 | 135 |
(4)在石墨烯晶体中,每个六元环占有
(5)已知金刚石晶体的晶胞参数为a nm,密度为ρg∙cm-3,则阿伏加德罗常数NA=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】回答下列问题:
(1)Li2O是离子晶体,其晶格能可通过图(a)的 Born−Haber循环计算得到。

可知,Li原子的第一电离能为___________ kJ·mol−1,O=O键键能为___________ kJ·mol−1,Li2O晶格能为___________ kJ·mol−1。
(2)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为___________ g·cm−3(列出计算式)。
(1)Li2O是离子晶体,其晶格能可通过图(a)的 Born−Haber循环计算得到。

可知,Li原子的第一电离能为
(2)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】2023年8月1日起,我国对镓(Ga)、锗(Ge)相关物质实施出口管制。镓、锗元素及其化合物有许多用途。请回答:
(1)基态锗(Ge)原子简化的核外电子排布式为______ 。
(2)Ga属于ⅢA族元素,可形成GaX3、GaX(X代表卤素原子)两类卤化物和实验式为GaX2的化合物,相邻元素Ge常见卤化物为GeX4。
①金属镓(Ga)的几种卤化物熔点如下表:
GaF3熔点比GaCl3熔点高很多的原因是________ 。
②比较GaCl3、GeCl4的键角:Cl-Ga-Cl____ Cl-Ge-Cl(填“>”、“<”或“=”)。
③资料显示:Ga不存在+Ⅳ价,请用化学式表示实验式为GaCl2化合物可能的组成形态:________ [用罗马字符标明Ga在化合物中的价态:如Ga(Ⅲ)Cl3]。
(3)砷化镓是一种重要的半导体材料。砷化镓的晶胞如图1所示,Ga原子做面心立方密堆积,As原子填充在一半由Ga原子构成的四面体空隙中。沿晶胞对角线A→B方向观察得到的投影图如 2所示。请回答:______ pm(用含a、b的式子表示)。
②请在图2中将沿晶胞对角线A→B方向的As原子所在的位置涂黑________ 。
(1)基态锗(Ge)原子简化的核外电子排布式为
(2)Ga属于ⅢA族元素,可形成GaX3、GaX(X代表卤素原子)两类卤化物和实验式为GaX2的化合物,相邻元素Ge常见卤化物为GeX4。
①金属镓(Ga)的几种卤化物熔点如下表:
| GaF3 | GaCl3 | GaBr3 | |
| 熔点/℃ | >1000 | 77.8 | 122.3 |
②比较GaCl3、GeCl4的键角:Cl-Ga-Cl
③资料显示:Ga不存在+Ⅳ价,请用化学式表示实验式为GaCl2化合物可能的组成形态:
(3)砷化镓是一种重要的半导体材料。砷化镓的晶胞如图1所示,Ga原子做面心立方密堆积,As原子填充在一半由Ga原子构成的四面体空隙中。沿晶胞对角线A→B方向观察得到的投影图如 2所示。请回答:

②请在图2中将沿晶胞对角线A→B方向的As原子所在的位置涂黑
您最近一年使用:0次



