铬元素在工业中各个领域应用广泛,回答下列问题:
(1)基态铬原子的外围电子排布式为____ 、电子占据的最高能级的轨道形状为____ 。
(2)常温下,氯化酰铬(CrO2Cl2)为暗红色液体,能溶解在常见的有机溶剂中。则氯化酰铬的晶体类型为____ ,CS2是一种常见的能溶解氯化酰铬的有机溶剂,其分子形状为____ 。
(3)氮化铬(CrN)晶体在工业上用途广泛,其晶胞结构如图所示,则该晶胞结构与____ (填一种常见的离子晶体的化学式)的晶胞结构一样;氮化铬晶体的熔点与MgO晶体的熔点的大小关系为____ 。
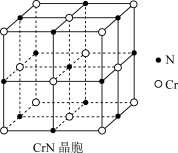
(4)已知氮化铬晶胞的边长为acm,阿伏加德罗常数值为NA,则该晶体的密度为____ (用含a、NA的式子表示)。
(1)基态铬原子的外围电子排布式为
(2)常温下,氯化酰铬(CrO2Cl2)为暗红色液体,能溶解在常见的有机溶剂中。则氯化酰铬的晶体类型为
(3)氮化铬(CrN)晶体在工业上用途广泛,其晶胞结构如图所示,则该晶胞结构与

(4)已知氮化铬晶胞的边长为acm,阿伏加德罗常数值为NA,则该晶体的密度为
更新时间:2022-03-18 16:20:13
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】蒙脱石散对消化道内的病毒、病菌及其产生的毒素、气体等有极强的固定、抑制作用,常用于成人及儿童急性、慢性腹泻。蒙脱石散的有效成分可表示为(AlMg)2(SixOy)(OH)z·nH2O。
(1)基态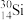 原子的核外电子排布式为
原子的核外电子排布式为__________ 。
(2)O、Mg、Al、Si四种元素的第一电离能从大到小的顺序为__________ 。
(3)SiCl4是无色透明液体,可以与N-甲基咪唑 等物质反应。
等物质反应。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液体流__________ (填“会”或“不会”)发生偏转。
②一个N—甲基咪唑分子中含有__________ 个σ键;SiCl4中硅原子的杂化方式为__________ 。
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成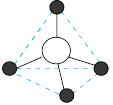 :其中
:其中 表示氧原子,中心
表示氧原子,中心 表示硅原子,其俯视图为
表示硅原子,其俯视图为 。
。
①SiO2晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。
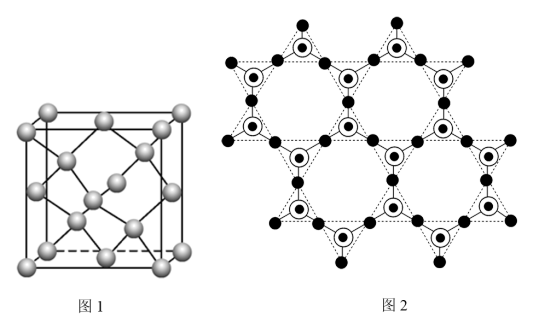
推测SiO2晶胞中含有__________ 个O原子,O—Si—O的键角为__________ 。
②蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图2所示,则x:y=__________ 。
(1)基态
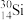 原子的核外电子排布式为
原子的核外电子排布式为(2)O、Mg、Al、Si四种元素的第一电离能从大到小的顺序为
(3)SiCl4是无色透明液体,可以与N-甲基咪唑
 等物质反应。
等物质反应。①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液体流
②一个N—甲基咪唑分子中含有
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成
 :其中
:其中 表示氧原子,中心
表示氧原子,中心 表示硅原子,其俯视图为
表示硅原子,其俯视图为 。
。①SiO2晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。

推测SiO2晶胞中含有
②蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图2所示,则x:y=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2018年11月《物理评论快报》报道了艾姆斯实验室制造的包含钙、钾、铁和砷以及少量镍的CaK(Fe1-xNix)4As4新型化合物材料,呈现出被称为刺猬自旋新磁态。有助于更好理解磁性与非常规超导性之间的联系。回答下列问题:
(1)基态镍原子的电子排布式为[Ar]______________ ;上述材料中所含元素的基态原子中,未成对电子数最多的是___________ (填元素符号)。
(2)铁及其离子易形成配离子,如[Fe(CN)6]3-、[Fe(CN)6]4-、Fe(CO)5等。所包括的非金属元素中第一电离能最大的是__________ (填元素符号);
(3)K3AsO3可用于碘的微量分析。
①K+的焰色反应呈紫色,金属元素能产生焰色实验的微观原因为____________ 。
②AsO33-的立体构型为________ ,写出一种与其互为等电子体的分子________
(填化学式)。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为___________ 。
(5)①金属镍的原子堆积方式如图所示,则金属镍晶胞俯视图为____ 。

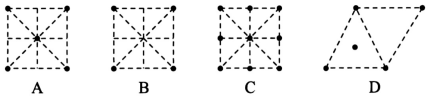
②某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=_____ g·cm-3。
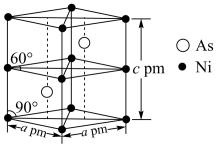
(1)基态镍原子的电子排布式为[Ar]
(2)铁及其离子易形成配离子,如[Fe(CN)6]3-、[Fe(CN)6]4-、Fe(CO)5等。所包括的非金属元素中第一电离能最大的是
(3)K3AsO3可用于碘的微量分析。
①K+的焰色反应呈紫色,金属元素能产生焰色实验的微观原因为
②AsO33-的立体构型为
(填化学式)。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(5)①金属镍的原子堆积方式如图所示,则金属镍晶胞俯视图为


②某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】I.金属催化剂M(Co、Ni)催化硼氢化钠( )水解释放
)水解释放 机理如下图所示:
机理如下图所示:

(1)过程Ⅱ中形成化学键的类型有________(填序号)。
(2) 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在________ 个配位键。
(3) 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为________ 。
Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为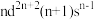 ,中子数为31,
,中子数为31,
(4)Q原子符号为________ ;基态Q原子核外成对电子数和未成对电子数之比为________ 。
Ⅲ. 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:
(5)钕(Nd)属于镧系元素,则其在元素周期表中处于________ 区,Co元素在元素周期表中的位置________ 。
Ⅳ.分子式为 的化合物的结构如图,
的化合物的结构如图,
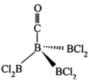
(6)其中B原子的杂化类型是________ ,B-B-B键的键角________ Cl-B-Cl的键角(填“ ”“
”“ ”或“
”或“ ”)。
”)。
 )水解释放
)水解释放 机理如下图所示:
机理如下图所示:
(1)过程Ⅱ中形成化学键的类型有________(填序号)。
| A.离子键 | B.金属键 | C.极性键 | D.非极性键 |
(2)
 最终会转化为
最终会转化为 ,1个
,1个 中存在
中存在(3)
 是一种重要的还原剂,其组成元素的电负性由大到小的顺序为
是一种重要的还原剂,其组成元素的电负性由大到小的顺序为Ⅱ.过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为
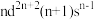 ,中子数为31,
,中子数为31,(4)Q原子符号为
Ⅲ.
 、
、 是新型磁性材料的成分。依据其中有关元素回答问题:
是新型磁性材料的成分。依据其中有关元素回答问题:(5)钕(Nd)属于镧系元素,则其在元素周期表中处于
Ⅳ.分子式为
 的化合物的结构如图,
的化合物的结构如图,
(6)其中B原子的杂化类型是
 ”“
”“ ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】第四周期的元素砷(As)和镍(Ni)具有广泛的应用。回答下列问题:
(1)基态As原子的核外电子排布式为____ 。
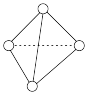
(2)砷单质的气态分子构型如图所示,在其中4条棱上各插入1个硫原子,形成As4S4,俗称雄黄,则雄黄可能有____ 种不同的结构;0.5molAs4S4中含有____ molAs—S键。
(3)亚砷酸(H3AsO3)形成的盐可用作长效杀虫剂和除草剂,AsO 的空间构型为
的空间构型为____ ;磷和砷同主族,亚磷酸(H3PO3)中心原子磷配位数为4,则亚磷酸为____ 元酸。
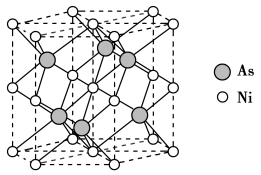
(4)As和Ni形成的一种晶体晶胞中原子堆积方式如图所示,晶体中As原子围成的空间构型为____ (填“三角形”“四面体”或“八面体”),图中六棱柱底边边长为apm,高为cpm,阿伏加德罗常数为NA,则该晶体的密度ρ=____ g•cm-3。
(1)基态As原子的核外电子排布式为
(2)砷单质的气态分子构型如图所示,在其中4条棱上各插入1个硫原子,形成As4S4,俗称雄黄,则雄黄可能有

(3)亚砷酸(H3AsO3)形成的盐可用作长效杀虫剂和除草剂,AsO
 的空间构型为
的空间构型为(4)As和Ni形成的一种晶体晶胞中原子堆积方式如图所示,晶体中As原子围成的空间构型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】请完成下列各题的填空:
(1)氢化钠(NaH)电子式为_________ ,氢负离子的离子结构示意 图为_________
(2)元素X的最外层电子数是次外层电子数的3倍,该元素名称是_________ ,该元素核外电子排布式为_________ ,画出该元素的外围电子排布图_________
(3)前四周期元素中,未成对电子数为5的元素符号是_________ ,该元素在周期表中的位置为第_________ 周期,_________ 族、_________ 区
(4)C、N、O的第一电离能由大到小的顺序为_________ 。由这三种元素和氢原子共同组成的离子化合物的化学式为_________ (只写一件)
(5)碳酸根离子( )的VSEPR模型为
)的VSEPR模型为_________ ,其中心原子的轨道杂化方式为_________ 。
(1)氢化钠(NaH)电子式为
(2)元素X的最外层电子数是次外层电子数的3倍,该元素名称是
(3)前四周期元素中,未成对电子数为5的元素符号是
(4)C、N、O的第一电离能由大到小的顺序为
(5)碳酸根离子(
 )的VSEPR模型为
)的VSEPR模型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C是中学化学中常见的三种元素(A、B、C代表元素符号)。A位于元素周期表中第4周期,其基态原子最外层电子数为2且内层轨道全部排满电子。短周期元素B的一种常见单质为淡黄色粉末。元素C的原子最外层电子数是其内层电子数的3倍。
(1)在第3周期中,第一电离能大于B的元素有_______ 种;A与B形成晶体的晶胞如图所示,该晶胞实际拥有Bn-的数目为_______ ;
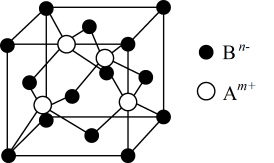
(2)B的氢化物(H2B)分子的空间构型为__________ ;
在乙醇中的溶解度:sH2C)>s(H2B),其原因是_______ 。
(3)B与C可形成BC
①BC 中,B原子轨道的杂化类型是
中,B原子轨道的杂化类型是________ 。
②人们将价电子数和原子数分别相同的不同分子、离子或原子团称为等电子体。与BC 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_______ (写出一种即可)。
(4)A的氯化物与氨水反应可形成配合物[A(NH3)4]Cl2,l mol该配合物中含有 键的物质的量为
键的物质的量为___ mol。
(1)在第3周期中,第一电离能大于B的元素有

(2)B的氢化物(H2B)分子的空间构型为
在乙醇中的溶解度:sH2C)>s(H2B),其原因是
(3)B与C可形成BC

①BC
 中,B原子轨道的杂化类型是
中,B原子轨道的杂化类型是②人们将价电子数和原子数分别相同的不同分子、离子或原子团称为等电子体。与BC
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)A的氯化物与氨水反应可形成配合物[A(NH3)4]Cl2,l mol该配合物中含有
 键的物质的量为
键的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】选修已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数是D的2倍。F元素在地壳中含量位于金属元素的第二位。回答下列问题:
(1)F元素价层电子排布式为_______________________ 。
(2)关于B2A2的下列说法中正确的是___________
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中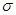 键和
键和 键数目比为1:1
键数目比为1:1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的A—B键属于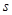 —
— 键
键
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为___________________
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能都高的主要原因是
__________________________________________________________________
(5)D的氢化物比E的氢化物沸点高,其主要原因是________________________ ;E的氢化物的价层电子对互斥模型为____________________ ,E原子的杂化方式为__________ 。
(6)F单质的晶体在不同温度下有两种堆积方式,即面心立方堆积和体心立方堆积,其晶胞的棱边长分别为a cm、b cm,则F单质的这两种晶体密度之比为_________ ,F原子的配位数之比为________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中
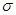 键和
键和 键数目比为1:1
键数目比为1:1C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的A—B键属于
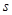 —
— 键
键(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能都高的主要原因是
(5)D的氢化物比E的氢化物沸点高,其主要原因是
(6)F单质的晶体在不同温度下有两种堆积方式,即面心立方堆积和体心立方堆积,其晶胞的棱边长分别为a cm、b cm,则F单质的这两种晶体密度之比为
您最近一年使用:0次
【推荐2】I.C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示石墨仅表示出其中的一层结构:

(1)C60、金刚石和石墨三者的关系是互为______ ;
A. 同分异构体 B.同素异形体 C.同系物 D.同位素
(2)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅硅单键的数目是______ NA;
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是______ ;
(4)观察CO2分子晶体结构的一部分,每个CO2分子周围有______ 个与之紧邻且等距的分子CO2;
(5)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为______ ,每个Cs+周围紧邻且等距的Clˉ数目为 ______ 。
II.金属铁及其化合物在合金材料以及催化剂等方面应用广泛。
(1)Fe能与CO形成配合物Fe(CO)5,熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于____ (填晶体类型)。1 mol Fe(CO)5中含有____ mol σ键。写出一种配体与CO互为等电子体的阴离子_____ 。
(2)已知某铁晶体的晶胞结构如图所示。

①该晶胞中含有铁原子的数目为___________ 。
②若晶胞的边长为a cm,则晶体铁的密度为________ g·cm-3(用代数式表示,阿伏伽德罗常数为NA)。

(1)C60、金刚石和石墨三者的关系是互为
A. 同分异构体 B.同素异形体 C.同系物 D.同位素
(2)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅硅单键的数目是
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)观察CO2分子晶体结构的一部分,每个CO2分子周围有
(5)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
II.金属铁及其化合物在合金材料以及催化剂等方面应用广泛。
(1)Fe能与CO形成配合物Fe(CO)5,熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于
(2)已知某铁晶体的晶胞结构如图所示。

①该晶胞中含有铁原子的数目为
②若晶胞的边长为a cm,则晶体铁的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】2019年,全球锂电池73%的产能来自中国,随着技术的不断进步,锂离子电池已经开始在重型设备、交通运输等诸多行业取代传统电池。回答下列问题:
(1)基态锂原子核外电子有____ 种不同空间运动状态,第二电离能锂____ (选填“>”、“<”或“=”)铍。
(2)某锂电池的正极材料为LiFePO4。
①基态铁原子价电子的轨道表达式为____ 。
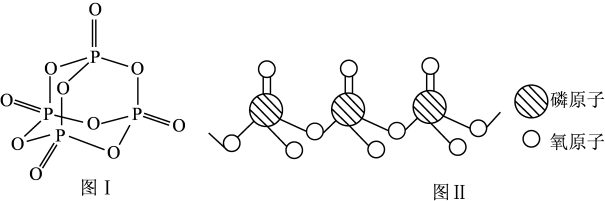
②磷元素能形成多种酸根和氧化物,其中一种氧化物的P4O10的结构如图I所示,其中P原子的杂化方式为____ ,P4O10分子是____ (选填“极性”或“非极性”)分子。
③图II是一种多聚磷酸根的示意图,由图可知该多聚磷酸根的化学式为____ 。(用n代表磷原子个数)
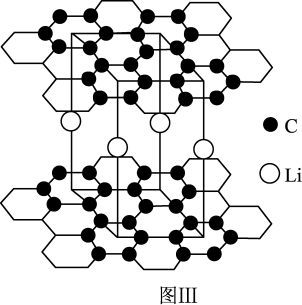
(3)某锂电池的负极是锂原子以层状规则排列嵌入石墨层间构成的材料,其结构如图III所示。
①关于石墨的导电性说法正确的是____ 。
A.石墨中碳原子之间以sp杂化轨道成键
B.石墨导电方向主要是沿着层面方向
C.石墨属于离子晶体
D.石墨中每个碳原子均有一个未参与杂化的轨道
②已知碳原子之间的最短距离为anm,则锂原子之间的最短距离为____ ,如果石墨层之间距离为bnm(b>3a),NA为阿伏加德罗常数的值,该材料的密度为____ g•cm-3。(列出表达式即可)
(1)基态锂原子核外电子有
(2)某锂电池的正极材料为LiFePO4。
①基态铁原子价电子的轨道表达式为
②磷元素能形成多种酸根和氧化物,其中一种氧化物的P4O10的结构如图I所示,其中P原子的杂化方式为
③图II是一种多聚磷酸根的示意图,由图可知该多聚磷酸根的化学式为

(3)某锂电池的负极是锂原子以层状规则排列嵌入石墨层间构成的材料,其结构如图III所示。

①关于石墨的导电性说法正确的是
A.石墨中碳原子之间以sp杂化轨道成键
B.石墨导电方向主要是沿着层面方向
C.石墨属于离子晶体
D.石墨中每个碳原子均有一个未参与杂化的轨道
②已知碳原子之间的最短距离为anm,则锂原子之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】钻(Co)是生产耐热介金、硬质介金、防介金、磁性合金和各种钻盐的重要原料。请回答下列问题:
(1)基态Co原子的价电子排布式为_______ 。
(2)Co同周期同族的三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为_______ (用化学式表示)。
(3)含钴配合物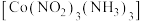 的中心离子的配位数为
的中心离子的配位数为_______ ,其中N采取的杂化类型为_______ 。
(4)钴蓝晶体结构如图所示,该立方晶胞有4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为_______ ,设阿伏加德罗常数的值为 ,该晶体密度为
,该晶体密度为_______  (列计算式)。
(列计算式)。

(1)基态Co原子的价电子排布式为
(2)Co同周期同族的三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
(3)含钴配合物
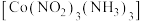 的中心离子的配位数为
的中心离子的配位数为(4)钴蓝晶体结构如图所示,该立方晶胞有4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为
 ,该晶体密度为
,该晶体密度为 (列计算式)。
(列计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】第ⅢA族元素及某些常见非金属元素的化合物在晶体材料等方面的用途非常广泛。回答下列问题:
(1)写出基态Ga原子的价电子轨道表示式__________________
(2)NH4HF2中HF2-的结构为F-H···F-,则NH4HF2中含有的化学键有_________
A.离子键 B.共价键 C.金属键 氢键 E.配位键
(3)CH3OH分子中的键角:H-C-H_______ H-O-C。(填“<”、“>”、“=”)
(4)B、Al、Ga单质的熔点依次为2300°C,660°C,29.8°C,解释熔点产生差异的原因:___________________
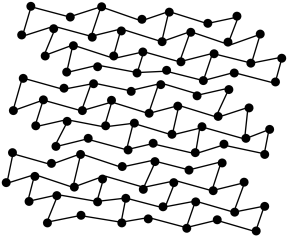
(5)黑磷是磷的一种同素异形体,与石墨烯类似,其晶体结构片段如图所示:其中最小的环为____ 元环,每个环平均含有____ 个P原子。
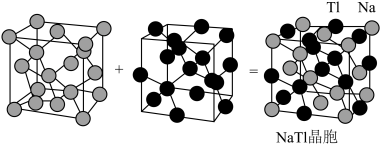
(6)铊化钠(NaTl)可看作是由两个金刚石晶格穿插得到的(如图),已知晶胞参数为a pm。
①铊化钠中Tl-Tl间最小距离为__________ pm。
②设阿伏加 德罗常数的值为NA,则NaTl的密度是________ g·cm-3(列出计算表达式)。
(1)写出基态Ga原子的价电子轨道表示式
(2)NH4HF2中HF2-的结构为F-H···F-,则NH4HF2中含有的化学键有
A.离子键 B.共价键 C.金属键 氢键 E.配位键
(3)CH3OH分子中的键角:H-C-H
(4)B、Al、Ga单质的熔点依次为2300°C,660°C,29.8°C,解释熔点产生差异的原因:
(5)黑磷是磷的一种同素异形体,与石墨烯类似,其晶体结构片段如图所示:其中最小的环为

(6)铊化钠(NaTl)可看作是由两个金刚石晶格穿插得到的(如图),已知晶胞参数为a pm。

①铊化钠中Tl-Tl间最小距离为
②设阿伏加 德罗常数的值为NA,则NaTl的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物有许多用途。回答下列问题:
(1)基态S原子中,电子占据的最高能层符号为______ 。
(2)H2S分子的立体构型是_____ ,属于_____ (填“非极性”“极性”)分子;根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同其他分子的是_________ 。
(3)气态三氧化硫以单分子形式存在,其分子的键角为____ ,其中共价键的类型有____ 种,固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_____ 。
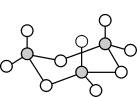
(4)下图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为_____ 。

(1)基态S原子中,电子占据的最高能层符号为
(2)H2S分子的立体构型是
(3)气态三氧化硫以单分子形式存在,其分子的键角为

(4)下图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

您最近一年使用:0次



