含氮化合物既是重要的化工原料,也是常见的污染物。
(1)已知:I.CO(g)+ O2(g)
O2(g)  CO2(g) △H1=—283.0kJ·mol-1
CO2(g) △H1=—283.0kJ·mol-1
II.N2(g)+O2(g) 2NO(g) △H2=+179.5kJ·mol-1
2NO(g) △H2=+179.5kJ·mol-1
则2NO(g)+2CO(g) N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=_______ kJ·mol-1。
(2)某小组模拟不同条件下的合成氨反应,向容器中充入3molN2和9molH2,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图1所示。
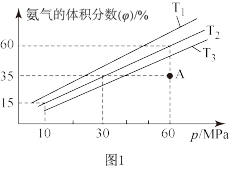
①T1、T2、T3由大到小的顺序为_______ 。
②在T2、60MPa条件下,A点v正_______ (填“>”、“<"或“=”)v逆。
③计算T2、60MPa平衡体系的平衡常数Kp=_______ MPa-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果保留两位有效数字)
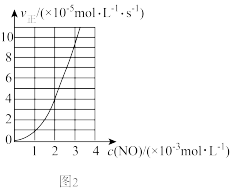
(3)NO的氧化还原反应为2NO(g)+2H2(g) N2(g)+2H2O(g)。研究表明:某温度时v正=k·cm(NO)·cn(H2),其中k=2.5×103mol(m+n-1)·L(m+n-1)·s-1.该温度下,当c(H2)=4.0×10-3mol·L-1时,实验测得v正与c(NO)的关系如图2所示,则m=
N2(g)+2H2O(g)。研究表明:某温度时v正=k·cm(NO)·cn(H2),其中k=2.5×103mol(m+n-1)·L(m+n-1)·s-1.该温度下,当c(H2)=4.0×10-3mol·L-1时,实验测得v正与c(NO)的关系如图2所示,则m=_______ ,n=_______ 。
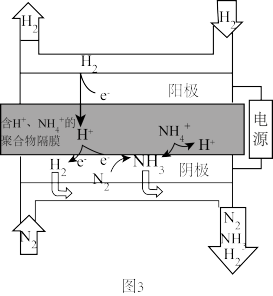
(4)我国的科研工作者研究在常温常压下电化学合成氨,工作原理如图3所示。其中阳极和阴极均为附有催化剂的膜电极。阴极发生的反应有三个,分别为2H++2e-=H2↑、_______ 和 =H++NH3↑。
=H++NH3↑。
(1)已知:I.CO(g)+
 O2(g)
O2(g)  CO2(g) △H1=—283.0kJ·mol-1
CO2(g) △H1=—283.0kJ·mol-1II.N2(g)+O2(g)
 2NO(g) △H2=+179.5kJ·mol-1
2NO(g) △H2=+179.5kJ·mol-1则2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H=
N2(g)+2CO2(g) △H=(2)某小组模拟不同条件下的合成氨反应,向容器中充入3molN2和9molH2,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图1所示。

①T1、T2、T3由大到小的顺序为
②在T2、60MPa条件下,A点v正
③计算T2、60MPa平衡体系的平衡常数Kp=
(3)NO的氧化还原反应为2NO(g)+2H2(g)
 N2(g)+2H2O(g)。研究表明:某温度时v正=k·cm(NO)·cn(H2),其中k=2.5×103mol(m+n-1)·L(m+n-1)·s-1.该温度下,当c(H2)=4.0×10-3mol·L-1时,实验测得v正与c(NO)的关系如图2所示,则m=
N2(g)+2H2O(g)。研究表明:某温度时v正=k·cm(NO)·cn(H2),其中k=2.5×103mol(m+n-1)·L(m+n-1)·s-1.该温度下,当c(H2)=4.0×10-3mol·L-1时,实验测得v正与c(NO)的关系如图2所示,则m=
(4)我国的科研工作者研究在常温常压下电化学合成氨,工作原理如图3所示。其中阳极和阴极均为附有催化剂的膜电极。阴极发生的反应有三个,分别为2H++2e-=H2↑、
 =H++NH3↑。
=H++NH3↑。
更新时间:2022-04-13 01:23:48
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
【推荐1】氮的化合物种类繁多,性质也各不相同。请回答下列问题:
(1)已知:①

②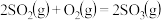

则 的
的
_______ 。
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:
 。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率
。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率 随温度的变化如图所示:
随温度的变化如图所示:

图中a、b、c三点中,达到平衡的点是_______ ;温度为1100K时, 的平衡体积分数为
的平衡体积分数为_______ 。
(3)现代技术用氨气将汽车尾气中的 还原为
还原为 和
和 ,反应原理是
,反应原理是
 。
。
①实际生产中 的反应温度不宜过高的原因是
的反应温度不宜过高的原因是_______ 。
②500℃时,在2L恒容密闭容器中充入1molNO、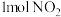 和
和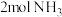 ,8min时反应达到平衡,此时
,8min时反应达到平衡,此时 的转化率为40%,平衡体系的压强为
的转化率为40%,平衡体系的压强为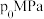 ,则0~8min内用
,则0~8min内用 表示的平均反应速率
表示的平均反应速率
_______  ,500℃时该反应的平衡常数
,500℃时该反应的平衡常数
_______ MPa(用含 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
③已知 ,
,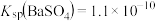 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中
_______ (保留三位有效数字)。
(1)已知:①


②
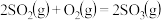

则
 的
的
(2)NO作为主要空气污染物,其主要来源是汽车尾气,研究人员用活性炭对汽车尾气中的NO进行吸附,并发生反应:

 。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率
。在恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时,测得NO的转化率 随温度的变化如图所示:
随温度的变化如图所示:
图中a、b、c三点中,达到平衡的点是
 的平衡体积分数为
的平衡体积分数为(3)现代技术用氨气将汽车尾气中的
 还原为
还原为 和
和 ,反应原理是
,反应原理是
 。
。①实际生产中
 的反应温度不宜过高的原因是
的反应温度不宜过高的原因是②500℃时,在2L恒容密闭容器中充入1molNO、
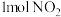 和
和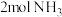 ,8min时反应达到平衡,此时
,8min时反应达到平衡,此时 的转化率为40%,平衡体系的压强为
的转化率为40%,平衡体系的压强为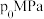 ,则0~8min内用
,则0~8min内用 表示的平均反应速率
表示的平均反应速率
 ,500℃时该反应的平衡常数
,500℃时该反应的平衡常数
 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。③已知
 ,
,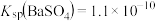 。向含有
。向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中
沉淀生成时,溶液中
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】船舶柴油机发动机工作时,反应产生的 尾气是空气主要污染物之一,研究
尾气是空气主要污染物之一,研究 的转化方法和机理具有重要意义。
的转化方法和机理具有重要意义。
已知: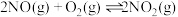





(1) 氧化脱除NO的总反应是
氧化脱除NO的总反应是
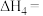
________ 。
(2)该反应过程有两步: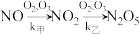 ,反应中各物质浓度变化如图所示。则速率常数
,反应中各物质浓度变化如图所示。则速率常数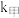
___________  (填“>”、“<”或“≈”),原因是
(填“>”、“<”或“≈”),原因是___________ 。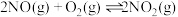 的反应历程分两步:
的反应历程分两步:
①则反应I与反应II的活化能:
___________ 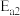 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
反应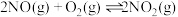 的平衡常数
的平衡常数
___________ (用 、
、 、
、 、
、 表示)。
表示)。
②在400k、初始压强为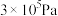 的恒温刚性容器中,按
的恒温刚性容器中,按 通入NO和
通入NO和 ,一定条件下发生反应。达平衡时NO转化率为90%,
,一定条件下发生反应。达平衡时NO转化率为90%, 转化率为40%。则
转化率为40%。则 的平衡常数
的平衡常数
___________ (分压=总压×物质的量分数;理想气体状态方程 ,
, )。
)。
(4)某研究小组将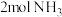 、
、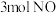 和一定量的
和一定量的 充入2L密闭容器中,在
充入2L密闭容器中,在 催化剂表面发生反应(
催化剂表面发生反应( ),NO的转化率随温度的变化情况如图所示:
),NO的转化率随温度的变化情况如图所示: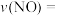
___________ (保留3位有效数字)。
②无氧条件下,NO生成 的转化率较低,原因可能是
的转化率较低,原因可能是___________ 。
 尾气是空气主要污染物之一,研究
尾气是空气主要污染物之一,研究 的转化方法和机理具有重要意义。
的转化方法和机理具有重要意义。已知:
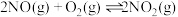





(1)
 氧化脱除NO的总反应是
氧化脱除NO的总反应是
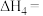
(2)该反应过程有两步:
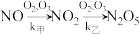 ,反应中各物质浓度变化如图所示。则速率常数
,反应中各物质浓度变化如图所示。则速率常数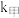
 (填“>”、“<”或“≈”),原因是
(填“>”、“<”或“≈”),原因是
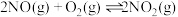 的反应历程分两步:
的反应历程分两步:| 步骤 | 反应 | 活化能 | 正反应速率方程 | 逆反应速率方程 |
| I |  (快) (快) |  | 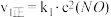 |  |
| II |  (慢) (慢) | 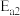 |  | 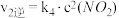 |

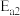 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。反应
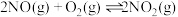 的平衡常数
的平衡常数
 、
、 、
、 、
、 表示)。
表示)。②在400k、初始压强为
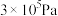 的恒温刚性容器中,按
的恒温刚性容器中,按 通入NO和
通入NO和 ,一定条件下发生反应。达平衡时NO转化率为90%,
,一定条件下发生反应。达平衡时NO转化率为90%, 转化率为40%。则
转化率为40%。则 的平衡常数
的平衡常数
 ,
, )。
)。(4)某研究小组将
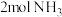 、
、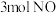 和一定量的
和一定量的 充入2L密闭容器中,在
充入2L密闭容器中,在 催化剂表面发生反应(
催化剂表面发生反应( ),NO的转化率随温度的变化情况如图所示:
),NO的转化率随温度的变化情况如图所示: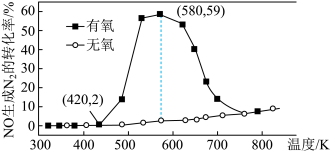
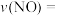
②无氧条件下,NO生成
 的转化率较低,原因可能是
的转化率较低,原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】研究 的捕集、回收、转化,对实现节能减排、资源利用、“碳中和”等目标具有重要意义。
的捕集、回收、转化,对实现节能减排、资源利用、“碳中和”等目标具有重要意义。
Ⅰ.将 还原成甲烷:
还原成甲烷:
ⅰ.Sabatier反应: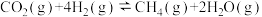

ⅱ.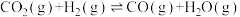
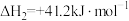
ⅲ.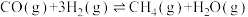
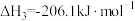
(1)
________ 。
(2)不同条件下按照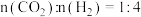 投料发生如上反应,
投料发生如上反应, 平衡转化率如图1所示。压强
平衡转化率如图1所示。压强 、
、 、
、 由小到大的顺序是
由小到大的顺序是________ ;压强为 时,随着温度升高,
时,随着温度升高, 的平衡转化率先减小后增大,解释温度高于600℃之后,随着温度升高
的平衡转化率先减小后增大,解释温度高于600℃之后,随着温度升高 转化率增大的原因是
转化率增大的原因是________ 。
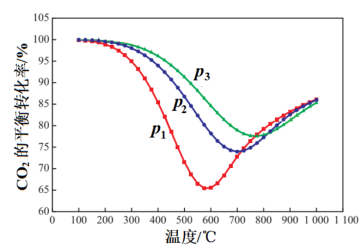
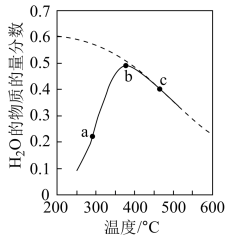
图1 图2
(3)按照 置于恒容密闭容器中发生如上反应,测得
置于恒容密闭容器中发生如上反应,测得 的物质的量分数与温度的关系如图2所示(虚线表示平衡曲线)。a、b、c三点的逆反应速率,
的物质的量分数与温度的关系如图2所示(虚线表示平衡曲线)。a、b、c三点的逆反应速率,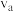 、
、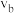 、
、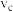 由大到小排序为
由大到小排序为________ ;高于380℃后, 的物质的量分数随温度升高而降低的原因是
的物质的量分数随温度升高而降低的原因是________________ 。
Ⅱ.将 还原成碳单质:Bosch反应:
还原成碳单质:Bosch反应: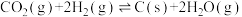
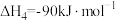
(4)Bosch反应自发进行,低温更有利于平衡正向移动,但是Bosch反应必须在高温下才能启动,原因是________________ 。
(5) 捕集和转化原理如图3所示。反应①完成之后,以
捕集和转化原理如图3所示。反应①完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到 ,在催化剂上检测到有积炭。下列有关说法正确的是
,在催化剂上检测到有积炭。下列有关说法正确的是_________
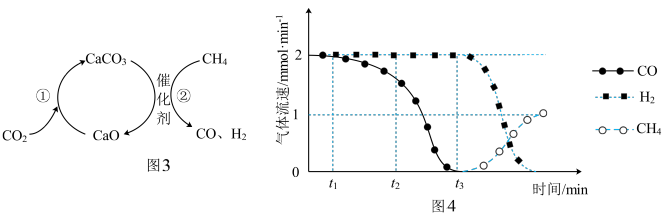
a.反应①为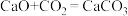 ;反应②为
;反应②为
b.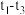 ,
, 比
比 多,且生成的
多,且生成的 速率不变,推测有副反应
速率不变,推测有副反应
c. 时刻,副反应生成
时刻,副反应生成 的速率大于反应②生成
的速率大于反应②生成 的速率
的速率
d. 之后,生成CO的速率为0,是因为反应②不再发生
之后,生成CO的速率为0,是因为反应②不再发生
 的捕集、回收、转化,对实现节能减排、资源利用、“碳中和”等目标具有重要意义。
的捕集、回收、转化,对实现节能减排、资源利用、“碳中和”等目标具有重要意义。Ⅰ.将
 还原成甲烷:
还原成甲烷:ⅰ.Sabatier反应:
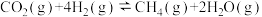

ⅱ.
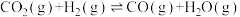
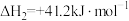
ⅲ.
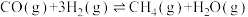
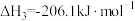
(1)

(2)不同条件下按照
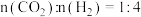 投料发生如上反应,
投料发生如上反应, 平衡转化率如图1所示。压强
平衡转化率如图1所示。压强 、
、 、
、 由小到大的顺序是
由小到大的顺序是 时,随着温度升高,
时,随着温度升高, 的平衡转化率先减小后增大,解释温度高于600℃之后,随着温度升高
的平衡转化率先减小后增大,解释温度高于600℃之后,随着温度升高 转化率增大的原因是
转化率增大的原因是

图1 图2
(3)按照
 置于恒容密闭容器中发生如上反应,测得
置于恒容密闭容器中发生如上反应,测得 的物质的量分数与温度的关系如图2所示(虚线表示平衡曲线)。a、b、c三点的逆反应速率,
的物质的量分数与温度的关系如图2所示(虚线表示平衡曲线)。a、b、c三点的逆反应速率,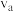 、
、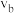 、
、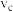 由大到小排序为
由大到小排序为 的物质的量分数随温度升高而降低的原因是
的物质的量分数随温度升高而降低的原因是Ⅱ.将
 还原成碳单质:Bosch反应:
还原成碳单质:Bosch反应: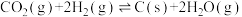
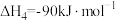
(4)Bosch反应自发进行,低温更有利于平衡正向移动,但是Bosch反应必须在高温下才能启动,原因是
(5)
 捕集和转化原理如图3所示。反应①完成之后,以
捕集和转化原理如图3所示。反应①完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到 ,在催化剂上检测到有积炭。下列有关说法正确的是
,在催化剂上检测到有积炭。下列有关说法正确的是
a.反应①为
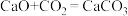 ;反应②为
;反应②为
b.
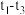 ,
, 比
比 多,且生成的
多,且生成的 速率不变,推测有副反应
速率不变,推测有副反应
c.
 时刻,副反应生成
时刻,副反应生成 的速率大于反应②生成
的速率大于反应②生成 的速率
的速率d.
 之后,生成CO的速率为0,是因为反应②不再发生
之后,生成CO的速率为0,是因为反应②不再发生
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】氮及其化合物在工农业生产、生活中有着重要作用。
1.下列元素中电负性最大的是____。
2.NH3和PH3都具有四面体结构,NH3比PH3的分解温度高的原因是____。
3.配合物Ni(CO)4也具有四面体结构,常温下Ni(CO)4为液态,易溶于CCl4、苯等有机溶剂。写出基态Ni的电子排布式____ ;Ni(CO)4属于____ 晶体。
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol
副反应:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol
有关物质产率与温度的关系如图。_________ 。
6.工业上采用物料比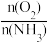 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:______________ 。
7.下列说法正确的是______________ 。
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
表中数据计算0~4min内υ(NO2)=_________ 。
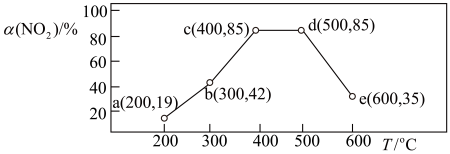
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点___ (填“是”或“不是”)反应达平衡的点。d点之后,转化率随温度升高而降低的原因是___ 。
1.下列元素中电负性最大的是____。
| A.N | B.P | C.Si | D.C |
| A.NH3分子间有氢键 | B.NH3分子极性强 |
| C.N-H键键能大于P-H键 | D.氨极易液化 |
4.Zn(NH3)42+离子也具有四面体结构,Zn2+可提供4个能量最低的空轨道与NH3参与形成配位键,这4个空轨道是____。
| A.3p | B.3d | C.4s | D.4p |
氨在某催化剂作用下只发生如下反应:
主反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H =-905kJ/mol
4NO(g)+6H2O(g) △H =-905kJ/mol副反应:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H =-1268kJ/mol
2N2(g)+6H2O(g) △H =-1268kJ/mol有关物质产率与温度的关系如图。
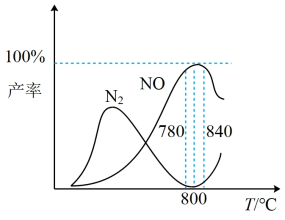
6.工业上采用物料比
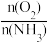 在1.7~2.0,主要目的是:
在1.7~2.0,主要目的是:7.下列说法正确的是
A. 工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B. 在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C. 选择合适的催化剂,可以大幅度提高NO在最终产物中的比率
8.一定温度下,在3.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应,CH4(g)+2NO2(g)
 CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:
CO2(g)+N2(g)+2H2O(g) △H <0,反应时间(t)与容器内气体总压强(p)的数据见下表:| 时间(t/min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强(p/100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
9.在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率 [α(NO2)/%] 如下图;c点
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】环氧丙烷( ,简写为PO)是重要的工业原料,利用丙烯(C3H6)气相直接环氧化是未来工业生产的趋势,寻找合适的催化剂是目前实验研究的热点。丙烯气相直接环氧化反应为:C3H6(g)+ H2(g)+ O2(g)=
,简写为PO)是重要的工业原料,利用丙烯(C3H6)气相直接环氧化是未来工业生产的趋势,寻找合适的催化剂是目前实验研究的热点。丙烯气相直接环氧化反应为:C3H6(g)+ H2(g)+ O2(g)=  (g)+ H2O(g) ΔH,回答下列问题:
(g)+ H2O(g) ΔH,回答下列问题:
(1)已知:
i.2C3H6(g)+O2(g)=2 (g)
(g) 
ii.H2(g)+ O2(g)=H2O(g)
O2(g)=H2O(g) 
则C3H6(g)+H2(g)+O2(g)= (g)+H2O(g) ΔH=
(g)+H2O(g) ΔH=_______ kJ·mol-1。
(2)①恒温恒容下,下列可判断丙烯气相直接环氧化反应达到平衡的是_______ (填标号)。
A.压强不再变化 B.密度不再变化
C.v正(丙烯): v正(环氧丙烷)=1:1 D.平均相对分子质量不再变化
②为增大C3H6的平衡转化率,可选择的条件是_______ (填标号)。
A.低温高压 B.增大C3H6浓度 C.使用高效催化剂 D.分离出产物
(3)选用Au/TS-1为催化剂,发生丙烯气相直接环氧化反应,副反应如下:
C3H6(g)+H2(g)+O2(g)=CH3CH2CHO(g)+H2O(g)
C3H6(g)+O2(g)=CH2=CHCHO(g)+H2O(g)
为探究TS-1的粒径对Au/TS-1催化活性的影响,恒温200℃、恒压pkPa条件下,C3H6与H2、O2各20.0mmol通入反应装置中,tmin后部分组分的物质的量如下表所示:
当粒径为240nm,tmin时反应恰好达到平衡状态,则C3H6的总转化率为_______ 。随着TS-1粒径的增大,PO生成的速率逐渐_______ (填“增大”或“减小”),原因是_______ 。
 ,简写为PO)是重要的工业原料,利用丙烯(C3H6)气相直接环氧化是未来工业生产的趋势,寻找合适的催化剂是目前实验研究的热点。丙烯气相直接环氧化反应为:C3H6(g)+ H2(g)+ O2(g)=
,简写为PO)是重要的工业原料,利用丙烯(C3H6)气相直接环氧化是未来工业生产的趋势,寻找合适的催化剂是目前实验研究的热点。丙烯气相直接环氧化反应为:C3H6(g)+ H2(g)+ O2(g)=  (g)+ H2O(g) ΔH,回答下列问题:
(g)+ H2O(g) ΔH,回答下列问题:(1)已知:
i.2C3H6(g)+O2(g)=2
 (g)
(g) 
ii.H2(g)+
 O2(g)=H2O(g)
O2(g)=H2O(g) 
则C3H6(g)+H2(g)+O2(g)=
 (g)+H2O(g) ΔH=
(g)+H2O(g) ΔH=(2)①恒温恒容下,下列可判断丙烯气相直接环氧化反应达到平衡的是
A.压强不再变化 B.密度不再变化
C.v正(丙烯): v正(环氧丙烷)=1:1 D.平均相对分子质量不再变化
②为增大C3H6的平衡转化率,可选择的条件是
A.低温高压 B.增大C3H6浓度 C.使用高效催化剂 D.分离出产物
(3)选用Au/TS-1为催化剂,发生丙烯气相直接环氧化反应,副反应如下:
C3H6(g)+H2(g)+O2(g)=CH3CH2CHO(g)+H2O(g)
C3H6(g)+O2(g)=CH2=CHCHO(g)+H2O(g)
为探究TS-1的粒径对Au/TS-1催化活性的影响,恒温200℃、恒压pkPa条件下,C3H6与H2、O2各20.0mmol通入反应装置中,tmin后部分组分的物质的量如下表所示:
| 粒径大小/nm | 240 | 450 | 810 | 1130 | |
| 物质的量 | PO | 1.80 | 1.45 | 1.09 | 0.672 |
| /mmol | 所有C3副产物 | 0.20 | 0.32 | 0.05 | 0.092 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氮的化合物在化肥、医药、炸药、材料等领域中有着极其重要用途。
(1)羟氨能与溴化银悬浊液反应:2NH2OH+2AgBr=N2↑+2Ag+2HBr+2H2O,羟氨的电子式为________ ;反应中烃氨表现________ 性.
(2)已知:a.N2(g)+3H2(g)=2NH3(g) △H=-92.2kJ/mol
b.H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol
c.2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) △H3
①△H3________ .
②反应c在常温下能快速进行的原因为________ .
(3)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g)≒N2O4(g) △H<0,甲中NO2的相关量随时间变化如下图所示。
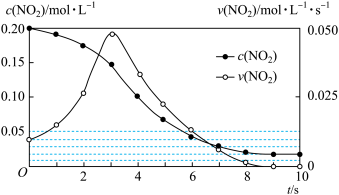
①0~3S内,甲容器中NO2的反应速率增大的原因是________ .
②甲达平衡时,温度若为T℃,此温度下的平衡常数Kc=________ .
③平衡时,K甲________ K乙(填“>”、“<”或“=”,下同),P甲________ P乙
(4)化学工作者对NO与H2的反应进行研究,提出下列3步机理:(k为速率常数)
第一步2NO=N2O2快反应,平衡时:V正=K正·c2(NO)=V逆=K逆·c(N2O2)
第二步N2O2+H2==N2O+H2O 慢反应 第三步N2O+H2=N2+H2O 快反应
其中可近似认为第二步反应不影响第一步平衡,下列说法正确的是________ .(填字母标号)
A.V(第一步逆反应)<V(第二步反应) B.总反应快慢主要由第二步反应决定
C.达平衡时,2c(NO)=c(N2O2) D.第一步反应的平衡常数K= K正/ K逆
(1)羟氨能与溴化银悬浊液反应:2NH2OH+2AgBr=N2↑+2Ag+2HBr+2H2O,羟氨的电子式为
(2)已知:a.N2(g)+3H2(g)=2NH3(g) △H=-92.2kJ/mol
b.H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol
c.2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) △H3
①△H3
②反应c在常温下能快速进行的原因为
(3)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g)≒N2O4(g) △H<0,甲中NO2的相关量随时间变化如下图所示。

①0~3S内,甲容器中NO2的反应速率增大的原因是
②甲达平衡时,温度若为T℃,此温度下的平衡常数Kc=
③平衡时,K甲
(4)化学工作者对NO与H2的反应进行研究,提出下列3步机理:(k为速率常数)
第一步2NO=N2O2快反应,平衡时:V正=K正·c2(NO)=V逆=K逆·c(N2O2)
第二步N2O2+H2==N2O+H2O 慢反应 第三步N2O+H2=N2+H2O 快反应
其中可近似认为第二步反应不影响第一步平衡,下列说法正确的是
A.V(第一步逆反应)<V(第二步反应) B.总反应快慢主要由第二步反应决定
C.达平衡时,2c(NO)=c(N2O2) D.第一步反应的平衡常数K= K正/ K逆
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】甲醇是重要的化工原料。利用合成气(主要成分为(CO,CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
ii:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
iii:CH3OH(g) CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
由此计算ΔH2=___ kJ·mol-1。已知ΔH1=-63kJ·mol-1,则ΔH3=___ kJ·mol-1。
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:
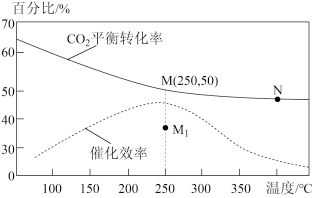
①下列说法不正确的是( )
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为___ ,250℃时反应的平衡常数Kp=___ (MPa)-2(保留三位有效数字);
③若要进一步提高甲醇产率,可采取的措施有___ (写两条即可)
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:___ 。
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g) CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
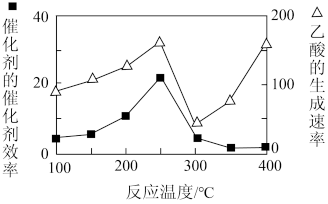
250~300℃时,乙酸的生成速率降低的主要原因是___ 。
300~400℃时,乙酸的生成速率升高的主要原因是___ 。
i:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1ii:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2iii:CH3OH(g)
 CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
| 化学键 | H—H | C=O | C≡O | H—O |
| E/KJ·mol-1 | 436 | 803 | 1076 | 465 |
由此计算ΔH2=
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:

①下列说法不正确的是
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为
③若要进一步提高甲醇产率,可采取的措施有
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)
 CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
250~300℃时,乙酸的生成速率降低的主要原因是
300~400℃时,乙酸的生成速率升高的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】空气污染治理是综合工程,其中氮氧化合物的治理是环保的一项重要工作,合理应用和处理氮的化合物,在生产生活中有着重要的意义。
(1)已知: N2(g)+O2(g)= 2NO(g) ΔH= +181.5kJ·mol-1。某科研小组尝试利用固体表面催化工艺进行NO的分解。若用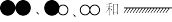 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是_______ (填字母)。

(2)为减少汽车尾气中NOx的排放,常采用CmHn(烃)催化还原NOx消除氮氧化物的污染。
如:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ∆H1 =-574kJ·mol-1;
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+ 2H2O(g) ∆H2 =-1160kJ·mol-1;
③CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+ 2H2O(g) ∆H3
则∆H3=_______ 。
(3)含氮化合物有很多种,其中亚硝酰氯(ClNO)是有机合成中常用的一种试剂。
已知: 2NO(g)+Cl2(g) 2ClNO(g ) ∆H<0
2ClNO(g ) ∆H<0
①一定温度下,将2 mol NO(g)与2 mol Cl2(g)置于2L恒容密闭容器中发生上述反应,若4 min末反应达到平衡状态,此时压强是初始时的0.8倍,则0~4 min内,平均反应速率v(Cl2)=_______ 。下列现象可判断反应达到平衡状态的是_______ (填选项字母)。
A.混合气体的平均相对分子质量不变
B.混合气体的密度保持不变
C.每消耗1 mol NO(g)同时生成1 mol ClNO(g)
D.NO和Cl2的物质的量之比保持不变
②为加快反应速率,同时提高NO(g)的平衡转化率,在保持其他条件不变时,可采取的措施有_______ (填选项字母)。
A.升高温度 B.缩小容器体积
C.使用合适的催化剂 D.再充入Cl2(g)
③一定条件下,在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO(g)的体积分数随 的变化如图所示,当
的变化如图所示,当 =2.5时,达到平衡状态,ClNO(g)的体积分数可能是图中的
=2.5时,达到平衡状态,ClNO(g)的体积分数可能是图中的_______ 点(填“D” “E”或“F”)。

(4)已知: 2NO(g)+O2(g) 2NO2 (g)的反应历程分两步:
2NO2 (g)的反应历程分两步:
①2NO(g) N2O2 (g) (快) v1正=k1正·c2(NO),v1逆 =k 1逆·c(N2O2);
N2O2 (g) (快) v1正=k1正·c2(NO),v1逆 =k 1逆·c(N2O2);
②N2O2 (g)+O2(g) 2NO2(g) (慢) v 2正= k2正c(N2O2)·c(O2), v2逆=k2逆·c2(NO2)。
2NO2(g) (慢) v 2正= k2正c(N2O2)·c(O2), v2逆=k2逆·c2(NO2)。
2NO(g)+O2(g) 2NO2 (g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
2NO2 (g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为_______ 。
(1)已知: N2(g)+O2(g)= 2NO(g) ΔH= +181.5kJ·mol-1。某科研小组尝试利用固体表面催化工艺进行NO的分解。若用
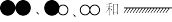 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如图所示。从吸附到解吸的过程中,能量状态最低的是
(2)为减少汽车尾气中NOx的排放,常采用CmHn(烃)催化还原NOx消除氮氧化物的污染。
如:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ∆H1 =-574kJ·mol-1;
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+ 2H2O(g) ∆H2 =-1160kJ·mol-1;
③CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+ 2H2O(g) ∆H3
则∆H3=
(3)含氮化合物有很多种,其中亚硝酰氯(ClNO)是有机合成中常用的一种试剂。
已知: 2NO(g)+Cl2(g)
 2ClNO(g ) ∆H<0
2ClNO(g ) ∆H<0①一定温度下,将2 mol NO(g)与2 mol Cl2(g)置于2L恒容密闭容器中发生上述反应,若4 min末反应达到平衡状态,此时压强是初始时的0.8倍,则0~4 min内,平均反应速率v(Cl2)=
A.混合气体的平均相对分子质量不变
B.混合气体的密度保持不变
C.每消耗1 mol NO(g)同时生成1 mol ClNO(g)
D.NO和Cl2的物质的量之比保持不变
②为加快反应速率,同时提高NO(g)的平衡转化率,在保持其他条件不变时,可采取的措施有
A.升高温度 B.缩小容器体积
C.使用合适的催化剂 D.再充入Cl2(g)
③一定条件下,在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO(g)的体积分数随
 的变化如图所示,当
的变化如图所示,当 =2.5时,达到平衡状态,ClNO(g)的体积分数可能是图中的
=2.5时,达到平衡状态,ClNO(g)的体积分数可能是图中的
(4)已知: 2NO(g)+O2(g)
 2NO2 (g)的反应历程分两步:
2NO2 (g)的反应历程分两步:①2NO(g)
 N2O2 (g) (快) v1正=k1正·c2(NO),v1逆 =k 1逆·c(N2O2);
N2O2 (g) (快) v1正=k1正·c2(NO),v1逆 =k 1逆·c(N2O2);②N2O2 (g)+O2(g)
 2NO2(g) (慢) v 2正= k2正c(N2O2)·c(O2), v2逆=k2逆·c2(NO2)。
2NO2(g) (慢) v 2正= k2正c(N2O2)·c(O2), v2逆=k2逆·c2(NO2)。2NO(g)+O2(g)
 2NO2 (g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
2NO2 (g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氮气来源广泛且转化生成的工业产品(如氨、肼类等)具有重要的社会效益和经济价值。我国科学家成功制备了一类以金属锌为中心离子、具有双氮负离子配位和稳定D-A-D夹心结构的多孔金属配位聚合物材料NJUZ-1.NJUZ-1双氮配位聚合物具有优异的固氮性能。能够将空气中的氮气经光催化还原为氮。
(1)氨分子的空间构型为___________ 。
(2)光催化固氮在NJUZ-1催化剂作用下的反应机理如下(*表示吸附态)
①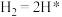
②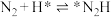 ;
;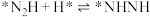 ;
;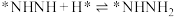 ;
;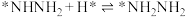 ;
;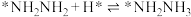 ;
;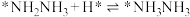
③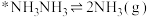
已知断裂1mol相应化学键需要的能量如下
写出光催化固氮在NJUZ-1催化剂作用下总反应的热化学方程式___________ 。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应: ΔH<0
ΔH<0
请完成下列问题:
①试比较化学平衡常数K1、K2的大小,K1___________ K2(填“>”、“<”或“=”)
②400℃时,反应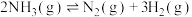 的化学平衡常数为
的化学平衡常数为___________ 。当NH3、N2和H2的物质的量分别为2mol、amol和1mol时,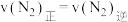 。a=
。a=___________ 。
③采用NJUZ-1将空气中的氮气经光催化还原为氨时需要将N2纯化,目的是___________ 。
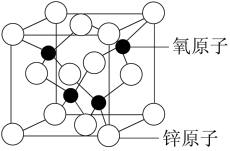
(4)氧化锌是制备NJUZ-1的重要原料之一,其结构有很多种,其中一种立方晶胞结构如图所示,Zn2+的配位数为___________ ;Zn2+周围等距且最近的Zn2+数为___________ 。
(1)氨分子的空间构型为
(2)光催化固氮在NJUZ-1催化剂作用下的反应机理如下(*表示吸附态)
①
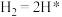
②
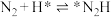 ;
;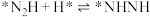 ;
;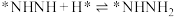 ;
;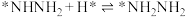 ;
;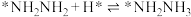 ;
;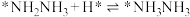
③
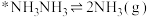
已知断裂1mol相应化学键需要的能量如下
| 化学键 |  |  |  |
| 能量 | 436kJ | 391kJ | 946kJ |
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ΔH<0
ΔH<0请完成下列问题:
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400℃时,反应
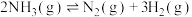 的化学平衡常数为
的化学平衡常数为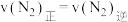 。a=
。a=③采用NJUZ-1将空气中的氮气经光催化还原为氨时需要将N2纯化,目的是
(4)氧化锌是制备NJUZ-1的重要原料之一,其结构有很多种,其中一种立方晶胞结构如图所示,Zn2+的配位数为

您最近一年使用:0次
【推荐1】含氮化合物是化工、能源、环保等领域的研究热点。回答下列问题:
(1)下图所示为利用H2O和空气中的N2以LDH超薄纳米为催化剂在光催化作用下合成氨的原理。

已知:Ⅰ.2NH3(g) N2(g)+3H2(g) ∆H=+92.4kJ/mol;Ⅱ.2H2(g)+O2(g)=2H2O(g) ∆H=—483.6kJ/mol,则上述合成氨的热化学方程式为
N2(g)+3H2(g) ∆H=+92.4kJ/mol;Ⅱ.2H2(g)+O2(g)=2H2O(g) ∆H=—483.6kJ/mol,则上述合成氨的热化学方程式为___________ 。
(2)合成尿素[CO(NH2)2]的反应为2NH3(g)+CO2(g) H2O(l)+CO(NH2)2(s) ∆H=—134kJ/mol。向恒容密闭容器中按物质的量之比4:1充入NH3和CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
H2O(l)+CO(NH2)2(s) ∆H=—134kJ/mol。向恒容密闭容器中按物质的量之比4:1充入NH3和CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。

①若用CO2的浓度变化表示反应速率,则A点的逆反应速率______ B点的正反应速率(填“>”“<”或“=”)。
②下列叙述中不能说明该反应达到平衡状态的是___________ (填选项字母)。
A.体系压强不再变化 B.气体平均摩尔质量不再变化
C.NH3的消耗速率和CO2的消耗速率之比为2:1 D.固体质量不再发生变化
③工业上合成尿素时,既能加快反应速率,又能提高平衡转化率的措施有___________ 。
A.升高温度 B.加入催化剂 C.将尿素及时分离出去 D.增大反应体系的压强
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。实验发现,NO易发生二聚反应2NO(g) N2O2(g)并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图所示。
N2O2(g)并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图所示。

①温度为T2时,达到平衡时体系的总压强为200kPa,X点N2O2的物质的量分数为___________ (保留三位有效数字),X点对应的平衡常数Kp=___________ kPa-1。
②如图所示,利用电解原理,可将废气中的NO转化为NH4NO3,阳极的电极反应式为___________ 。

(1)下图所示为利用H2O和空气中的N2以LDH超薄纳米为催化剂在光催化作用下合成氨的原理。

已知:Ⅰ.2NH3(g)
 N2(g)+3H2(g) ∆H=+92.4kJ/mol;Ⅱ.2H2(g)+O2(g)=2H2O(g) ∆H=—483.6kJ/mol,则上述合成氨的热化学方程式为
N2(g)+3H2(g) ∆H=+92.4kJ/mol;Ⅱ.2H2(g)+O2(g)=2H2O(g) ∆H=—483.6kJ/mol,则上述合成氨的热化学方程式为(2)合成尿素[CO(NH2)2]的反应为2NH3(g)+CO2(g)
 H2O(l)+CO(NH2)2(s) ∆H=—134kJ/mol。向恒容密闭容器中按物质的量之比4:1充入NH3和CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
H2O(l)+CO(NH2)2(s) ∆H=—134kJ/mol。向恒容密闭容器中按物质的量之比4:1充入NH3和CO2,使反应进行,保持温度不变,测得CO2的转化率随时间的变化情况如图所示。
①若用CO2的浓度变化表示反应速率,则A点的逆反应速率
②下列叙述中不能说明该反应达到平衡状态的是
A.体系压强不再变化 B.气体平均摩尔质量不再变化
C.NH3的消耗速率和CO2的消耗速率之比为2:1 D.固体质量不再发生变化
③工业上合成尿素时,既能加快反应速率,又能提高平衡转化率的措施有
A.升高温度 B.加入催化剂 C.将尿素及时分离出去 D.增大反应体系的压强
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。实验发现,NO易发生二聚反应2NO(g)
 N2O2(g)并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图所示。
N2O2(g)并快速达到平衡。向真空钢瓶中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图所示。
①温度为T2时,达到平衡时体系的总压强为200kPa,X点N2O2的物质的量分数为
②如图所示,利用电解原理,可将废气中的NO转化为NH4NO3,阳极的电极反应式为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有关物质间有如图所示的转化关系。已知B、D、G是常见的金属单质,E为常见的非金属单质,H常温下为无色液体,K为红棕色气体。
(1)F的电子式为______________ ,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目:_________________________________
(2)反应①的离子方程式为____________________________________________ 。
(3)C与足量G反应的化学方程式为_____________________________________ 。其中,还原剂与氧化剂的物质的量之比为____________ ,检验反应中生成的金属离子的试剂为______________ 。
(4)Al能与A发生置换反应,生成物溶质与Na2CO3不能在溶液中大量共存,用离子方程式表示其原因:__________________________________
(5)I可由某种氢化物催化氧化得到,其反应的化学方程式为_______________________________ 。
(6) 漂白粉和F都应密封保存,写出漂白粉露置于空气中失效的化学方程式:________________________________________________________________________

(1)F的电子式为
(2)反应①的离子方程式为
(3)C与足量G反应的化学方程式为
(4)Al能与A发生置换反应,生成物溶质与Na2CO3不能在溶液中大量共存,用离子方程式表示其原因:
(5)I可由某种氢化物催化氧化得到,其反应的化学方程式为
(6) 漂白粉和F都应密封保存,写出漂白粉露置于空气中失效的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】雌黄 As2S3 和雄黄 As4S4 都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有 抗病毒疗效也用来入药。
(1)砷元素有+2、+3 两种常见价态。雄黄在空气中加热至 300℃时会生成两种氧化物,其 中一种氧化物为剧毒的砒霜(As2O3),则物质 a 是_____ ,可用双氧水将 As2O3 氧化为 H3AsO4,写出该反应的化学方程式:________ 。
(2)亚砷酸 H3AsO3 可以用于治疗白血病,其在溶液中 存在多种微粒形态,25℃时,各种微粒物质的量分数与 溶液的 pH 关系如图所示。
①人体血液的 pH 在 7.35 ~7.45 之间,用药后人体中 含砷元素的主要微粒是_____ 。
②下列说法不正确的是_____ (填字母序号)。
A.n(H3AsO3):n(H2AsO3-)=1:1 时,溶液显碱性
B.25℃时,H3AsO3 的第一电离平衡常数的值 Ka1=10-5
C.在 K3AsO3 溶液中, c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
③将 KOH 溶液滴入亚砷酸溶液,当pH 调至 11 时发生反应的离子方程式 是_____ 。
(3)P 和 As 属于同主族元素,存在亚磷酸(H3PO3),该酸与足量的 NaOH 溶液反应生成Na2HPO3。工业电解 Na2HPO3 溶液可得到亚磷酸,装置示意图如下:

①产品室中反应的离子方程式为_____ ;
②得到 1mol 亚磷酸的同时,阴极室制得 NaOH 质量为_____ g。
(1)砷元素有+2、+3 两种常见价态。雄黄在空气中加热至 300℃时会生成两种氧化物,其 中一种氧化物为剧毒的砒霜(As2O3),则物质 a 是

(2)亚砷酸 H3AsO3 可以用于治疗白血病,其在溶液中 存在多种微粒形态,25℃时,各种微粒物质的量分数与 溶液的 pH 关系如图所示。
①人体血液的 pH 在 7.35 ~7.45 之间,用药后人体中 含砷元素的主要微粒是
②下列说法不正确的是
A.n(H3AsO3):n(H2AsO3-)=1:1 时,溶液显碱性
B.25℃时,H3AsO3 的第一电离平衡常数的值 Ka1=10-5
C.在 K3AsO3 溶液中, c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
③将 KOH 溶液滴入亚砷酸溶液,当pH 调至 11 时发生反应的离子方程式 是
(3)P 和 As 属于同主族元素,存在亚磷酸(H3PO3),该酸与足量的 NaOH 溶液反应生成Na2HPO3。工业电解 Na2HPO3 溶液可得到亚磷酸,装置示意图如下:

①产品室中反应的离子方程式为
②得到 1mol 亚磷酸的同时,阴极室制得 NaOH 质量为
您最近一年使用:0次



