氮气来源广泛且转化生成的工业产品(如氨、肼类等)具有重要的社会效益和经济价值。我国科学家成功制备了一类以金属锌为中心离子、具有双氮负离子配位和稳定D-A-D夹心结构的多孔金属配位聚合物材料NJUZ-1.NJUZ-1双氮配位聚合物具有优异的固氮性能。能够将空气中的氮气经光催化还原为氮。
(1)氨分子的空间构型为___________ 。
(2)光催化固氮在NJUZ-1催化剂作用下的反应机理如下(*表示吸附态)
①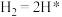
②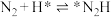 ;
;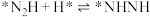 ;
;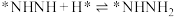 ;
;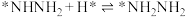 ;
;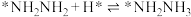 ;
;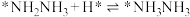
③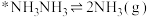
已知断裂1mol相应化学键需要的能量如下
写出光催化固氮在NJUZ-1催化剂作用下总反应的热化学方程式___________ 。
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应: ΔH<0
ΔH<0
请完成下列问题:
①试比较化学平衡常数K1、K2的大小,K1___________ K2(填“>”、“<”或“=”)
②400℃时,反应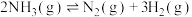 的化学平衡常数为
的化学平衡常数为___________ 。当NH3、N2和H2的物质的量分别为2mol、amol和1mol时,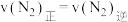 。a=
。a=___________ 。
③采用NJUZ-1将空气中的氮气经光催化还原为氨时需要将N2纯化,目的是___________ 。
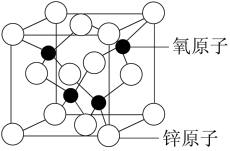
(4)氧化锌是制备NJUZ-1的重要原料之一,其结构有很多种,其中一种立方晶胞结构如图所示,Zn2+的配位数为___________ ;Zn2+周围等距且最近的Zn2+数为___________ 。
(1)氨分子的空间构型为
(2)光催化固氮在NJUZ-1催化剂作用下的反应机理如下(*表示吸附态)
①
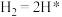
②
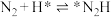 ;
;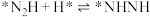 ;
;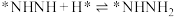 ;
;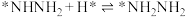 ;
;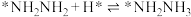 ;
;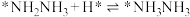
③
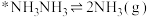
已知断裂1mol相应化学键需要的能量如下
| 化学键 |  |  |  |
| 能量 | 436kJ | 391kJ | 946kJ |
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:
 ΔH<0
ΔH<0请完成下列问题:
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②400℃时,反应
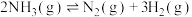 的化学平衡常数为
的化学平衡常数为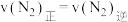 。a=
。a=③采用NJUZ-1将空气中的氮气经光催化还原为氨时需要将N2纯化,目的是
(4)氧化锌是制备NJUZ-1的重要原料之一,其结构有很多种,其中一种立方晶胞结构如图所示,Zn2+的配位数为

更新时间:2024-04-08 08:03:56
|
相似题推荐
【推荐1】我国力争于2030年前做到碳达峰。 和
和 催化重整是
催化重整是 利用的研究热点之一、该催化重整反应体系主要涉及以下反应:
利用的研究热点之一、该催化重整反应体系主要涉及以下反应:
反应Ⅰ:主反应


反应Ⅱ:副反应

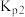
反应Ⅲ:积碳反应

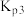
反应Ⅳ:积碳反应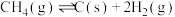

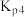
(1)有关化学键键能数据如表:
已知CO中含有的化学键为C≡O,则反应Ⅱ的
_______ kJ/mol。
(2)下列关于该重整反应体系的说法正确的是_______(填字母)。
(3)恒温下,往2L密闭容器中加入2mol 、2mol
、2mol 进行该催化重整反应(不考虑除主反应外的其他反应),2min后测得
进行该催化重整反应(不考虑除主反应外的其他反应),2min后测得 的转化率为40%,则2min内平均反应速率
的转化率为40%,则2min内平均反应速率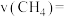
_______  。
。
(4)设 为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应Ⅲ、Ⅳ的
为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应Ⅲ、Ⅳ的 随
随 (T表示温度)的变化如图所示。据图判断,反应Ⅰ的
(T表示温度)的变化如图所示。据图判断,反应Ⅰ的
_______ 0(填“大于”“小于”或“等于”),说明判断的理由_______ 。

(5)在恒温、体系总压恒定为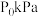 下,往密闭容器中加入
下,往密闭容器中加入 、
、 进行该催化重整反应(不考虑除主反应外的其他反应),达到平衡状态时,
进行该催化重整反应(不考虑除主反应外的其他反应),达到平衡状态时, 的转化率为50%。则该温度下的平衡常数
的转化率为50%。则该温度下的平衡常数
_______  (用含
(用含 的代数式表示)。
的代数式表示)。
 和
和 催化重整是
催化重整是 利用的研究热点之一、该催化重整反应体系主要涉及以下反应:
利用的研究热点之一、该催化重整反应体系主要涉及以下反应:反应Ⅰ:主反应



反应Ⅱ:副反应


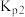
反应Ⅲ:积碳反应


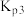
反应Ⅳ:积碳反应
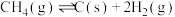

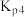
(1)有关化学键键能数据如表:
| 化学键 | H—H | H—O | C=O | C≡O |
键能/ | 436 | 463 | 803 | 1076 |
已知CO中含有的化学键为C≡O,则反应Ⅱ的

(2)下列关于该重整反应体系的说法正确的是_______(填字母)。
A.加入催化剂,可提高 的平衡转化率 的平衡转化率 |
B.增大 的浓度,反应Ⅰ、Ⅱ的正反应速率均增加 的浓度,反应Ⅰ、Ⅱ的正反应速率均增加 |
C.随着投料比 的增大,达到平衡时 的增大,达到平衡时 的转化率增大 的转化率增大 |
| D.在一定条件下建立平衡后,移去部分积碳,反应Ⅲ和反应Ⅳ平衡均向右移动 |
 、2mol
、2mol 进行该催化重整反应(不考虑除主反应外的其他反应),2min后测得
进行该催化重整反应(不考虑除主反应外的其他反应),2min后测得 的转化率为40%,则2min内平均反应速率
的转化率为40%,则2min内平均反应速率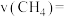
 。
。(4)设
 为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应Ⅲ、Ⅳ的
为分压平衡常数(用分压代替浓度,气体分压=总压×该组分的物质的量分数),反应Ⅲ、Ⅳ的 随
随 (T表示温度)的变化如图所示。据图判断,反应Ⅰ的
(T表示温度)的变化如图所示。据图判断,反应Ⅰ的

(5)在恒温、体系总压恒定为
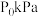 下,往密闭容器中加入
下,往密闭容器中加入 、
、 进行该催化重整反应(不考虑除主反应外的其他反应),达到平衡状态时,
进行该催化重整反应(不考虑除主反应外的其他反应),达到平衡状态时, 的转化率为50%。则该温度下的平衡常数
的转化率为50%。则该温度下的平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐2】丙烯是一种重要的化工原料,可以由丙烷在催化剂作用下,制得:
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):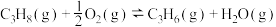
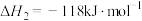
(1)已知键能: ,
,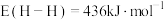 ,
, 。由此计算:
。由此计算: 分子中共价键的键能为
分子中共价键的键能为_______ 。
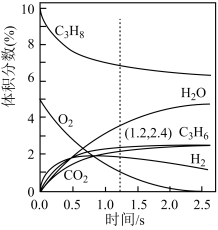
(2)在一定温度和总压恒定的条件下,向反应装置通入气体浓度比为 的混合气体(
的混合气体( 不参加反应),各组分气体的体积分数随时间的变化关系如图所示;反应一段时间后,实验测得消耗的
不参加反应),各组分气体的体积分数随时间的变化关系如图所示;反应一段时间后,实验测得消耗的 和
和 的质量之比小于2.75的原因可能是
的质量之比小于2.75的原因可能是_______ 。
(3)恒温刚性密闭容器中通入气体分压比为 的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
反应Ⅱ: k
k
反应Ⅲ: k′
k′
实验测得丙烯的净生成速率方程为: ,试推测丙烯的浓度随时间的变化,在图中画出变化趋势图
,试推测丙烯的浓度随时间的变化,在图中画出变化趋势图_______ 。

(4)关于上述反应,下列说法不正确 的是_______。
(5)已知:ⅰ.一般来说,在过氧化物( )存在下,丙烯与HBr发生自由基机理的反马氏加成反应生成1-溴丙烷:
)存在下,丙烯与HBr发生自由基机理的反马氏加成反应生成1-溴丙烷:
ⅱ.以 作溶剂,光、热或过氧化物存在时,丙烯与HBr、NBS固体可发生自由基机理的取代反应(固体表面):
作溶剂,光、热或过氧化物存在时,丙烯与HBr、NBS固体可发生自由基机理的取代反应(固体表面):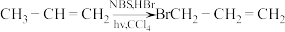 。NBS固体
。NBS固体极易 与HBr快速反应生成 ,进而生成溴自由基(用
,进而生成溴自由基(用 表示)发生后续反应。
表示)发生后续反应。
①若过氧化物存在下,丙烯与HBr的反马氏加成反应的机理如下:
引发阶段:
Ⅰ.
Ⅱ._______;
链的传递:
Ⅲ. CH3-CH=CH2+Br·→C H3-CH-CH2Br
Ⅳ. CH3-C H-CH2Br+HBr→CH3-CH2-CH2Br+Br·
链的终止:(若自由基之间相互结合或被反应容器壁所捕获,链反应即行终止)
请你补充引发阶段步骤Ⅱ:_______ 。按此机理分析预测,写出可能生成的另两种有机物的结构简式_______ 、_______ 。
②在满足上述自由基反应的条件下,丙烯与HBr的加成和取代反应存在竞争关系,两个反应的进程和能量系如图所示:

请说明在不同条件下两者反应主要产物不同的原因:_______ 。
反应Ⅰ(直接脱氢):


反应Ⅱ(氧化脱氢):
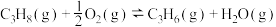
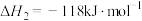
(1)已知键能:
 ,
,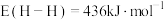 ,
, 。由此计算:
。由此计算: 分子中共价键的键能为
分子中共价键的键能为(2)在一定温度和总压恒定的条件下,向反应装置通入气体浓度比为
 的混合气体(
的混合气体( 不参加反应),各组分气体的体积分数随时间的变化关系如图所示;反应一段时间后,实验测得消耗的
不参加反应),各组分气体的体积分数随时间的变化关系如图所示;反应一段时间后,实验测得消耗的 和
和 的质量之比小于2.75的原因可能是
的质量之比小于2.75的原因可能是
(3)恒温刚性密闭容器中通入气体分压比为
 的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):
的混合气体,已知某反应条件下只发生如下反应(k,k′为速率常数):反应Ⅱ:
 k
k反应Ⅲ:
 k′
k′实验测得丙烯的净生成速率方程为:
 ,试推测丙烯的浓度随时间的变化,在图中画出变化趋势图
,试推测丙烯的浓度随时间的变化,在图中画出变化趋势图
(4)关于上述反应,下列说法
A.总压恒定时,通 过多或过少都会降低丙烯的产率 过多或过少都会降低丙烯的产率 |
B.将空气经碱液净化处理后,按合适比例与 混合,可作原料气制丙烯 混合,可作原料气制丙烯 |
C.提高原料气中 的体积分数,能使反应Ⅱ平衡右移,一定能提高丙烯产率 的体积分数,能使反应Ⅱ平衡右移,一定能提高丙烯产率 |
| D.实际生产过程中,应该根据反应达平衡后丙烯的体积分数最大值确定反应的温度 |
 )存在下,丙烯与HBr发生自由基机理的反马氏加成反应生成1-溴丙烷:
)存在下,丙烯与HBr发生自由基机理的反马氏加成反应生成1-溴丙烷:
ⅱ.以
 作溶剂,光、热或过氧化物存在时,丙烯与HBr、NBS固体可发生自由基机理的取代反应(固体表面):
作溶剂,光、热或过氧化物存在时,丙烯与HBr、NBS固体可发生自由基机理的取代反应(固体表面):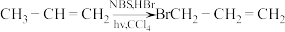 。NBS固体
。NBS固体 ,进而生成溴自由基(用
,进而生成溴自由基(用 表示)发生后续反应。
表示)发生后续反应。①若过氧化物存在下,丙烯与HBr的反马氏加成反应的机理如下:
引发阶段:
Ⅰ.

Ⅱ._______;
链的传递:
Ⅲ. CH3-CH=CH2+Br·→
Ⅳ.
链的终止:(若自由基之间相互结合或被反应容器壁所捕获,链反应即行终止)
请你补充引发阶段步骤Ⅱ:
②在满足上述自由基反应的条件下,丙烯与HBr的加成和取代反应存在竞争关系,两个反应的进程和能量系如图所示:

请说明在不同条件下两者反应主要产物不同的原因:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】化学固定、催化活化循环利用 的研究,备受重视。铜基催化剂上
的研究,备受重视。铜基催化剂上 加氢合成甲醇是重要的利用途径。该工艺主要发生合成甲醇的反应Ⅰ和逆水汽变换反应Ⅱ。
加氢合成甲醇是重要的利用途径。该工艺主要发生合成甲醇的反应Ⅰ和逆水汽变换反应Ⅱ。
I.
II.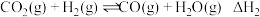
已知甲醇的选择性
(1)反应I能自发进行的条件是___________ 。(填“低温”或“高温”或“任意温度”)
(2)根据下表中的键能数据,计算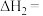
___________ 。
(3)恒温恒容条件下,原料气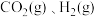 以物质的量浓度1∶3投料,甲醇的选择性为50%。已知初始
以物质的量浓度1∶3投料,甲醇的选择性为50%。已知初始 ,
, 平衡转化率为50%,则该条件下反应I的平衡常数
平衡转化率为50%,则该条件下反应I的平衡常数
_______ 。
(4)已知催化剂表面金属能吸附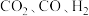 分子,反应I和II发生在催化剂表面的不同活性位点。在
分子,反应I和II发生在催化剂表面的不同活性位点。在 、
、 条件下,将原料气按照a、b、c、d四种方式以相同流速通过催化剂,测得各组分转化率(X)和选择性(S)如下表所示。
条件下,将原料气按照a、b、c、d四种方式以相同流速通过催化剂,测得各组分转化率(X)和选择性(S)如下表所示。
原料气组成与转化率和选择性的关系
①由上表数据可知,其他条件一定时,原料气中 体积分数越大,生成的甲醇
体积分数越大,生成的甲醇___________ 越多(填“一定”或“不一定”)
②根据上表数据,推测随着原料气中掺杂 体积分数的增大,
体积分数的增大, 转化率迅速降低的原因是
转化率迅速降低的原因是___________ 。
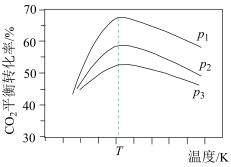
③在催化剂作用下发生上述反应I、II,达平衡时 的转化率随温度和压强的变化如右图所示,则
的转化率随温度和压强的变化如右图所示,则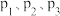 由大到小的顺序为
由大到小的顺序为___________ ,当压强一定时, 的平衡转化率呈现如图变化的原因是
的平衡转化率呈现如图变化的原因是___________ 。
 的研究,备受重视。铜基催化剂上
的研究,备受重视。铜基催化剂上 加氢合成甲醇是重要的利用途径。该工艺主要发生合成甲醇的反应Ⅰ和逆水汽变换反应Ⅱ。
加氢合成甲醇是重要的利用途径。该工艺主要发生合成甲醇的反应Ⅰ和逆水汽变换反应Ⅱ。I.

II.
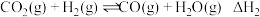
已知甲醇的选择性

(1)反应I能自发进行的条件是
(2)根据下表中的键能数据,计算
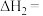
| 化学键 |  |  |  |  |
键能/ | 436 | 1071 | 464 | 803 |
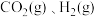 以物质的量浓度1∶3投料,甲醇的选择性为50%。已知初始
以物质的量浓度1∶3投料,甲醇的选择性为50%。已知初始 ,
, 平衡转化率为50%,则该条件下反应I的平衡常数
平衡转化率为50%,则该条件下反应I的平衡常数
(4)已知催化剂表面金属能吸附
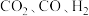 分子,反应I和II发生在催化剂表面的不同活性位点。在
分子,反应I和II发生在催化剂表面的不同活性位点。在 、
、 条件下,将原料气按照a、b、c、d四种方式以相同流速通过催化剂,测得各组分转化率(X)和选择性(S)如下表所示。
条件下,将原料气按照a、b、c、d四种方式以相同流速通过催化剂,测得各组分转化率(X)和选择性(S)如下表所示。原料气组成与转化率和选择性的关系
原料气(体积分数)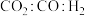 (%) (%) | 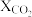 | 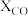 | 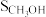 |  |
| (a)16∶0∶84 | 18 | 0 | 43 | 56 |
| (b)16∶0.6∶83.4 | 12 | 0 | 61 | 38 |
| (c)16∶2∶82 | 11 | 0 | 89 | 11 |
| (d)16∶4∶80 | 9 | 6.0 | 99 | 0 |
 体积分数越大,生成的甲醇
体积分数越大,生成的甲醇②根据上表数据,推测随着原料气中掺杂
 体积分数的增大,
体积分数的增大, 转化率迅速降低的原因是
转化率迅速降低的原因是③在催化剂作用下发生上述反应I、II,达平衡时
 的转化率随温度和压强的变化如右图所示,则
的转化率随温度和压强的变化如右图所示,则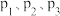 由大到小的顺序为
由大到小的顺序为 的平衡转化率呈现如图变化的原因是
的平衡转化率呈现如图变化的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】氢能是一种理想的绿色能源,一种太阳能两步法甲烷蒸气重整制氢原理合成示意图如下:

回答下列问题:
(1)第Ⅰ步:NiFe2O4(s)+CH4(g) NiO(s)+2FeO(s)+CO(g)+2H2(g)
NiO(s)+2FeO(s)+CO(g)+2H2(g)  =a kJ·mol-1。总反应可表示为:CH4(g)+H2O(g)
=a kJ·mol-1。总反应可表示为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)  =b kJ·mol-1。写出第Ⅱ步反应的热化学方程式:
=b kJ·mol-1。写出第Ⅱ步反应的热化学方程式:___________ 。
(2)实验测得分步制氢比直接利用CH4和H2O(g)反应具有更高的反应效率,原因是___________ 。
(3)第Ⅰ、Ⅱ步反应的lgKp-T图象如下。

由图象可知a___________ b(填“大于”或“小于”),1000℃时,第Ⅱ步反应的化学平衡常数K=___________ ,测得该温度下第Ⅰ步反应平衡时CH4的平衡分压p(CH4)=4.0kPa,则平衡混合气体中H2的体积分数为___________ (保留一位小数)。

(4)第Ⅰ步反应产生的合成气(CO和H2的混合气体)可用于F-T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应CO+H2O(g) CO2+H2,如图为相同条件下用不同催化剂在不同时间段测得反应体系内CO2的体积分数,据此应选择的催化剂是
CO2+H2,如图为相同条件下用不同催化剂在不同时间段测得反应体系内CO2的体积分数,据此应选择的催化剂是___________ (填“Ⅰ”或“Ⅱ”),选择的依据是___________ 。

回答下列问题:
(1)第Ⅰ步:NiFe2O4(s)+CH4(g)
 NiO(s)+2FeO(s)+CO(g)+2H2(g)
NiO(s)+2FeO(s)+CO(g)+2H2(g)  =a kJ·mol-1。总反应可表示为:CH4(g)+H2O(g)
=a kJ·mol-1。总反应可表示为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)  =b kJ·mol-1。写出第Ⅱ步反应的热化学方程式:
=b kJ·mol-1。写出第Ⅱ步反应的热化学方程式:(2)实验测得分步制氢比直接利用CH4和H2O(g)反应具有更高的反应效率,原因是
(3)第Ⅰ、Ⅱ步反应的lgKp-T图象如下。

由图象可知a

(4)第Ⅰ步反应产生的合成气(CO和H2的混合气体)可用于F-T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应CO+H2O(g)
 CO2+H2,如图为相同条件下用不同催化剂在不同时间段测得反应体系内CO2的体积分数,据此应选择的催化剂是
CO2+H2,如图为相同条件下用不同催化剂在不同时间段测得反应体系内CO2的体积分数,据此应选择的催化剂是
您最近一年使用:0次
【推荐2】以NOx为主要成分的雾霾综合治理是当前重要的研究课题,其中汽车尾气的处理尤为重要。请回答下列问题:
(1)某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理示意图如下。

已知:2NO2(g) N2O4(g) ΔH<0,下列说法错误的是__________
N2O4(g) ΔH<0,下列说法错误的是__________
(2)NO和CO均为汽车尾气的成分,在催化转换器中可发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g) ,已知该反应为自发反应,则该反应的反应热ΔH
N2(g)+2CO2(g) ,已知该反应为自发反应,则该反应的反应热ΔH___________ 0(填“>”或“<”或“=”)。
(3)已知:N2(g) + O2(g)=2NO(g) ΔH= a kJ·mol-1
C(s) + O2(g)=CO2(g) ΔH= b kJ·mol-1
2C(s) + O2(g)=2CO(g) ΔH= c kJ·mol-1
则2CO(g)+2NO(g) N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=___________ kJ·mol-1 (用含a、b、c的表达式表示)。
(4)一定温度下,将2 mol CO、4 mol NO充入2 L密闭容器。5 min到达平衡,测得N2的物质的量为0.5 mol,则:
①5min内v(NO)=___________ 。该反应的平衡常数的数值为K=___________ (保留两位小数)。
②该条件下,可判断此反应到达平衡的标志是______
A.单位时间内,消耗2 mol CO同时形成1 mol N2
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.CO与NO的转化率比值不再改变
(5)某研究小组探究催化剂Ⅰ、Ⅱ对CO、NO转化的影响。将CO和NO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________ 。
②温度低于200℃时,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因是___________ 。
(6)在酸性溶液中,间接电化学法可对NO进行无害化处理,其工作原理如图所示。

①阳极反应为:___________ ;
②为使电解产物全部转化为NH4NO3,需要补充物质A,A是___________ 。
(1)某MOFs多孔材料孔径大小和形状恰好将N2O4“固定”,能高选择性吸附NO2。废气中的NO2被吸附后,经处理能全部转化为HNO3。原理示意图如下。

已知:2NO2(g)
 N2O4(g) ΔH<0,下列说法错误的是__________
N2O4(g) ΔH<0,下列说法错误的是__________| A.温度升高时不利于NO2吸附 |
B.多孔材料“固定”N2O4,促进2NO2(g) N2O4(g)平衡正向移动 N2O4(g)平衡正向移动 |
| C.转化为HNO3的反应是2N2O4 + O2 + 2H2O = 4HNO3 |
| D.每获得0.4mol HNO3时,转移电子的数目为6.02×1022 |
(2)NO和CO均为汽车尾气的成分,在催化转换器中可发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g) ,已知该反应为自发反应,则该反应的反应热ΔH
N2(g)+2CO2(g) ,已知该反应为自发反应,则该反应的反应热ΔH(3)已知:N2(g) + O2(g)=2NO(g) ΔH= a kJ·mol-1
C(s) + O2(g)=CO2(g) ΔH= b kJ·mol-1
2C(s) + O2(g)=2CO(g) ΔH= c kJ·mol-1
则2CO(g)+2NO(g)
 N2(g)+2CO2(g) ΔH=
N2(g)+2CO2(g) ΔH=(4)一定温度下,将2 mol CO、4 mol NO充入2 L密闭容器。5 min到达平衡,测得N2的物质的量为0.5 mol,则:
①5min内v(NO)=
②该条件下,可判断此反应到达平衡的标志是
A.单位时间内,消耗2 mol CO同时形成1 mol N2
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.CO与NO的转化率比值不再改变
(5)某研究小组探究催化剂Ⅰ、Ⅱ对CO、NO转化的影响。将CO和NO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:

①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为
②温度低于200℃时,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因是
(6)在酸性溶液中,间接电化学法可对NO进行无害化处理,其工作原理如图所示。

①阳极反应为:
②为使电解产物全部转化为NH4NO3,需要补充物质A,A是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】煤的气化是一种重要的制氢途径。生成水煤气的反应如下:
Ⅰ。

Ⅱ。

回答下列问题:
(1)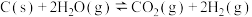 的
的
___________ 。
(2)恒温恒容下,下列关于反应Ⅱ的说法正确的是___________(填标号)。
(3)在一定温度下,向1L密闭容器中加入足量的C(s)和amol (g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡,
(g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡, (g)的转化率为50%,此时CO的物质的量为bmol。
(g)的转化率为50%,此时CO的物质的量为bmol。
①0~tmin内, 的平均反应速率为
的平均反应速率为___________  ;
;
②反应Ⅱ的平衡常数
___________ 。
(4)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下:
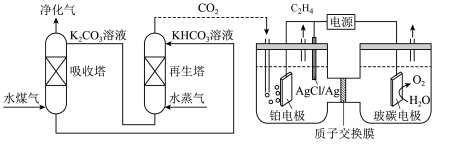
①吸收塔中 溶液的作用是吸收
溶液的作用是吸收 ,反应的离子方程式为
,反应的离子方程式为___________ ;
②阳极反应式为___________ 。
Ⅰ。


Ⅱ。


回答下列问题:
(1)
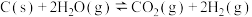 的
的
(2)恒温恒容下,下列关于反应Ⅱ的说法正确的是___________(填标号)。
| A.压强保持不变时,说明该反应已达平衡 |
| B.平衡时向容器中充入惰性气体,平衡不移动 |
| C.混合气体的平均摩尔质量不变时,说明该反应已达平衡 |
D.平衡时向容器中充入 (g),平衡正向移动 (g),平衡正向移动 |
 (g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡,
(g)发生反应Ⅰ、Ⅱ,经过tmin达到平衡, (g)的转化率为50%,此时CO的物质的量为bmol。
(g)的转化率为50%,此时CO的物质的量为bmol。①0~tmin内,
 的平均反应速率为
的平均反应速率为 ;
;②反应Ⅱ的平衡常数

(4)一种脱除和利用水煤气中
 方法的示意图如下:
方法的示意图如下:
①吸收塔中
 溶液的作用是吸收
溶液的作用是吸收 ,反应的离子方程式为
,反应的离子方程式为②阳极反应式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】据世界权威刊物《自然》最近报道,选择碲化锆 (ZrTe5) 为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。Te属于ⅥA族元素。回答下列问题:
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是_______ ,Zr2+的价层电子轨道表示式是_______ 。
(2)Zr、Te、Cl的电负性由大到小的顺序是_______ ,H2O、H2Se、H2Te的沸点由高到低的顺序是_______ 酸性强弱比较: H2SO4_______ H2TeO4 (填“>”或“<”)。
(3)H2Te和CO2均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是_______ 。
(4)[Zr(C2H5O)2]2+是 Zr4+形成的一种配离子,其中的配位原子是_______ (填原子符号),1个[Zr(C2H5O)2]2+离子中含共价键的数目是_______ 。
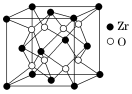
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr原子的配位数是_______ 。 若晶胞中距离最近的两个氧原子间的距离为a nm,则立方氧化锆的密度为_______ g·cm-3 (写出计算表达式)。
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是
(2)Zr、Te、Cl的电负性由大到小的顺序是
(3)H2Te和CO2均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是
(4)[Zr(C2H5O)2]2+是 Zr4+形成的一种配离子,其中的配位原子是
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr原子的配位数是

您最近一年使用:0次
【推荐2】2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画,《千里江山图》之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
(1)石青,又名蓝矿石,化学式为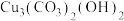 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有______ 种, 的空间构型为
的空间构型为________ 。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为________ 。
(2)亚铁氰化钾,化学式为 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是________ (填元素符号), 中C原子的杂化方式
中C原子的杂化方式_______ , 中σ键和π键的数目之比为
中σ键和π键的数目之比为________ 。
(3) 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
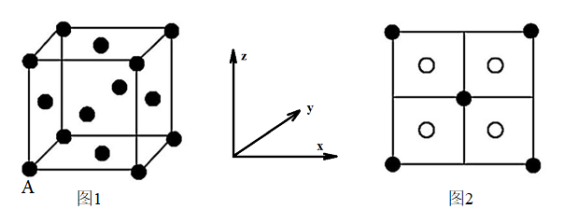
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是______ , 配位数为
配位数为________ 。已知图1中A原子的原子分数坐标为(0,0,0),则与A原子距离最近的 的原子分数坐标为
的原子分数坐标为________ 。若晶胞参数anm,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为________ (用含a和d的式子表示)。
(1)石青,又名蓝矿石,化学式为
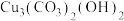 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有 的空间构型为
的空间构型为 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)亚铁氰化钾,化学式为
 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是 中C原子的杂化方式
中C原子的杂化方式 中σ键和π键的数目之比为
中σ键和π键的数目之比为(3)
 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是 配位数为
配位数为 的原子分数坐标为
的原子分数坐标为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)在第二周期中,第一电离能比N高的主族元素是_______ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是_______ (填序号)。
A. B.
B.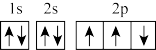
C.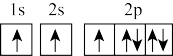 D.
D.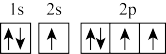
(2)科学家从(NH4)2SO4中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 的空间构型与NH
的空间构型与NH 相同,则1个N4H
相同,则1个N4H 中含有
中含有_______ 个σ键。
(3)科学家合成了一种阳离子为“N ”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为N8的离子晶体,其阳离子电子式为
”化学式为N8的离子晶体,其阳离子电子式为_______ ,阴离子的空间构型为_______ 。
(4)GaN、GaP、GaAs熔融状态均不导电,熔点如表所示。其中GaN晶胞如图所示,结构可看作金刚石晶胞内部的碳原子被N原子代替(如b),顶点和面心的碳原子被Ga原子代替(如a)。

①试分析GaN、GaP、GaAs熔点依次降低的原因:_______ ;
②GaN晶胞中与Ga原子周围与它最近且相等距离的Ga原子有_______ 个。
(1)在第二周期中,第一电离能比N高的主族元素是
A.
 B.
B.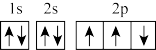
C.
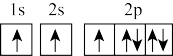 D.
D.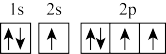
(2)科学家从(NH4)2SO4中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO
 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 的空间构型与NH
的空间构型与NH 相同,则1个N4H
相同,则1个N4H 中含有
中含有(3)科学家合成了一种阳离子为“N
 ”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的,5个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为N8的离子晶体,其阳离子电子式为
”化学式为N8的离子晶体,其阳离子电子式为(4)GaN、GaP、GaAs熔融状态均不导电,熔点如表所示。其中GaN晶胞如图所示,结构可看作金刚石晶胞内部的碳原子被N原子代替(如b),顶点和面心的碳原子被Ga原子代替(如a)。

| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
②GaN晶胞中与Ga原子周围与它最近且相等距离的Ga原子有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】第一代半导体材料(Si. Ge等)与第二代半导体材料(GaAs、 InSb等)一起,将人类推进了信息时代。近年来,以碳化硅( SiC)、氮化镓(GaN)为代表的第三代半导体材料的出现,开辟了人类资源和能源节约型社会的新发展,也成为了科学家研究的热点。
(1)基态锗原子的价电子排布图为_____ 。
(2)N、P、As位于同一主族,基态氮原子的核外共有____ 种不同运动状态的电子,N20的空间构型为____ ,与P043-互为等电子体的分子有 ____ (填一种即可)。
(3)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。

酞菁钴中碳原子的杂化轨道类型为____ ;与钴离子通过配位键结合的氮原子的编号是_____ 。
(4)已知PH3分子的键角约为94°,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因_____________________ 。
(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有______ 。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:

试从结构的角度分析它们熔点不同的原因___________________ 。
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为d pm,NA代表阿伏伽德罗常数 的值,则磷化铝晶体的密度ρ=____ g/cm3。

(1)基态锗原子的价电子排布图为
(2)N、P、As位于同一主族,基态氮原子的核外共有
(3)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。

酞菁钴中碳原子的杂化轨道类型为
(4)已知PH3分子的键角约为94°,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因
(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:

试从结构的角度分析它们熔点不同的原因
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为d pm,NA代表阿伏伽德罗常数 的值,则磷化铝晶体的密度ρ=

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】污染物的处理和资源的充分利用是化学重要的研究课题,工业上用化工厂尾气中低浓度 还原软锰矿(主要成分为
还原软锰矿(主要成分为 ,另含有少量铁、铝、铜、镍、铅等金属化合物)制备高性能磁性材料的主要原料
,另含有少量铁、铝、铜、镍、铅等金属化合物)制备高性能磁性材料的主要原料 的流程如下:
的流程如下: 如下
如下
② 难溶于水、乙醇,潮湿时易被空气氧化,
难溶于水、乙醇,潮湿时易被空气氧化, 时开始分解;
时开始分解;
③溶液中某离子的浓度 时,即可认为该离子已沉淀完全。
时,即可认为该离子已沉淀完全。
(1)基态锰原子的价电子排布式为___________ , 的空间结构为
的空间结构为___________ 。
(2)为提高“还原酸浸”的效率,可以采取的措施有___________ (答出一条即可);上述流程多次涉及过滤操作,实验室进行过滤操作时需要用到的玻璃仪器有烧杯、___________ 。
(3)“还原酸浸”中所发生的最主要的氧化还原反应的离子方程式为___________ 。
(4)“除铜镍铅”时,为使它们完全沉淀,需控制溶液中 的浓度的最小值为
的浓度的最小值为___________ mol/L。
(5)“洗涤、干燥”中,为减少损失,宜选用的洗涤剂为___________ 。
(6)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为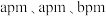 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
___________ ,该晶体的密度为___________  。
。
 还原软锰矿(主要成分为
还原软锰矿(主要成分为 ,另含有少量铁、铝、铜、镍、铅等金属化合物)制备高性能磁性材料的主要原料
,另含有少量铁、铝、铜、镍、铅等金属化合物)制备高性能磁性材料的主要原料 的流程如下:
的流程如下:
 如下
如下| 难溶物 |  |  |  |  |
 |  |  | 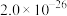 | 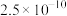 |
 难溶于水、乙醇,潮湿时易被空气氧化,
难溶于水、乙醇,潮湿时易被空气氧化, 时开始分解;
时开始分解;③溶液中某离子的浓度
 时,即可认为该离子已沉淀完全。
时,即可认为该离子已沉淀完全。(1)基态锰原子的价电子排布式为
 的空间结构为
的空间结构为(2)为提高“还原酸浸”的效率,可以采取的措施有
(3)“还原酸浸”中所发生的最主要的氧化还原反应的离子方程式为
(4)“除铜镍铅”时,为使它们完全沉淀,需控制溶液中
 的浓度的最小值为
的浓度的最小值为(5)“洗涤、干燥”中,为减少损失,宜选用的洗涤剂为
(6)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为
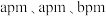 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】前四周期很多元素在工业及生活方面有很多重要应用。回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构简式如图:
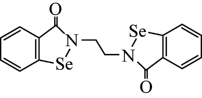
①基态 原子的核外电子有
原子的核外电子有____ 种空间运动状态。
②该新药分子中有_____ 种不同化学环境的H原子。
③比较键角大小:气态SeO3分子____ SeO 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是_____ 。
(2)“钛”被称为21世纪金属,基态钛原子价电子的排布图为____ 。
(3)CrO5中有4个-1价的O。CrO5中π键与σ键个数比为____ 。
(4)[Co(NH3)4Cl2]+呈八面体结构,其中Co3+采取的杂化类型为____ (填编号①dsp2、②sp3d、③sp3d2)。能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是____ (填标号)。
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(5)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是____ (填元素符号),写出与CN-互为等电子体的一种分子的化学式为____ 。
(6)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为( ,
, ,0)。此晶胞中与n点最远的S的坐标为
,0)。此晶胞中与n点最远的S的坐标为____ 。若Zn与S弹性相切,其半径分别为apm和bpm,则ZnS的密度为____ g•cm-3(用含a、b、NA的式子表示)。

(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构简式如图:

①基态
 原子的核外电子有
原子的核外电子有②该新药分子中有
③比较键角大小:气态SeO3分子
 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)“钛”被称为21世纪金属,基态钛原子价电子的排布图为
(3)CrO5中有4个-1价的O。CrO5中π键与σ键个数比为
(4)[Co(NH3)4Cl2]+呈八面体结构,其中Co3+采取的杂化类型为
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(5)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是
(6)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为(
 ,
, ,0)。此晶胞中与n点最远的S的坐标为
,0)。此晶胞中与n点最远的S的坐标为
您最近一年使用:0次



