氮(N)、磷(P)、砷(As)等第VA族元素的化合物在研究和生产中有重要用途,请回答下列问题:
(1)第三周期元素的原子中,第一电离能大于磷原子的有_______ 种。
(2)氮族元素氯化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(RH3)性质可能有_______ (填序号)。
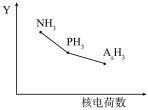
A.稳定性 B.沸点 C.R−H键之间的键角 D.分子间作用力 E.还原性
(3)经测定发现,某种N2O5固体由NO 和
和 两种离子组成,阳离子中N原子的杂化方式是
两种离子组成,阳离子中N原子的杂化方式是_______ 杂化,阴离子的空间构型为_______ 。
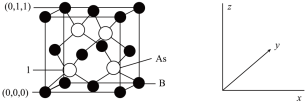
(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如下图所示,则1号砷原子的坐标为_______ 。已知阿伏加德罗常数的值为NA,若晶胞参数为apm,则该晶体的密度为_______ g·cm−3(列出含a、NA的计算式即可)。
(1)第三周期元素的原子中,第一电离能大于磷原子的有
(2)氮族元素氯化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(RH3)性质可能有

A.稳定性 B.沸点 C.R−H键之间的键角 D.分子间作用力 E.还原性
(3)经测定发现,某种N2O5固体由NO
 和
和 两种离子组成,阳离子中N原子的杂化方式是
两种离子组成,阳离子中N原子的杂化方式是(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如下图所示,则1号砷原子的坐标为

更新时间:2022-04-21 19:08:34
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期元素A、B、C、D、E在元素周期表中的位置如图所示,其中E的原子半径是同周期主族元素中最小的。请回答下列问题:

(1)A元素用于考古学的一种核素的符号为___ 。
(2)B元素最简单氢化物的化学式是__ ,溶于水后溶液呈___ (填“酸性”“碱性”或“中性”)。
(3)元素C与氢形成的原子比为1:1的化合物中___ (填“含有”或“没有”)非极性键,实验室常用该化合物的溶液加少量MnO2制取C的单质,该反应中MnO2作___ (填“氧化剂”“还原剂”或“催化剂”)。
(4)D的元素符号是__ ,高纯D的单质在电子工业上是一种良好的___ (填“导体”或“半导体)材料,A与D的非金属性比较:A__ D(填“>”或“<”)。
(5)B的最简单氢化物与E的氢化物在溶液中反应的离子方程式___ 。

(1)A元素用于考古学的一种核素的符号为
(2)B元素最简单氢化物的化学式是
(3)元素C与氢形成的原子比为1:1的化合物中
(4)D的元素符号是
(5)B的最简单氢化物与E的氢化物在溶液中反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
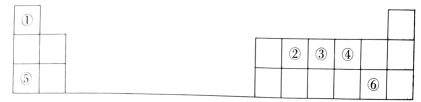
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】短周期主族元素X、Y、Z和M的原子序数依次增大,相关信息如下表:
请回答下列问题:
(1)Z的元素符号是_______ ,X元素灼烧时火焰呈现的颜色是_______ 。
(2)Y原子的得电子能力比Z原子的得电子能力_______ (填“强”或“弱”),原因是_______ (从原子结构角度分析)。
(3)写出X的单质在单质 中燃烧的化学方程式:
中燃烧的化学方程式:_______ ,单质 ,与单质
,与单质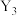 的关系是
的关系是_______ 。
(4)设计实验比较X与M原子的失电子能力强弱:_______ 。
| 元素 | 相关信息 |
| X | 最外层电子数是核外电子总数的 |
| Y | 地壳中含量最多的元素 |
| Z | Z的质子数比Y的质子数多1 |
| M | M与X同主族 |
(1)Z的元素符号是
(2)Y原子的得电子能力比Z原子的得电子能力
(3)写出X的单质在单质
 中燃烧的化学方程式:
中燃烧的化学方程式: ,与单质
,与单质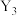 的关系是
的关系是(4)设计实验比较X与M原子的失电子能力强弱:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
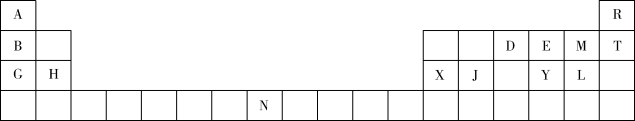
回答下列问题:
(1)D的简单气态氢化物的VSEPR模型为_______ 。
(2)第一电离能H_______ X(填“>”“<”或“=”),其原因是_______ 。
(3)电负性E_______ M(填“>”“<”或“=”)。
(4)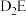 的沸点比
的沸点比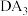 的沸点低,其原因是
的沸点低,其原因是_______ 。
(5)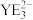 的键角比
的键角比 的键角小的原因是
的键角小的原因是_______ 。

回答下列问题:
(1)D的简单气态氢化物的VSEPR模型为
(2)第一电离能H
(3)电负性E
(4)
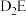 的沸点比
的沸点比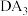 的沸点低,其原因是
的沸点低,其原因是(5)
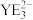 的键角比
的键角比 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
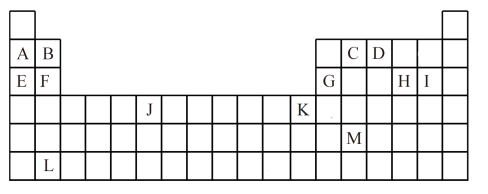
试回答下列问题:
(1)一个J原子(基态)中未成对电子数为_____ ,L的原子序数为_____ ,M的简化电子排布式为_____ 。
(2)K位于元素周期表中第_____ 周期、_____ 族,属于_____ 区元素;
(3)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式_____ 。
(4)下列有关说法正确的是_____

试回答下列问题:
(1)一个J原子(基态)中未成对电子数为
(2)K位于元素周期表中第
(3)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式
(4)下列有关说法正确的是_____
A.第一电离能 | B.电负性 |
C.原子半径 | D.最高价含氧酸的酸性 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
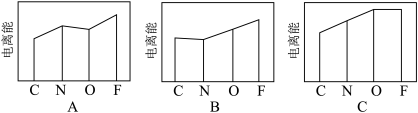
(1)图A、B、C分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同),第一电离能I1的变化图是_______ 。
(2)NE是微电子工业中一种优良的等离子蚀刻气体,NF3分子空间构型为_______ ,NH3的键角约为107°,推测NF3的键角______ 107°(填“>”,“<”或“=”)。
(3)X射线衍射测定等发现,I3AsF6中存在I 离子。I
离子。I 中心原子的杂化方式为
中心原子的杂化方式为_________ 。
(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示。若该立方晶胞参数为apm,NA为阿伏加德罗常数:计算品体的密度为_______ g•cm-3(列出表达式)。[注:1皮米(pm)=1.0×10-12米(m)]

(1)图A、B、C分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同),第一电离能I1的变化图是

(2)NE是微电子工业中一种优良的等离子蚀刻气体,NF3分子空间构型为
(3)X射线衍射测定等发现,I3AsF6中存在I
 离子。I
离子。I 中心原子的杂化方式为
中心原子的杂化方式为(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示。若该立方晶胞参数为apm,NA为阿伏加德罗常数:计算品体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】硒化物(如KCu4Se8)可用于太阳能电池、光感传感器、热电发电与制冷等。回答下列问题:
(1)基态Se原子核外电子排布式为___________ 。
(2)K与Cu同周期,但金属K的熔点低,这明显是因为___________ 。
(3)O、S、Se的简单氢化物分子的键角由大到小的顺序为___________ 。(用分子式表示)
(4)离子型配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为___________ ,配体中碳原子的杂化方式是___________ 。
(5)TMTSF(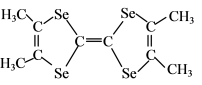 )中σ键与π键数目的比值是
)中σ键与π键数目的比值是___________ 。
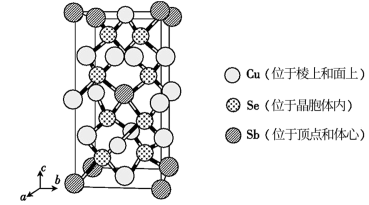
(6)由Cu,Sb,Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度是___________ g∙cm-3(列式即可)
(1)基态Se原子核外电子排布式为
(2)K与Cu同周期,但金属K的熔点低,这明显是因为
(3)O、S、Se的简单氢化物分子的键角由大到小的顺序为
(4)离子型配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为
(5)TMTSF(
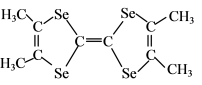 )中σ键与π键数目的比值是
)中σ键与π键数目的比值是(6)由Cu,Sb,Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题
(1)Na原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(2)相同压强下,部分元素氟化物的熔点见下表:
试解释上表中氟化物熔点差异的原因:_______ 。
(3)SiF4分子的空间构型为_______ 。
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因__________ 。
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数__________ 。
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
(1)Na原子核外共有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
(3)SiF4分子的空间构型为
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】如图是元素周期表的一部分:
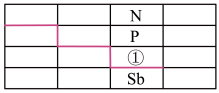
(1)与①同周期的主族元素中,第一电离能比①大的有_______ 种。
(2)基态锑(Sb)原子的价电子排布式为_______ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,则[H2F]+的空间结构为_______ 。
(3)下列说法正确的是_______ (填字母)。
a.N2H4分子中含5个σ键和1个π键
b.基态P原子中,电子占据的最高能级符号为M
c.Sb 位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(4)GaN、GaP都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,解释GaN、GaP熔点变化原因_______ 。
(5)GaN晶胞结构如图1所示,已知六棱柱底边边长为a cm。
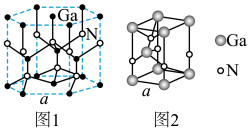
①晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_______ ;
②从GaN晶体中分割出的平行六面体如图2,若该平行六面体的体积为 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为_______ g·cm−3 (用a、NA表示)。

(1)与①同周期的主族元素中,第一电离能比①大的有
(2)基态锑(Sb)原子的价电子排布式为
(3)下列说法正确的是
a.N2H4分子中含5个σ键和1个π键
b.基态P原子中,电子占据的最高能级符号为M
c.Sb 位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(4)GaN、GaP都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,解释GaN、GaP熔点变化原因
| 物质 | GaN | GaP |
| 熔点/℃ | 1 700 | 1 480 |
(5)GaN晶胞结构如图1所示,已知六棱柱底边边长为a cm。

①晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为
②从GaN晶体中分割出的平行六面体如图2,若该平行六面体的体积为
 a3cm3,GaN晶体的密度为
a3cm3,GaN晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)基态F原子的核外电子排布式是___________ 。
(2)B、C、D元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是___________ ;B、C元素的这些氢化物的熔、沸点相差较大的主要原因是___________ 。
(4)A、B、D可形成分子式为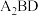 的某化合物,则该化合物分子中B原子的杂化轨道类型是
的某化合物,则该化合物分子中B原子的杂化轨道类型是___________ ;1mol该分子中含有π键的数目是___________ 。
(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为___________ (用化学式表示)。
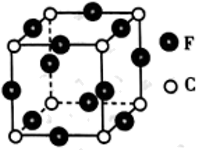
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是___________ ,C原子的配位数是___________ 。
(1)基态F原子的核外电子排布式是
(2)B、C、D元素的第一电离能由大到小的顺序是
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是
(4)A、B、D可形成分子式为
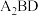 的某化合物,则该化合物分子中B原子的杂化轨道类型是
的某化合物,则该化合物分子中B原子的杂化轨道类型是(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】氮及其化合物,在工农业生产中作用巨大。
(1)下列有关氮的化合物的说法,正确的是___________。
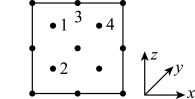
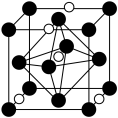
(2)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为___________ ,它的硬度超过金刚石的主要原因是___________ 。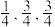 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为___________ 、___________ 。___________ ,氮化钼晶胞边长为a pm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关氮的化合物的说法,正确的是___________。
| A.肼(N2H4)的沸点低于乙烷(C2H6) |
| B.NH3极易溶于水,原因之一是NH3能够与水分子形成分子间氢键 |
| C.NF3和NH3空间构型均为三角锥形,分子中键角:NH3>NF3 |
D.尿素(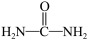 )中σ键与π键的比例为7:1 )中σ键与π键的比例为7:1 |
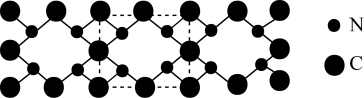
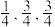 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为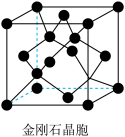
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】氧缺位体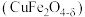 是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是
是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备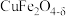 的流程如下:
的流程如下:

已知:①
②已知几种金属离子沉淀的 如表所示:
如表所示:
请回答下列问题:
(1)“焙烧”中生成了 、
、 ,写出“焙烧”中主要化学方程式:
,写出“焙烧”中主要化学方程式:_______ ,“焙烧”产生的 在有氧环境下利用石灰石浆液吸收可转变为
在有氧环境下利用石灰石浆液吸收可转变为_______ (填化学式)。
(2)“调 ”范围为
”范围为_______ ,从滤渣2中提取 的操作包括加入过量
的操作包括加入过量 溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是
溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是_______ (填化学式)
(3)“氧化”中 的作用是
的作用是_______ (用离子方程式表示)。
(4)“煅烧”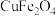 的化学方程式为
的化学方程式为_______ ,氧缺位值( )越大,活性越
)越大,活性越_______ (填“高”或“低”),与水反应制备 越容易。
越容易。
(5)钾、铁、硒形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示。已知:a、b、c的单位为 ,
, 为阿伏加德罗常数的数值,该晶体密度为
为阿伏加德罗常数的数值,该晶体密度为_______  (只列计算式)。
(只列计算式)。

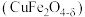 是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是
是热化学循环分解水制氢的氧化物体系。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备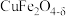 的流程如下:
的流程如下:
已知:①

②已知几种金属离子沉淀的
 如表所示:
如表所示:| 金属氢氧化物 |  |  |  |  |
开始沉淀的 | 2.7 | 7.6 | 4.0 | 6.4 |
完全沉淀的 | 3.7 | 9.6 | 5.2 | 7.6 |
(1)“焙烧”中生成了
 、
、 ,写出“焙烧”中主要化学方程式:
,写出“焙烧”中主要化学方程式: 在有氧环境下利用石灰石浆液吸收可转变为
在有氧环境下利用石灰石浆液吸收可转变为(2)“调
 ”范围为
”范围为 的操作包括加入过量
的操作包括加入过量 溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是
溶液、过滤、向滤液通入过量的气体R,过滤、灼烧,气体R是(3)“氧化”中
 的作用是
的作用是(4)“煅烧”
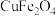 的化学方程式为
的化学方程式为 )越大,活性越
)越大,活性越 越容易。
越容易。(5)钾、铁、硒形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示。已知:a、b、c的单位为
 ,
, 为阿伏加德罗常数的数值,该晶体密度为
为阿伏加德罗常数的数值,该晶体密度为 (只列计算式)。
(只列计算式)。
您最近一年使用:0次



