I.联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
(1)在25℃时,1.00gN2H4(l)与足量N2O4(1)完全反应生成N2(g)和H2O(1),放出19.14kJ的热量。写出该反应的热化学方程式_______ 。
II.NO2是氮的常见氧化物,能自发发生如下反应:2NO2(g)⇌N2O4(g) =-57.20kJ/mol
=-57.20kJ/mol
(2)写出该反应的平衡常数表达式K=_______ 。已知:在一定温度下的密闭容器中,该反应已达到平衡。保持其他条件不变,下列措施能提高NO2转化率的是_______ 。
a.减小NO2的浓度 b.降低温度 c.增大压强 d.升高温度
III.Na2CO3俗称纯碱,是生活中的常用物质。某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案进行操作并记录实验现象。
(3)①该实验表明,Na2CO3溶液显碱性的原因是_______ (请结合化学用语,简要说明)。
②从形成盐的酸和碱的强弱角度看,Na2CO3属于_______ 盐。
③为了使Na2CO3溶液中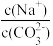 的比值变小,可适量加入(或通入)的物质是
的比值变小,可适量加入(或通入)的物质是_______ 。
a.CO2气体 b.KOH固体 c.HCl气体 d.Na2CO3固体
(1)在25℃时,1.00gN2H4(l)与足量N2O4(1)完全反应生成N2(g)和H2O(1),放出19.14kJ的热量。写出该反应的热化学方程式
II.NO2是氮的常见氧化物,能自发发生如下反应:2NO2(g)⇌N2O4(g)
 =-57.20kJ/mol
=-57.20kJ/mol(2)写出该反应的平衡常数表达式K=
a.减小NO2的浓度 b.降低温度 c.增大压强 d.升高温度
III.Na2CO3俗称纯碱,是生活中的常用物质。某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案进行操作并记录实验现象。
| 实验操作 | 实验现象 |
| 取少量Na2CO3固体,加入无水酒精,充分振荡、静置 | 溶液为无色 |
| 取上层清液于试管中,滴加酚酞试剂 | 溶液为无色 |
| 在试管中继续加入少量水 | 溶液变为红色 |
| 向该红色溶液中滴加足量BaCl2溶液(中性) | 红色褪去 |
②从形成盐的酸和碱的强弱角度看,Na2CO3属于
③为了使Na2CO3溶液中
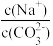 的比值变小,可适量加入(或通入)的物质是
的比值变小,可适量加入(或通入)的物质是a.CO2气体 b.KOH固体 c.HCl气体 d.Na2CO3固体
更新时间:2022-04-28 14:29:30
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
(1)图1表示反应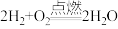 的能量变化。
的能量变化。
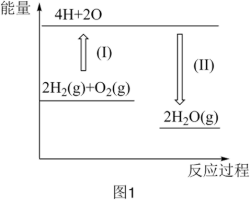
已知断开1molH—H键、1mol 键和1molH—O键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)中生成2mol
键和1molH—O键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)中生成2mol (g)时
(g)时_______ (填“吸收”或“放出”)_______ kJ能量。
(2)由 和NO反应生成
和NO反应生成 和
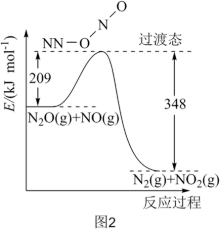
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为_______  ,若反应生成
,若反应生成 ,其
,其
_______  。
。
(3)在25℃、101kPa下,一定质量的CH3CH2OH(l)完全燃烧生成液态水时放出热量 kJ,其燃烧生成的
kJ,其燃烧生成的 用过量饱和石灰水吸收可得100g
用过量饱和石灰水吸收可得100g 沉淀,则CH3CH2OH燃烧的热化学方程式为
沉淀,则CH3CH2OH燃烧的热化学方程式为_______ 。
(1)图1表示反应
 的能量变化。
的能量变化。
已知断开1molH—H键、1mol
 键和1molH—O键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)中生成2mol
键和1molH—O键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)中生成2mol (g)时
(g)时(2)由
 和NO反应生成
和NO反应生成 和
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为 ,若反应生成
,若反应生成 ,其
,其
 。
。
(3)在25℃、101kPa下,一定质量的CH3CH2OH(l)完全燃烧生成液态水时放出热量
 kJ,其燃烧生成的
kJ,其燃烧生成的 用过量饱和石灰水吸收可得100g
用过量饱和石灰水吸收可得100g 沉淀,则CH3CH2OH燃烧的热化学方程式为
沉淀,则CH3CH2OH燃烧的热化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】为解决能源短缺问题,工业生产中应合理利用化学能。
(1)25 ℃,1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为______________________ 。
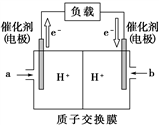
(2)上图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从________ 处通入(填“a”或“b”),电池内部H+向_______ (填“左”或“右”)移动。写出电池负极的电极反应式________ 。正极的电极反应式_______________________ 。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
已知:N2(g)+3H2(g)===2NH3(g) ΔH=-93 kJ·mol-1。
试根据表中所列键能数据计算a的数值________ 。
当可逆反应中净生成N—H物质的量为2mol 时,反应放热_____________ 。
(4)已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g)的ΔH=________ 。
(1)25 ℃,1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为

(2)上图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)===2NH3(g) ΔH=-93 kJ·mol-1。
试根据表中所列键能数据计算a的数值
当可逆反应中净生成N—H物质的量为2mol 时,反应放热
(4)已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g)的ΔH=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】运用化学反应原理研究氮、氧等元素的单质及其化合物的反应有重要意义。
Ⅰ.(1)一定温度和压强下,反应N2(g) + 3H2(g) 2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡
2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡______ (填“向左”、“向右”或“不”)移动;若使用活性更强的催化剂,该反应的ΔH______ (填“增大”、“减小”或“不改变”)。
(2)在一定温度和压强下,已知:
O2 (g) = O2+ (g) + e-; H1= 1175.7 kJ/mol
H1= 1175.7 kJ/mol
PtF6 (g) + e- = PtF6- (g); H2=-771.1" kJ/mol
H2=-771.1" kJ/mol
O2PtF6 (s) = O2+ (g) + PtF (g);
(g); H3=482.2kJ/mol
H3=482.2kJ/mol
则反应O2 (g) + PtF6 (g) = O2PtF6(s); H=
H=______ kJ/mol。
Ⅱ.现有常温下的六种溶液:①0.01 mol/L CH3COOH溶液;②0.01 mol/L HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01 mol/L CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01 mol/L HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)⑤、⑥溶液比较,pH较大的是______ 。
(2)六种溶液中,水的电离程度相同的是______ 。
(3)若②、③混合后所得溶液pH=7,则消耗溶液的体积:②______ ③(选填“>”、“<”或“=”)。
(4)稀释相同倍数后,溶液的pH:①______ ②,③______ ④(选填“>”、“<”或“=”)。
Ⅰ.(1)一定温度和压强下,反应N2(g) + 3H2(g)
 2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡
2NH3(g)达到化学平衡状态。若向平衡体系中通入氩气,平衡(2)在一定温度和压强下,已知:
O2 (g) = O2+ (g) + e-;
 H1= 1175.7 kJ/mol
H1= 1175.7 kJ/molPtF6 (g) + e- = PtF6- (g);
 H2=-771.1" kJ/mol
H2=-771.1" kJ/molO2PtF6 (s) = O2+ (g) + PtF
 (g);
(g); H3=482.2kJ/mol
H3=482.2kJ/mol则反应O2 (g) + PtF6 (g) = O2PtF6(s);
 H=
H=Ⅱ.现有常温下的六种溶液:①0.01 mol/L CH3COOH溶液;②0.01 mol/L HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01 mol/L CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01 mol/L HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)⑤、⑥溶液比较,pH较大的是
(2)六种溶液中,水的电离程度相同的是
(3)若②、③混合后所得溶液pH=7,则消耗溶液的体积:②
(4)稀释相同倍数后,溶液的pH:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】乙酰苯胺为无色晶体,具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称。实验室常用苯胺与乙酸反应制备乙酰苯胺:
 +CH3COOH
+CH3COOH
 +H2O
+H2O
相关的文献数据如下:
实验流程如下:
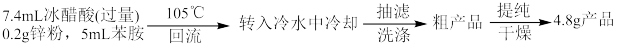
据此回答下列问题:
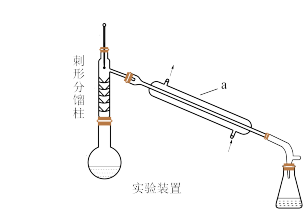
(1)实验装置中仪器a的名称_________ ,圆底烧瓶中加入少许锌粉目的是_______ ,锥形瓶中蒸馏物主要成分是_______ (填化学式)。
(2)反应需控制温度在105℃左右的原因是_______ ,判断反应已基本完全的依据是_______ 。
(3)粗产品中所含有机杂质主要为_______ ,进一步提纯的实验方法为_______ ,证明提纯后的产品为乙酰苯胺的简单实验方法为_______ 。
(4)计算所得到乙酰苯胺的产率是_______ 。
 +CH3COOH
+CH3COOH
 +H2O
+H2O
相关的文献数据如下:
| 物质 | 密度g/ml | 熔点℃ | 沸点℃ | 溶解性 |
| 冰醋酸 | 1.05 | 16.6 | 118 | 易溶于水 |
| 苯胺 | 1.02 | -6 | 184.4 | 微溶于水,易氧化 |
| 乙酰苯胺 | 1.21 | 114.3 | 305 | 微溶于冷水,易溶于热水 |
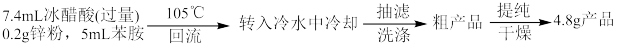
据此回答下列问题:
(1)实验装置中仪器a的名称
(2)反应需控制温度在105℃左右的原因是
(3)粗产品中所含有机杂质主要为
(4)计算所得到乙酰苯胺的产率是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】黄铁矿[主要成分为二硫化亚铁(FeS2)]、焦炭和适量空气混合加热发生如下反应:
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为_____ mol。
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2。将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g) S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0
iii.SO2(g)+3CO(g) COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0
理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。_____ 。
②随温度升高,S2平衡产率上升,推测其原因是_____ 。
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为_____ 。
(3)处理后的尾气仍含少量SO2,经Na2CO3溶液洗脱处理后,所得洗脱液主要成分为Na2CO3、NaHCO3和Na2SO3.利用生物电池技术,可将洗脱液中的Na2SO3转化为单质硫(以S表示)回收。_____ 。
②一段时间后,若洗脱液中 的物质的量减小了1mol,则理论上
的物质的量减小了1mol,则理论上 减小了
减小了_____ mol。
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2。将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g)
 S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0iii.SO2(g)+3CO(g)
 COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。
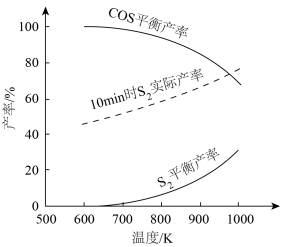
②随温度升高,S2平衡产率上升,推测其原因是
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为
(3)处理后的尾气仍含少量SO2,经Na2CO3溶液洗脱处理后,所得洗脱液主要成分为Na2CO3、NaHCO3和Na2SO3.利用生物电池技术,可将洗脱液中的Na2SO3转化为单质硫(以S表示)回收。
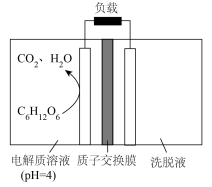
②一段时间后,若洗脱液中
 的物质的量减小了1mol,则理论上
的物质的量减小了1mol,则理论上 减小了
减小了
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】二氧化碳催化加氢制甲醇,不仅有利于减少温室气体二氧化碳,而且还可以获得大量的重要有机化工原料甲醇。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) 平衡常数K
CH3OH(g)+H2O(g) 平衡常数K
该反应一般认为通过如下步骤来实现:
i.CO2(g)+3H2(g) CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
ii.CO(g)+ 2H2(g) CH3OH(g) △H =-90 kJ/mol 平衡常数K2
CH3OH(g) △H =-90 kJ/mol 平衡常数K2
①则总反应的△H=____ kJ/mol;平衡常数K=_______ (用K1、K2表示)。
②上述总反应在容积不变的密闭容器进行,在t0时达到平衡,当其他条件不变时,改变某一条件,下列图像的描述,说法正确的是__________ 。
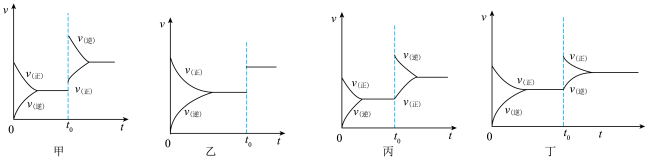
A.图甲表示t0时升高温度对反应速率的影响
B.图乙表示t0时加压或催化剂对反应速率的影响
C.图丙表示t0时分离出甲醇对反应速率的影响, 同时可以提高甲醇的产率
D.图丁表示t0时增加CO2的物质的量对反应速率的影响,同时可以提高CO2的转化率
(2)若T1时时将6 molCO2和8molH2充入容积为2 L的密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),H2的物质的量变化如下表所示。
CH3OH(g)+H2O(g),H2的物质的量变化如下表所示。
①在T℃条件下0- 5min内, 以CO2表示的该反应速率v(CO2)=_____ ,该条件 下的平面常数K=_______ 。
②第15 min后,温度调整到T1℃, 数据变化如上表所示,则T1______ T2(填“>”、“<” 或“=”)。
③若15 min时,保持T1不变,向该容器中再加入该四种反应混合物各1 mol,则此时反应_____ 移动(填*正向”、“逆向" 或“不");
④T1℃达到平衡后,保持其他条件不变,在t1时刻迅速将容器体积压缩至1 L,t2时重新达到平衡,请在图中画出t1时刻后c(H+)的变化趋势_____ 。
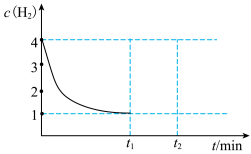 。
。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) 平衡常数K
CH3OH(g)+H2O(g) 平衡常数K该反应一般认为通过如下步骤来实现:
i.CO2(g)+3H2(g)
 CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1
CO(g) +H2O(g) △H= +41 kJ/mol 平衡常数K1ii.CO(g)+ 2H2(g)
 CH3OH(g) △H =-90 kJ/mol 平衡常数K2
CH3OH(g) △H =-90 kJ/mol 平衡常数K2①则总反应的△H=
②上述总反应在容积不变的密闭容器进行,在t0时达到平衡,当其他条件不变时,改变某一条件,下列图像的描述,说法正确的是

A.图甲表示t0时升高温度对反应速率的影响
B.图乙表示t0时加压或催化剂对反应速率的影响
C.图丙表示t0时分离出甲醇对反应速率的影响, 同时可以提高甲醇的产率
D.图丁表示t0时增加CO2的物质的量对反应速率的影响,同时可以提高CO2的转化率
(2)若T1时时将6 molCO2和8molH2充入容积为2 L的密闭容器中发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),H2的物质的量变化如下表所示。
CH3OH(g)+H2O(g),H2的物质的量变化如下表所示。| 物质的量/mol | T1/℃ | T2/℃ | |||||
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
| H2 | 8.0 | 3.5 | 2.0 | 2.0 | 1.5 | 1.0 | 1.0 |
②第15 min后,温度调整到T1℃, 数据变化如上表所示,则T1
③若15 min时,保持T1不变,向该容器中再加入该四种反应混合物各1 mol,则此时反应
④T1℃达到平衡后,保持其他条件不变,在t1时刻迅速将容器体积压缩至1 L,t2时重新达到平衡,请在图中画出t1时刻后c(H+)的变化趋势
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】CO2和CH4是两种主要的温室气体,以CO2和CH4为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。回答下列问题:
(1)工业上CO2-CH4催化重整是目前大规模制取合成气(CO和H2混合气)的重要方法,其原理为:
反应I:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1
CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1
反应II:CO(g)+H2O(g) CO2(g)+H2(g) ∆H2=-41 kJ·mol-1
CO2(g)+H2(g) ∆H2=-41 kJ·mol-1
几种化学键的键能如表所示:
①a=_______ kJ·mol-1。
②反应II中,若逆反应活化能Ea(逆)为124 kJ·mol-1,则Ea(正)为_______ kJ·mol-1。
(2)将等物质的量的CH4(g)和H2O(g)充入恒温恒容的密闭容器中,发生反应I和反应II,容器内气体的压强随时间的变化如表所示。
①若用单位时间内气体分压(气体分压=气体总压×体积分数)的变化来表示反应速率,则反应I前120min内的平均反应速率v(CH4)=_______ kPa·min-1(结果保留2位小数)。
②300 min时,测得氢气分压为100 kPa,则反应II在该温度下的平衡常数Kp=_______ (Kp为用气体分压表示的平衡常数,结果保留2位小数)。
(3)向2 L容器中充入1 mol CH4和1 mol H2O,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH4体积分数如图I所示,某温度下逆反应速率与容器中c(CH4)关系如图II所示:
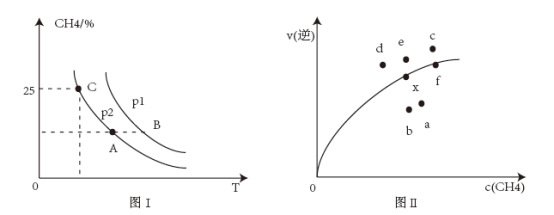
①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序为_______ ,p1_______ p2(填“>”“<”或“=”)。
②图II中当x点平衡体系升高至某温度时,反应可重新达平衡状态,新平衡点可能是_______ (填标号)。
(1)工业上CO2-CH4催化重整是目前大规模制取合成气(CO和H2混合气)的重要方法,其原理为:
反应I:CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1
CO(g)+3H2(g) ∆H1=+206.4 kJ·mol-1反应II:CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H2=-41 kJ·mol-1
CO2(g)+H2(g) ∆H2=-41 kJ·mol-1几种化学键的键能如表所示:
| 化学键 | C-H | H-O | H-H | C O O |
键能/kJ mol-1 mol-1 | 413 | 467 | 436 | a |
①a=
②反应II中,若逆反应活化能Ea(逆)为124 kJ·mol-1,则Ea(正)为
(2)将等物质的量的CH4(g)和H2O(g)充入恒温恒容的密闭容器中,发生反应I和反应II,容器内气体的压强随时间的变化如表所示。
| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 100 | 118 | 132 | 144 | 154 | 162 | 162 |
①若用单位时间内气体分压(气体分压=气体总压×体积分数)的变化来表示反应速率,则反应I前120min内的平均反应速率v(CH4)=
②300 min时,测得氢气分压为100 kPa,则反应II在该温度下的平衡常数Kp=
(3)向2 L容器中充入1 mol CH4和1 mol H2O,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH4体积分数如图I所示,某温度下逆反应速率与容器中c(CH4)关系如图II所示:

①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序为
②图II中当x点平衡体系升高至某温度时,反应可重新达平衡状态,新平衡点可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)  2NOCl(g)。
2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) K1
NaNO3(s)+NOCl(g) K1
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g) 2NOCl(g) K3
2NOCl(g) K3
反应①②③对应的平衡常数依次为K1、K2、K3,则K3与K1、K2之间的关系为_________ 。
(2)300℃时,2NOCl(g) 2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为
2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为带有单位 的速率常数,其值只与温度有关),测得速率与浓度的关系如表所示:
n=_________ ,k=_________ 。
(3)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入一定量NO和 Cl2合成NOCl,方程式为2NO(g)+Cl2(g) 2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H
2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H _________ (填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图1曲线b所示,则改变的条件是_________ 。
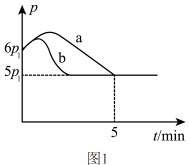
(4)若把2molNO和1molCl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图2所示,若反应一直保持在p压强条件下进行,则M点的分压平衡常数Kp=_________ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。

 2NOCl(g)。
2NOCl(g)。(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g) K1
NaNO3(s)+NOCl(g) K1②4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2③2NO(g)+Cl2(g)
 2NOCl(g) K3
2NOCl(g) K3反应①②③对应的平衡常数依次为K1、K2、K3,则K3与K1、K2之间的关系为
(2)300℃时,2NOCl(g)
 2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为
2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为| 序号 | c(NOCl)/mol·L-1 | v正/mol·L-1·s-1 |
| ① | 0.30 | 3.60×10-9 |
| ② | 0.60 | l.44×10-8 |
| ③ | 0.90 | 3.24×10-8 |
(3)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入一定量NO和 Cl2合成NOCl,方程式为2NO(g)+Cl2(g)
 2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H
2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H 
(4)若把2molNO和1molCl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图2所示,若反应一直保持在p压强条件下进行,则M点的分压平衡常数Kp=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上制取CuCl2的生产流程如下:
请结合下表数据,回答下列问题:
(1)溶液A中加入NaClO的目的是____________________________ ;
此反应离子方程式为_____________________________________ ;
(2)在溶液B中加入CuO的作用是______________________________ ;
(3)操作a的目的是_________________________________________ ;
(4)在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是__________ 。

请结合下表数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
此反应离子方程式为
(2)在溶液B中加入CuO的作用是
(3)操作a的目的是
(4)在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】2015年8月12日天津港发生了危化品特大爆炸事故,爆炸仓库存有大量氰化钠(NaCN)、硝酸铵、四氯化钛等物品。
(1)NaCN溶液中各离子浓度大小关系为______ 。已知NaCN遇酸能产生HCN; 时,HCN的电离常数
时,HCN的电离常数
 ;
; 的电离常数
的电离常数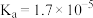
 。体积均为100mL、
。体积均为100mL、 的
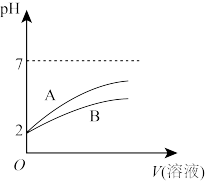
的 溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示
溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示 溶的pH变化趋势的曲线是
溶的pH变化趋势的曲线是 ______  选填“A”或“B”
选填“A”或“B” ;相同条件下,NaCN溶液的pH
;相同条件下,NaCN溶液的pH ______  选填“
选填“ ”、“
”、“ ”或“
”或“ ”
” 溶液的pH。
溶液的pH。
(2)200℃固体硝酸铵可以分解为 和
和 ,此过程中每转移电子8mol放出热量
,此过程中每转移电子8mol放出热量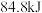 ,写出此反应的热化学方程式
,写出此反应的热化学方程式 ______ 。
(3)工业上用氯气和二氧化钛制备 ,一定条件下发生反应:
,一定条件下发生反应: ;
; 。此温度下,该反应的平衡常数为400,在密闭容器中加入
。此温度下,该反应的平衡常数为400,在密闭容器中加入 和
和 ,反应到t时刻测得各组分的浓度如表所示:
,反应到t时刻测得各组分的浓度如表所示:
①根据表中数据判断t时刻此反应向 ______ 反应方向进行 选填“正”或“逆”
选填“正”或“逆” 。
。
②若经10min反应达到平衡,则该时间内反应速率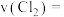
______ 。 ;下列措施中,可以使平衡向右移动的是
;下列措施中,可以使平衡向右移动的是 ______  选填序号
选填序号 。
。
a.使用催化剂 b.增大压强 c.减小压强 d.升高温度

(1)NaCN溶液中各离子浓度大小关系为
 时,HCN的电离常数
时,HCN的电离常数
 ;
; 的电离常数
的电离常数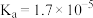
 。体积均为100mL、
。体积均为100mL、 的
的 溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示
溶液和HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示 溶的pH变化趋势的曲线是
溶的pH变化趋势的曲线是  选填“A”或“B”
选填“A”或“B” ;相同条件下,NaCN溶液的pH
;相同条件下,NaCN溶液的pH  选填“
选填“ ”、“
”、“ ”或“
”或“ ”
” 溶液的pH。
溶液的pH。(2)200℃固体硝酸铵可以分解为
 和
和 ,此过程中每转移电子8mol放出热量
,此过程中每转移电子8mol放出热量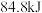 ,写出此反应的热化学方程式
,写出此反应的热化学方程式 (3)工业上用氯气和二氧化钛制备
 ,一定条件下发生反应:
,一定条件下发生反应: ;
; 。此温度下,该反应的平衡常数为400,在密闭容器中加入
。此温度下,该反应的平衡常数为400,在密闭容器中加入 和
和 ,反应到t时刻测得各组分的浓度如表所示:
,反应到t时刻测得各组分的浓度如表所示:| 物质 |  |  |  |
浓度 |  | 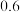 | 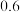 |
 选填“正”或“逆”
选填“正”或“逆” 。
。②若经10min反应达到平衡,则该时间内反应速率
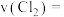
 ;下列措施中,可以使平衡向右移动的是
;下列措施中,可以使平衡向右移动的是  选填序号
选填序号 。
。a.使用催化剂 b.增大压强 c.减小压强 d.升高温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氯化亚铜(CuCl)是一种重要的化工产品。它难溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在水溶液中存在平衡:CuCl(白色)+2Cl﹣⇌[CuCl3]2﹣(无色溶液)。在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4﹣nCln],n随着环境酸度的改变而改变。某研究小组设计如下两种方案制备氯化亚铜。
方案一:铜粉还原CuSO4溶液
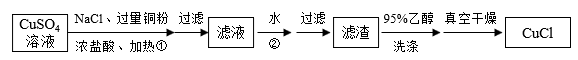
请回答:
(1)步骤①中发生反应的离子方程式为_______ 。
(2)步骤②中,加入大量水的作用是_______ 。
(3)如图流程中用95%乙醇洗涤和真空干燥是为了防止_______ 。
(4)随着pH减小,Cu2(OH)4﹣nCln中铜的质量分数_______ 。
A增大B不变C减小D不能确定
方案二:在氯化氢气流中加热CuCl2•2H2O晶体制备,其流程和实验装置(夹持仪器略)如图:
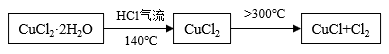
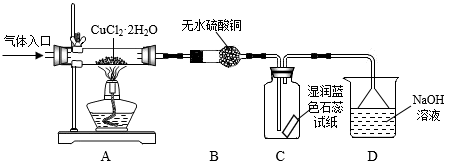
请回答:
(5)实验操作的先后顺序是a→_______ →_______ →_______ →e(填操作的编号)
a检查装置的气密性后加入药品b点燃酒精灯,加热
c在“气体入口”处通入干燥HCl d熄灭酒精灯,冷却
e停止通入HCl,然后通入N2
(6)在实验过程中,观察到B中无水硫酸铜由白色变为蓝色,C中试纸的颜色变化是_______ 。
(7)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2杂质,请分析产生CuCl2杂质的原因_______ 。
方案一:铜粉还原CuSO4溶液

请回答:
(1)步骤①中发生反应的离子方程式为
(2)步骤②中,加入大量水的作用是
(3)如图流程中用95%乙醇洗涤和真空干燥是为了防止
(4)随着pH减小,Cu2(OH)4﹣nCln中铜的质量分数
A增大B不变C减小D不能确定
方案二:在氯化氢气流中加热CuCl2•2H2O晶体制备,其流程和实验装置(夹持仪器略)如图:


请回答:
(5)实验操作的先后顺序是a→
a检查装置的气密性后加入药品b点燃酒精灯,加热
c在“气体入口”处通入干燥HCl d熄灭酒精灯,冷却
e停止通入HCl,然后通入N2
(6)在实验过程中,观察到B中无水硫酸铜由白色变为蓝色,C中试纸的颜色变化是
(7)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2杂质,请分析产生CuCl2杂质的原因
您最近一年使用:0次

 制备
制备 的原理
的原理 溶液与50 mL 0.55 mol/L NaOH溶液充分反应,测得放出1.4 kJ的热量,写出该过程表示中和热的热化学方程式:
溶液与50 mL 0.55 mol/L NaOH溶液充分反应,测得放出1.4 kJ的热量,写出该过程表示中和热的热化学方程式:
 ,则除去CO气体的适宜条件是
,则除去CO气体的适宜条件是

