过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)基态Cr原子核外电子排布式为_______ 。
(2)Cr和K属于同一周期,但金属Cr的熔点、沸点等都比金属K高,原因是_______ 。
(3)三价铬离子能形成多种配位化合物。 中提供孤电子对形成配位键的原子是
中提供孤电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(4) 是
是 中一种配体分子。N与P同主族,
中一种配体分子。N与P同主族, 分子的空间构型为
分子的空间构型为_______ 。 的沸点比
的沸点比 的
的_______ (填“高”或“低”),原因是_______ 。
(5)在金属材料中添加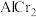 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。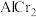 具有体心四方结构,如图所示。
具有体心四方结构,如图所示。

已知: ,
, ,NA为阿伏加德罗常数的值,则
,NA为阿伏加德罗常数的值,则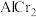 晶体的密度是
晶体的密度是_______  。(列出计算式)
。(列出计算式)
(1)基态Cr原子核外电子排布式为
(2)Cr和K属于同一周期,但金属Cr的熔点、沸点等都比金属K高,原因是
(3)三价铬离子能形成多种配位化合物。
 中提供孤电子对形成配位键的原子是
中提供孤电子对形成配位键的原子是(4)
 是
是 中一种配体分子。N与P同主族,
中一种配体分子。N与P同主族, 分子的空间构型为
分子的空间构型为 的沸点比
的沸点比 的
的(5)在金属材料中添加
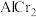 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。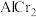 具有体心四方结构,如图所示。
具有体心四方结构,如图所示。
已知:
 ,
, ,NA为阿伏加德罗常数的值,则
,NA为阿伏加德罗常数的值,则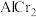 晶体的密度是
晶体的密度是 。(列出计算式)
。(列出计算式)
更新时间:2022-05-03 14:24:26
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】铁元素被称为“人类第一元素”,铁及其化合物具有广泛的用途。
(1)水体中过量的 是一种重要污染物,可利用纳米铁粉将其除去。
是一种重要污染物,可利用纳米铁粉将其除去。
①基态铁原子核外电子排布式:___________ ;铁元素在元素周期表中的位置为___________ ,属于___________ 区元素。
②相同条件下,向含有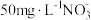 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图1所示,产生该差异的可能原因为
的去除速率差异如图1所示,产生该差异的可能原因为___________ 。


(2)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图2所示。储氢时, 分子位于晶胞体心和棱的中心位置。
分子位于晶胞体心和棱的中心位置。
①该晶胞中 的配位数是
的配位数是___________ 。
②该合金储满氢后所得晶体的化学式是___________ 。
(3)在生产中,常用 处理
处理 的含
的含 (
( 价)废水得到
价)废水得到 和
和 。
。 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释其原因:
,请利用核外电子排布的相关原理解释其原因:___________ 。
(1)水体中过量的
 是一种重要污染物,可利用纳米铁粉将其除去。
是一种重要污染物,可利用纳米铁粉将其除去。①基态铁原子核外电子排布式:
②相同条件下,向含有
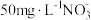 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图1所示,产生该差异的可能原因为
的去除速率差异如图1所示,产生该差异的可能原因为

(2)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图2所示。储氢时,
 分子位于晶胞体心和棱的中心位置。
分子位于晶胞体心和棱的中心位置。①该晶胞中
 的配位数是
的配位数是②该合金储满氢后所得晶体的化学式是
(3)在生产中,常用
 处理
处理 的含
的含 (
( 价)废水得到
价)废水得到 和
和 。
。 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释其原因:
,请利用核外电子排布的相关原理解释其原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金。请完成以下有关物质结构的问题:
(1)写出Fe2+的最高能层的电子排布式:________________ 。
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为________________ ;
已知CrO5中Cr为+6价,则CrO5的结构式为________ 。
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为_______ ;已知该物质的中心原子价电子数与配体提供电子总数之和为18,则n=__________ ;与Ni(CO)n中配体互为等电子体的阴离子化学式为________________ 。
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是_________ 晶体,键角是_________ ;在SiC中,如果以一个硅原子为中心,则与硅原子次近的第二层有________ 个硅原子。
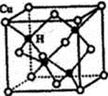
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为______ cm(用含d和Na的式子表示)。
(1)写出Fe2+的最高能层的电子排布式:
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为
已知CrO5中Cr为+6价,则CrO5的结构式为
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】齐家坪遗址是一处新石器时代晚期文化遗址,出土的铜镜是迄今为止我国发现最早的铜镜。铜及其化合物在工农业生产中有广泛的应用。
I.金属铜的晶胞结构模型如图1所示。 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为___________ 。
(2)设晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为___________ 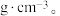
II. 能与
能与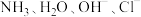 等形成配位数为4的配合物。
等形成配位数为4的配合物。
将 投入
投入 的混合溶液中进行“氨浸”,控制温度为
的混合溶液中进行“氨浸”,控制温度为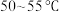 ,
, 约为9.5,
约为9.5, 转化为
转化为 溶液。
溶液。
(3) 中基态铜离子核外电子排布式为
中基态铜离子核外电子排布式为___________ 。
(4) 结构中,若用两个
结构中,若用两个 代替两个
代替两个 ,可以得到两种不同结构的化合物,由此推测
,可以得到两种不同结构的化合物,由此推测 的空间结构为
的空间结构为___________ 。
(5) 可以与乙二胺
可以与乙二胺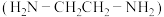 形成配离子,如图2所示:
形成配离子,如图2所示: 原子成键时采取的杂化方式是
原子成键时采取的杂化方式是___________ 杂化。
②乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是
均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是___________ 。
III.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(6)下列物质中,属于顺磁性物质的是___________ (填字母)。
A.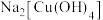 B.
B. C.
C.
I.金属铜的晶胞结构模型如图1所示。
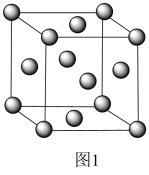
 原子周围距离最近的
原子周围距离最近的 原子数目为
原子数目为(2)设晶胞参数为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为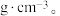
II.
 能与
能与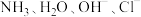 等形成配位数为4的配合物。
等形成配位数为4的配合物。将
 投入
投入 的混合溶液中进行“氨浸”,控制温度为
的混合溶液中进行“氨浸”,控制温度为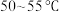 ,
, 约为9.5,
约为9.5, 转化为
转化为 溶液。
溶液。(3)
 中基态铜离子核外电子排布式为
中基态铜离子核外电子排布式为(4)
 结构中,若用两个
结构中,若用两个 代替两个
代替两个 ,可以得到两种不同结构的化合物,由此推测
,可以得到两种不同结构的化合物,由此推测 的空间结构为
的空间结构为(5)
 可以与乙二胺
可以与乙二胺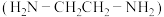 形成配离子,如图2所示:
形成配离子,如图2所示: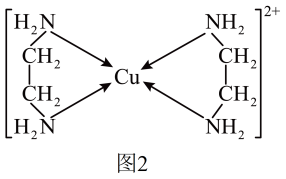
 原子成键时采取的杂化方式是
原子成键时采取的杂化方式是②乙二胺和三甲胺
 均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是
均属于胺,但乙二胺比三甲胺的溶解度大很多,原因是III.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
(6)下列物质中,属于顺磁性物质的是
A.
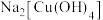 B.
B. C.
C.
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为___________ 。
(2)在BF3分子中B原子的杂化轨道类型为___________ 。
(3)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(4)已知(CN)2是直线形分子,且有对称性,其中π键与σ键的个数比为___________ 。
(5)基态S原子价电子排布式___________ ;S原子的核外电子运动状态有___________ 种。
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为
(2)在BF3分子中B原子的杂化轨道类型为
(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)已知(CN)2是直线形分子,且有对称性,其中π键与σ键的个数比为
(5)基态S原子价电子排布式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】过渡金属元素在日常生活中有广泛的应用。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为__________ ;基态 Mn原子核外有____ 种运动状态不同的电子,M层的电子云有_______ 种不同的伸展方向。
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是____________________________________
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒__________ (写出一种),K3[Co(NO2)6]中存在的作用力有___________ a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为____________
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。
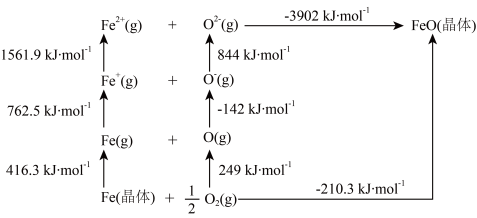
可知,O原子的第一电子亲和能为________ kJ•mol-1,FeO晶格能为________ kJ•mol-1。
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为_______________ ,已知该晶体的密度为ρg•cm-3,NA是阿伏加 德罗常数的值,则晶胞参数为_________ pm(列出计算式即可)

(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。

可知,O原子的第一电子亲和能为
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】光电材料[氟代硼铍酸钾晶体(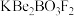 )等]是目前科学家特别关注的材料。其结构如图,其中氧原子已省略,图中的原子分别位于立方体的顶点、棱及面上,可由BeO、
)等]是目前科学家特别关注的材料。其结构如图,其中氧原子已省略,图中的原子分别位于立方体的顶点、棱及面上,可由BeO、 和
和 在一定条件下制得,同时放出
在一定条件下制得,同时放出 气体。
气体。
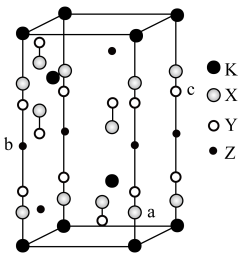
(1)基态B原子中有________ 种能量不同的电子,存在未成对电子的能级电子云空间有________ 种伸展方向。
(2)组成元素中非金属元素的电负性由强到弱的顺序为________ (填元素符号); 中B原子的杂化方式为
中B原子的杂化方式为________ ,已知苯分子中含有大π键,可记为 (右下角“6”表示6个原子,右上角“6”表示6个共用电子),实验测得
(右下角“6”表示6个原子,右上角“6”表示6个共用电子),实验测得 分子中B-F键的键长远小于二者原子半径之和,所以
分子中B-F键的键长远小于二者原子半径之和,所以 分子中存在大π键,可表示为
分子中存在大π键,可表示为________ 。
(3)已知卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有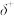 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,接受
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,接受 的
的 进攻。则
进攻。则 发生水解的产物是
发生水解的产物是________ 。
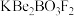 )等]是目前科学家特别关注的材料。其结构如图,其中氧原子已省略,图中的原子分别位于立方体的顶点、棱及面上,可由BeO、
)等]是目前科学家特别关注的材料。其结构如图,其中氧原子已省略,图中的原子分别位于立方体的顶点、棱及面上,可由BeO、 和
和 在一定条件下制得,同时放出
在一定条件下制得,同时放出 气体。
气体。
(1)基态B原子中有
(2)组成元素中非金属元素的电负性由强到弱的顺序为
 中B原子的杂化方式为
中B原子的杂化方式为 (右下角“6”表示6个原子,右上角“6”表示6个共用电子),实验测得
(右下角“6”表示6个原子,右上角“6”表示6个共用电子),实验测得 分子中B-F键的键长远小于二者原子半径之和,所以
分子中B-F键的键长远小于二者原子半径之和,所以 分子中存在大π键,可表示为
分子中存在大π键,可表示为(3)已知卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有
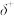 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,接受
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,接受 的
的 进攻。则
进攻。则 发生水解的产物是
发生水解的产物是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体。
(1)第二周期中基态原子与基态Co原子具有相同未成对电子数的元素是_______ 。
(2)Fe、Co、Ni原子半径相似、化学性质相似,原因是_______ 。
(3)配合物Fe(CO)5的中心原子价电子数与配体提供电子总数之和为_______ 。CO与N2互为等电子体,CO分子具有的化学键类型有_______ 。
A.σ键 B.π键 C.离子键 D.金属键
(4)Ni(CO)4的结构与相关性质如表,其空间构型为_______ ,Ni的杂化形式为_______ ,其为_______ 晶体。
(5)钙钛矿中含有Sm、Ni、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中Sm和O如图所示,Ni位于O形成正八面体空隙中.晶胞边长为apm,设NA为阿伏加德罗常数的数值,则该氧化物的密度为_______ g•cm-3(列出计算表达式)。

(1)第二周期中基态原子与基态Co原子具有相同未成对电子数的元素是
(2)Fe、Co、Ni原子半径相似、化学性质相似,原因是
(3)配合物Fe(CO)5的中心原子价电子数与配体提供电子总数之和为
A.σ键 B.π键 C.离子键 D.金属键
(4)Ni(CO)4的结构与相关性质如表,其空间构型为
| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 | -19.3℃ | 43℃ | 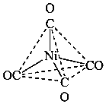 |
(5)钙钛矿中含有Sm、Ni、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中Sm和O如图所示,Ni位于O形成正八面体空隙中.晶胞边长为apm,设NA为阿伏加德罗常数的数值,则该氧化物的密度为

您最近一年使用:0次
【推荐2】铁及其化合物在生产生活及科研中应用广泛。
(1)聚合硫酸铁的化学式为 ,是常用的水处理剂。基态铁原子的核外电子排布式为
,是常用的水处理剂。基态铁原子的核外电子排布式为_____ ,聚合硫酸铁中铁元素阳离子有_____ 个未成对电子。
(2)Fe3+、Co3+与 、CN-等可形成络合离子。
、CN-等可形成络合离子。
① 可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为
可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为______ ,1mol 中含有σ键的数目为
中含有σ键的数目为________ 。
② 中Co的配位数为
中Co的配位数为______ ,C、N、O的第一电离能最大的为_____ ,其原因是_____ 。
③已知 与CS2为等电子体,则
与CS2为等电子体,则 的空间构型为
的空间构型为______ 。
(3)化合物FeF3熔点高于1000℃,而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的可能原因是_______ 。
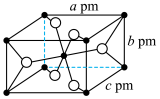
(4)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=_____ g·cm-3(列出计算式即可)。
(1)聚合硫酸铁的化学式为
 ,是常用的水处理剂。基态铁原子的核外电子排布式为
,是常用的水处理剂。基态铁原子的核外电子排布式为(2)Fe3+、Co3+与
 、CN-等可形成络合离子。
、CN-等可形成络合离子。①
 可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为
可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为 中含有σ键的数目为
中含有σ键的数目为②
 中Co的配位数为
中Co的配位数为③已知
 与CS2为等电子体,则
与CS2为等电子体,则 的空间构型为
的空间构型为(3)化合物FeF3熔点高于1000℃,而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的可能原因是
(4)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据图中所示数据计算该晶体密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】黄铜矿(主要成分为CuFeS2)是生产铜、铁和硫酸的原料。回答下列问题:
(1)基态Cu原子的价电子排布式为________ 。
(2)从原子结构角度分析,第一电离能I1(Fe)与I1(Cu)的关系是:I1(Fe)________ (填“>”“<”或“=”)I1(Cu)。
(3)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如下图:

①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为________ 。
②1 mol吡咯分子中所含的σ键总数为________ 个。分子中的大π键可用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为________ 。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为________ (填化学式)。
④血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过________ 键相结合的。
(4)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为________________ 。H2SO4的酸性强于H2SO3的原因是______________________________________________________________ 。
(1)基态Cu原子的价电子排布式为
(2)从原子结构角度分析,第一电离能I1(Fe)与I1(Cu)的关系是:I1(Fe)
(3)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如下图:

①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为
②1 mol吡咯分子中所含的σ键总数为
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为
④血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过
(4)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)下列氮原子的不同的电子排布。
A.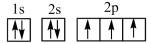 B.
B.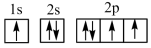
C.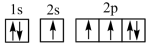 D.
D.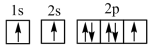
能量最高的是_______ ;其电子在发生跃迁时,不能产生发射光谱的是_______ 。
(2)铵盐与碱加热可制备氨气。NH 转化为NH3过程中,没有发生变化的是
转化为NH3过程中,没有发生变化的是_______ 。
A.键角 B.粒子的空间结构 C.杂化方式
(3)已知离子核外没有未成对d电子的过渡金属离子形成的水合离子是无色的,Ti4+、V3+、Ni2+三种离子的水合离子无颜色的是_______ (填离子符号)。
(4)共价化合物CrO5中有4个-1价的O,CrO5中σ键与π键个数比为_______ 。
(5)N、O、S的第一电离能( )大小为I1(N)>I1(O)>I1(S),原因是
)大小为I1(N)>I1(O)>I1(S),原因是_______
(6)氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为_______ ;
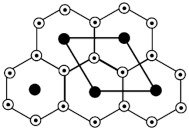
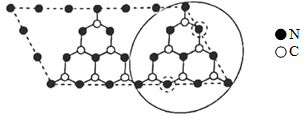
(7)g-C3N4具有和石墨相似的层状结构,其中一种二维平面结构如下图所示。每个基本结构单元(图中实线圈部分)中两个N原子(图中虚线圈所示)被O原子代替,形成O掺杂的g-C3N4(OPCN)。OPCN的化学式为_______ 。
(1)下列氮原子的不同的电子排布。
A.
 B.
B.
C.
 D.
D.
能量最高的是
(2)铵盐与碱加热可制备氨气。NH
 转化为NH3过程中,没有发生变化的是
转化为NH3过程中,没有发生变化的是A.键角 B.粒子的空间结构 C.杂化方式
(3)已知离子核外没有未成对d电子的过渡金属离子形成的水合离子是无色的,Ti4+、V3+、Ni2+三种离子的水合离子无颜色的是
(4)共价化合物CrO5中有4个-1价的O,CrO5中σ键与π键个数比为
(5)N、O、S的第一电离能(
 )大小为I1(N)>I1(O)>I1(S),原因是
)大小为I1(N)>I1(O)>I1(S),原因是(6)氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为

(7)g-C3N4具有和石墨相似的层状结构,其中一种二维平面结构如下图所示。每个基本结构单元(图中实线圈部分)中两个N原子(图中虚线圈所示)被O原子代替,形成O掺杂的g-C3N4(OPCN)。OPCN的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硫脲[SC(NH2)2]别名硫代尿素,是一种白色固体,熔点182℃。硫脲可代替氰化物用于提炼金的新工艺。酸性条件下,硫脲在氧化剂(如Fe3+、H2O2、O2)存在下能溶解金,形成配离子Au[SC(NH2)2] 。
。
回答下列问题:
(1)C、N、S三种元素中第一电离能最大的是___ (填元素符号)。
(2)Au与Cu同族,价电子排布式为5d106s1,Au位于元素周期表的___ 区,Au+的价电子排布式为___ 。
(3)硫脲分子中碳原子的杂化方式为___ ,σ键和π键数目之比为___ 。
(4)写出硫脲在硫酸铁存在下溶解金的离子方程式___ 。
(5)硫脲加热到150℃时可转变成硫氰酸铵(NH4SCN),SCN-的空间构型为___ 形。
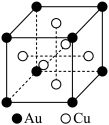
(6)一种铜金合金晶体具有面心立方最密堆积的结构,其晶胞如图所示,则该合金中Au原子与Cu原子个数之比为___ 。若铜和金的半径分别为apm和bpm,相对原子质量分别为MA和MB,阿伏加 德罗常数的值为NA,计算晶体的密度为___ g/cm3。
 。
。回答下列问题:
(1)C、N、S三种元素中第一电离能最大的是
(2)Au与Cu同族,价电子排布式为5d106s1,Au位于元素周期表的
(3)硫脲分子中碳原子的杂化方式为
(4)写出硫脲在硫酸铁存在下溶解金的离子方程式
(5)硫脲加热到150℃时可转变成硫氰酸铵(NH4SCN),SCN-的空间构型为
(6)一种铜金合金晶体具有面心立方最密堆积的结构,其晶胞如图所示,则该合金中Au原子与Cu原子个数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氮是生命物质的重要组成元素之一,氮及其化合物与我们的生产、科研密切相关。
(1) 通过衰变反应可获得
通过衰变反应可获得 。
。
①基态 原子的价电子排布图为
原子的价电子排布图为___ ,其核外电子有__ 种运动状态。
②第二周期元素的第一电离能介于C、N之间的为___ (填元素符号)。
(2)某科研机构曾预想合成一个纯粹由氮组成的新物种——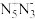 ,以取代有毒的肼类火箭燃料。
,以取代有毒的肼类火箭燃料。 的空间构型为
的空间构型为___ 。
(3)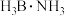 是一种有效、安全的固体储氢材料,可由
是一种有效、安全的固体储氢材料,可由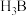 与
与 反应生成,B与N之间形成配位键,氮原子提供
反应生成,B与N之间形成配位键,氮原子提供___ ,在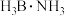 中B原子的杂化方式为
中B原子的杂化方式为___ 。
(4)在高压下氮气会发生聚合得到高聚氮,这种高聚氮晶体中每个氮原子都通过三个单键与其他氮原子结合并向空间发展构成立体网状结构。该晶体的结构片段如图所示:
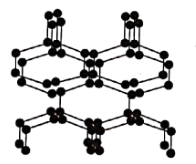
高聚氮晶体属于_____ 晶体,高聚氮晶体中n(N):n(N-N)=____ 。
(1)
 通过衰变反应可获得
通过衰变反应可获得 。
。①基态
 原子的价电子排布图为
原子的价电子排布图为②第二周期元素的第一电离能介于C、N之间的为
(2)某科研机构曾预想合成一个纯粹由氮组成的新物种——
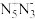 ,以取代有毒的肼类火箭燃料。
,以取代有毒的肼类火箭燃料。 的空间构型为
的空间构型为(3)
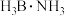 是一种有效、安全的固体储氢材料,可由
是一种有效、安全的固体储氢材料,可由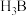 与
与 反应生成,B与N之间形成配位键,氮原子提供
反应生成,B与N之间形成配位键,氮原子提供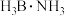 中B原子的杂化方式为
中B原子的杂化方式为(4)在高压下氮气会发生聚合得到高聚氮,这种高聚氮晶体中每个氮原子都通过三个单键与其他氮原子结合并向空间发展构成立体网状结构。该晶体的结构片段如图所示:

高聚氮晶体属于
您最近一年使用:0次



