一种无机纳米晶体材料,仅由铯、铅、溴三种元素构成,在太阳能电池方向有巨大应用前景。回答下列问题:
(1)基态 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为_______ 。 属于
属于_______ 区元素。
(2)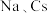 位于同主族,
位于同主族,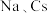 元素的第一电离能分别为
元素的第一电离能分别为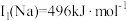 、
、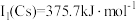 。
。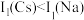 的原因是
的原因是_______ 。
(3) 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是_______ 。
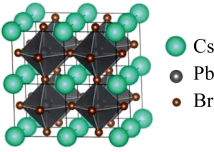
(4)该晶体材料的立方结构如图所示,其化学式为_______ 。若其晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度=_______  。
。
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是_______ 。
②某大学采用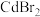 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,_______ (离子)脱离晶格,用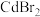 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是_______ 。
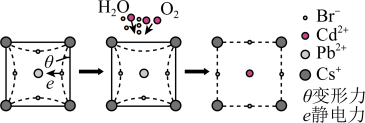
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
(1)基态
 原子核外电子占据能量最高的能级的电子云轮廓图形状为
原子核外电子占据能量最高的能级的电子云轮廓图形状为 属于
属于(2)
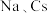 位于同主族,
位于同主族,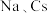 元素的第一电离能分别为
元素的第一电离能分别为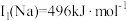 、
、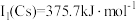 。
。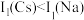 的原因是
的原因是(3)
 三种元素的电负性如下表。
三种元素的电负性如下表。 具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是
具有较高的熔点(855℃),PbBr2具有较低的熔点(373℃),原因是| 电负性 | ||
| F | Br | Pb |
| 4.0 | 2.8 | 1.9 |
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体密度=
,则该晶体密度= 。
。
(5)该晶体材料电池并未实现商业化,原因在于自身的不稳定性。
①该晶体材料在潮湿环境中易从固体变成溶液(发生相变),导致器件效率降低,其原因是
②某大学采用
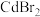 对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,
对该材料进行钝化处理可有效提高其稳定性,钝化机理如图所示。根据晶格应变驰豫,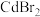 钝化后的晶体比原晶体材料更稳定,其原因是
钝化后的晶体比原晶体材料更稳定,其原因是
(已知:应力与应变相伴而生,从原子尺度上来理解,应力为单位晶格上的作用力,应变即为晶格的拉伸或收缩,对应于拉伸应变和压缩应变。对应出现的驰豫是指一个宏观平衡系统由于受到外界的作用变为非平衡状态,再从非平衡状态过渡到新的平衡态的过程。)
2022·河北邢台·模拟预测 查看更多[2]
更新时间:2022-05-05 13:45:32
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】在下图所示的转化关系中,A~J分别表示中学化学中常见的一种物质,其中部分反应物、生成物没有列出。已知反应③是一种重要的工业生产原理,A、B、C、D、E、F六种物质中含有同一种元素。请回答下列问题:
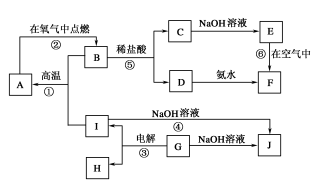
(1)I、G、J三种物质中所含同一种元素在周期表中的位置是_______ 。
(2)写出反应④的离子方程式_________ 。
(3)写出反应⑥的化学方程式_________ 。
(4)写出反应③的电极反应式:阳极:______ ;阴极:______ 。
(5)从能量变化的角度看,①②③④反应中焓变ΔH<0的反应是_____ 。(填序号)
(6)A、B、C、D、E、F六种物质中所含同一种元素的电子排布式________ 。

(1)I、G、J三种物质中所含同一种元素在周期表中的位置是
(2)写出反应④的离子方程式
(3)写出反应⑥的化学方程式
(4)写出反应③的电极反应式:阳极:
(5)从能量变化的角度看,①②③④反应中焓变ΔH<0的反应是
(6)A、B、C、D、E、F六种物质中所含同一种元素的电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】钛被视为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”,钛和钛的化合物在航天、化工、建筑、医疗中都有着广泛的用途。回答下列问题:
(1)基态钛原子核外有___________ 种能量不同的电子, 的电子排布式为
的电子排布式为___________ 。
(2)钛与卤素形成的化合物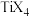 熔点如下表
熔点如下表
它们熔点差异的原因___________ 。
(3) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
① 与
与 互为等电子体,
互为等电子体, 的空间构型为
的空间构型为______ 。
② 由
由 和
和 构成,
构成, 中B原子的杂化类型是
中B原子的杂化类型是______ , 所含元素电负性由小到大的顺序为
所含元素电负性由小到大的顺序为______
③ 中存在的作用力为
中存在的作用力为______ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)有一种氮化钛晶体的晶胞与 晶胞相似,该晶体的晶胞参数为
晶胞相似,该晶体的晶胞参数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为_______  。用
。用 掺杂
掺杂 后,其晶胞结构如下图所示,距离
后,其晶胞结构如下图所示,距离 最近的
最近的 有
有______ 个。( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

(1)基态钛原子核外有
 的电子排布式为
的电子排布式为(2)钛与卤素形成的化合物
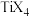 熔点如下表
熔点如下表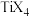 |  |  |  |  |
| 熔点℃ | 377 |  | 38.3 | 153 |
(3)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①
 与
与 互为等电子体,
互为等电子体, 的空间构型为
的空间构型为②
 由
由 和
和 构成,
构成, 中B原子的杂化类型是
中B原子的杂化类型是 所含元素电负性由小到大的顺序为
所含元素电负性由小到大的顺序为③
 中存在的作用力为
中存在的作用力为A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)有一种氮化钛晶体的晶胞与
 晶胞相似,该晶体的晶胞参数为
晶胞相似,该晶体的晶胞参数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为 。用
。用 掺杂
掺杂 后,其晶胞结构如下图所示,距离
后,其晶胞结构如下图所示,距离 最近的
最近的 有
有 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
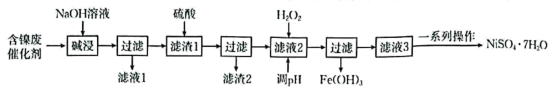
已知:①常温下,部分金属化合物的 近似值如表所示:
近似值如表所示:
②金属活泼性: 。
。
③ 。
。
回答下列问题:
(1) 元素在元素周期表中的位置为
元素在元素周期表中的位置为_______ ,其基态原子的价层电子排布式为_______ 。
(2)“滤液1”中的主要溶质为 、
、_______ 。
(3)加入硫酸时, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)加入 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤_______ (填“能”或“不能”)用适量稀硝酸代替,理由是_______ 。然后调节溶液的 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为_______ (保留3位有效数字,离子浓度小于或等于 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是_______ 。
(5)用配位滴定法测定粗品中 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是_______ %;下列操作会使测定结果偏低的是_______ (填标号)。
A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
已知:①常温下,部分金属化合物的
 近似值如表所示:
近似值如表所示:| 化学式 |  |  | 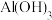 |  |  |
 近似值 近似值 | 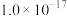 | 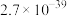 | 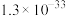 | 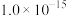 |  |
 。
。③
 。
。回答下列问题:
(1)
 元素在元素周期表中的位置为
元素在元素周期表中的位置为(2)“滤液1”中的主要溶质为
 、
、(3)加入硫酸时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)加入
 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是(5)用配位滴定法测定粗品中
 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】根据表中五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列问题:
(1)在周期表中,最可能处于同一族的是_______ (填序号,下同)。
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是______
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是_____
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是_______ 区元素,其氯化物的化学式为_______ 。
(5)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明了原子核外_______ ,如果U元素是短周期的元素,你估计它的第二次电离能飞跃数据将是第_______ 个。
(6)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是_______ ,其中元素_______ 的第一电离能反常高的原因是_______ 。
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是
A.硼 B.铍 C.氦 D.氢
(4)T元素最可能是
(5)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明了原子核外
(6)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】H、C、N、O、Na、Fe、Cu是常见的七种元素,请回答下列问题:
(1)N、O、Na原子第一电离能由小到大的顺序是_______ (用元素符号和“<”表示); Cu原子的价电子排布图为_______ 。
(2)Fe3+、Cu2+基态的核外电子排布式中未成对电子数最多的是_______ ; Cu2+在水中呈现蓝色是因为形成了水合铜离子,其化学式为_______ ,水分子与铜离子间结合的化学键名称为_______ 。
(3)根据价层电子对互斥理论判断下列分子或离子中空间构型是V形的是_______ (填序号)。
①H3O+②H2O ③NO
(4)(CN)2分子中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为_______ ,1个分子中含有_______ 个π键;则(CN)2中C原子的杂化类型为_______ 。
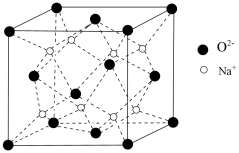
(5)O和Na形成的一种只含有离子键的离子化合物,其晶胞结构如图,该离子化合物的化学式为_______ ;已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a=_______ cm。(用含p、NA的代数式表示)
(1)N、O、Na原子第一电离能由小到大的顺序是
(2)Fe3+、Cu2+基态的核外电子排布式中未成对电子数最多的是
(3)根据价层电子对互斥理论判断下列分子或离子中空间构型是V形的是
①H3O+②H2O ③NO
(4)(CN)2分子中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
(5)O和Na形成的一种只含有离子键的离子化合物,其晶胞结构如图,该离子化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】碳酸二甲酯(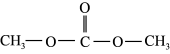 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
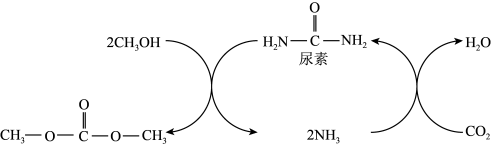
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②_______ 。
(2)下列有关 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。
(3)含钛、铁、铜、锌的催化剂在制备碳酸二甲酯的过程中,催化效果较好。
①基态钛原子核外s能级和p能级的电子数之比为_______ 。
②含钛新型正极材料 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为_______ 。
③已知:存在未成对电子的金属离子具有顺磁性。 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是_______ (填离子符号);这四种金属离子各1mol中,未成对电子数最多的金属离子是_______ (填离子符号)。
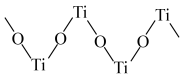
④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为_______ 。
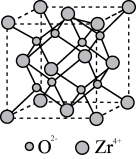
(4)在 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是_______ 。若该晶胞的密度为 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是_______  (列出计算式)。
(列出计算式)。
 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②
(2)下列有关
 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。A. 的键角小于 的键角小于 的键角,是因为 的键角,是因为 的中心原子上孤电子对对成键电子对有较大的斥力 的中心原子上孤电子对对成键电子对有较大的斥力 |
B. 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 |
C. 的沸点比 的沸点比 的高,是因为N-H键能比P-H键能大 的高,是因为N-H键能比P-H键能大 |
D.1mol 中含有12molσ键 中含有12molσ键 |
①基态钛原子核外s能级和p能级的电子数之比为
②含钛新型正极材料
 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为③已知:存在未成对电子的金属离子具有顺磁性。
 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为

(4)在
 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】金属钛(Ti)被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)基态Ti原子的电子排布式为[Ar]___________ ,Ti原子核外有___________ 种空间运动状态不同的电子。
(2)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是___________ ,H、B、Ti的电负性由大到小的顺序为___________ 。
(3)锆(Zr)与钛(Ti)是同一副族的相邻元素,ZrCl4可以与乙二胺(H2NCH2CH2NH2)形成六配位化合物[ZrCl4(H2NCH2CH2NH2)]。
①乙二胺中,N原子的杂化方式为___________ 。
②1mol[ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为___________ mol。
③乙二胺形成配合物后,H-N-H键角将变大,原因是___________ 。
(4)钙钛矿(主要成分CaTiO3),晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则相距最近的Ca和O之间的距离为___________ pm(列出计算式)。

(1)基态Ti原子的电子排布式为[Ar]
(2)Ti(BH4)2是一种储氢材料。BH
 的空间构型是
的空间构型是(3)锆(Zr)与钛(Ti)是同一副族的相邻元素,ZrCl4可以与乙二胺(H2NCH2CH2NH2)形成六配位化合物[ZrCl4(H2NCH2CH2NH2)]。
①乙二胺中,N原子的杂化方式为
②1mol[ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为
③乙二胺形成配合物后,H-N-H键角将变大,原因是
(4)钙钛矿(主要成分CaTiO3),晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则相距最近的Ca和O之间的距离为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】我国科学家及其合作团队研究发现,六方相(hcp)Fe—H、Fe—C和Fe—O合金在地球内核温压下转变成超离子态。该研究表明地球内核并非传统认知的固态,而是由固态铁和流动的轻元素组成的超离子态。请用所学知识回答下列问题:
(1)基态铁原子最外层电子所在能级的电子云轮廓图为_______ 形。
(2)H、C、O三种元素的电负性由大到小的排序为_______ (填元素符号)。
(3)锰和铁处于同一周期,锰、铁电离能数据如表所示:
请解释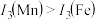 的主要原因:
的主要原因:_______ 。
(4)H、C,O三种元素可以组成很多种物质。
① 、
、 、
、 、
、 、
、 中属于非极性分子的有
中属于非极性分子的有_______ (填化学式),其中 的立体构型为
的立体构型为_______ 。
②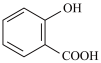 的沸点
的沸点_______ (填“大于”、“小于”或“等于”)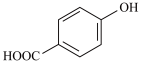 的沸点。
的沸点。
(5)用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。
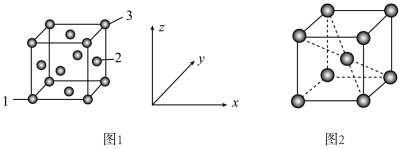
①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为_______ 。
②若图2中晶胞参数为apm,设 为阿伏加德罗常数的值,则晶体的密度为
为阿伏加德罗常数的值,则晶体的密度为_______ (用含a、 的代数式表示)
的代数式表示) 。
。
(1)基态铁原子最外层电子所在能级的电子云轮廓图为
(2)H、C、O三种元素的电负性由大到小的排序为
(3)锰和铁处于同一周期,锰、铁电离能数据如表所示:
| 元素 | 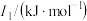 |  |  |
| Mn | 717.3 | 1509.9 | 3248 |
| Fe | 762.5 | 1561.9 | 2953 |
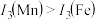 的主要原因:
的主要原因:(4)H、C,O三种元素可以组成很多种物质。
①
 、
、 、
、 、
、 、
、 中属于非极性分子的有
中属于非极性分子的有 的立体构型为
的立体构型为②
 的沸点
的沸点 的沸点。
的沸点。(5)用X射线衍射仪测定发现铁晶体有两种晶胞结构,如图1、图2所示。

①原子坐标参数可以描述晶胞内部各微粒的相对位置。设图1中1号原子的坐标参数为(0,0,0),3号原子的坐标参数为(1,1,1),则2号原子的坐标参数为
②若图2中晶胞参数为apm,设
 为阿伏加德罗常数的值,则晶体的密度为
为阿伏加德罗常数的值,则晶体的密度为 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】Ⅰ、用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。 (1—4小题填序号)
(1) 由离子键和非极性键构成的是_________________
(2) 由极性键和非极性键构成的是_________________
(3) 不存在化学键的是________
(4) 共价化合物有_________________
(5) 写出下列物质的电子式:Na2O2___________
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第________ 周期________ 族,属________ 区元素
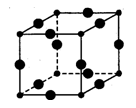
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为____ ,Cu+半径为acm,N3-半径为bcm,Cu3N的密度为_________ g·cm-3。(阿伏加德罗常数用NA表示,Cu、N相对分子质量为64、14)
(1) 由离子键和非极性键构成的是
(2) 由极性键和非极性键构成的是
(3) 不存在化学键的是
(4) 共价化合物有
(5) 写出下列物质的电子式:Na2O2
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】【化学——选修3 物质结构与性质】
铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置为_________________________ 。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于______________ (填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=____________ 。Fe(CO)x在一定条件下发生反应:Fe(CO)x(s)=Fe(s)+xCO(g)。已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有_______________ 、_____________ 。
(3)K3[Fe(CN)6]溶液可用于检验___________ (填离子符号)。CN-中碳原子杂化轨道类型为__________ ,C、N、O三元素的第一电离能由大到小的顺序为__________ (用元素符号表示)。
(4)铜晶体铜碳原子的堆积方式如右图所示。

①基态铜原子的核外电子排布式为____________________ 。
②每个铜原子周围距离最近的铜原子数目___________________ 。
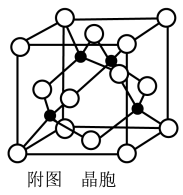
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子,空心圆代表M原子)。
①该晶体的化学式为_________________ 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于____________ (填“离子”或“共价”)化合物。
③已知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子与M原子之间的最短距离为_______________ pm(只写计算式)。
铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置为
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(3)K3[Fe(CN)6]溶液可用于检验
(4)铜晶体铜碳原子的堆积方式如右图所示。

①基态铜原子的核外电子排布式为
②每个铜原子周围距离最近的铜原子数目
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子,空心圆代表M原子)。

①该晶体的化学式为
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
③已知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子与M原子之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】C、N和Si能形成多种高硬度材料,如 。
。
(1) 和
和 中硬度较高的是
中硬度较高的是_______ ,理由是_______ 。
(2)C和N能形成一种类石墨结构材料,其合成过程如下图。该类石塑结构材料化合物的化学式为_______ 。

(3)C和N还能形成一种五、元环状有机物咪唑(im),其结构为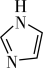 。化合物
。化合物 的结构示意图如下:
的结构示意图如下:

①基态Co原子的价层电子轨道表达式(价层电子排布图)为_______ 。
②N与Co之间的共价键类型是配位键,判断的理由是_______ 。
③阴离子 中心原子
中心原子 的价层电子对数为
的价层电子对数为_______ 。阳离子 和
和 之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式
之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式_______ 。例如水中氢键的表示式为: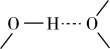
(4)晶胞内部各微粒的相对位置可以用原子坐标参数表示。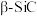 为立方晶系晶体,其晶胞中原子的坐标为
为立方晶系晶体,其晶胞中原子的坐标为
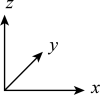
C: ;……
;……
Si: 。
。
①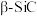 立方晶胞中含有
立方晶胞中含有_______ 个Si原子、_______ 个C原子;
②已知晶胞参数为a,Si原子半径为 ,C原子半径为
,C原子半径为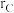 ,该晶胞中原子的体积占晶胞体积的百分率为
,该晶胞中原子的体积占晶胞体积的百分率为_______ (列出计算式即可)。
 。
。(1)
 和
和 中硬度较高的是
中硬度较高的是(2)C和N能形成一种类石墨结构材料,其合成过程如下图。该类石塑结构材料化合物的化学式为

(3)C和N还能形成一种五、元环状有机物咪唑(im),其结构为
 。化合物
。化合物 的结构示意图如下:
的结构示意图如下:
①基态Co原子的价层电子轨道表达式(价层电子排布图)为
②N与Co之间的共价键类型是配位键,判断的理由是
③阴离子
 中心原子
中心原子 的价层电子对数为
的价层电子对数为 和
和 之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式
之间除了阴阳离子间的静电作用力,还存在氢键作用,画出该氢键的表示式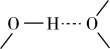
(4)晶胞内部各微粒的相对位置可以用原子坐标参数表示。
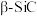 为立方晶系晶体,其晶胞中原子的坐标为
为立方晶系晶体,其晶胞中原子的坐标为
C:
 ;……
;……Si:
 。
。①
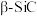 立方晶胞中含有
立方晶胞中含有②已知晶胞参数为a,Si原子半径为
 ,C原子半径为
,C原子半径为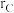 ,该晶胞中原子的体积占晶胞体积的百分率为
,该晶胞中原子的体积占晶胞体积的百分率为
您最近一年使用:0次
【推荐3】绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
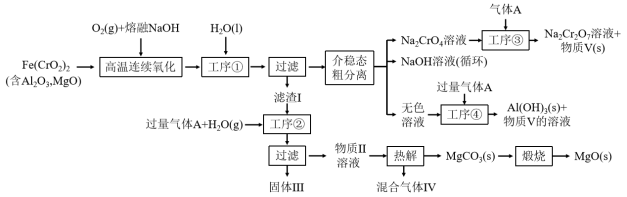
回答下列问题:
(1)高温连续氧化工序中被氧化的元素是_______ (填元素符号),Cr元素在元素周期表中的位置_______ ,
(2)滤渣I的主要成分是_______ (填化学式)。
(3)工序③中发生反应的离子方程式为_______ 。
(4)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_____ 。钠在火焰上灼烧产生的黄光是一种_______ (填“吸收光谱” 或“发射光谱”)。
(5)工序④溶液中的铝元素恰好完全转化为沉淀的pH为_______ 。(通常认为溶液中离子浓度小于10-5mol•L-1为沉淀完全;A1(OH)3+OH-⇌Al(OH) :K=100.63,Kw=10-14,Ksp[A1(OH)3]=10-33)
:K=100.63,Kw=10-14,Ksp[A1(OH)3]=10-33)
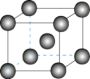
(6)基态Al原子的核外电子排布式为_______ 。Fe的晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,若晶胞参数为a nm,则Fe晶胞的密度为_______ g•cm-3(用含NA和a的代数式表示)。

回答下列问题:
(1)高温连续氧化工序中被氧化的元素是
(2)滤渣I的主要成分是
(3)工序③中发生反应的离子方程式为
(4)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为
(5)工序④溶液中的铝元素恰好完全转化为沉淀的pH为
 :K=100.63,Kw=10-14,Ksp[A1(OH)3]=10-33)
:K=100.63,Kw=10-14,Ksp[A1(OH)3]=10-33)(6)基态Al原子的核外电子排布式为

您最近一年使用:0次



