反应aA(g)+bB(g) cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:回答问题:
cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:回答问题:
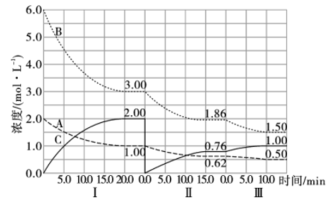
(1)反应的化学方程式中,a:b:c为_______ 。
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为_______ 。
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是_______ 。
(4)由第一次平衡到第二次平衡,平衡移动的方向是_______ ,采取的措施是_______ 。
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低:T2_______ T3(填“>”“=”“<”),判断的理由是_______ 。
 cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:回答问题:
cC(g) △H<0在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如图所示:回答问题:
(1)反应的化学方程式中,a:b:c为
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为
(3)B的平衡转化率αI(B)、αII(B)、αIII(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡移动的方向是
(5)比较第II阶段反应温度(T2)和第III阶段反应温度(T3)的高低:T2
更新时间:2022-05-13 17:00:10
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】
(1)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
①5min末A的物质的量浓度为______________ mol/L·
②前5min内用B表示的化学反应速率v(B)为_________ mol/(L·min)。
③化学方程式中X值为__________ 。
④此反应在四种不同情况下的反应速率分别为:①v(A)=5mol/(L·min);②v(B)=6mol/(L·min);③v(C)=4.5mol/(L·min);④v(D)=8mol/(L·min)。其中反应速率最快的是__________ (填编号)。
(2)相对分子质量为72的烷烃,它的一氯代物只有一种,此烷烃的结构简式为_________ 。
(3)某气态烷烃和一气态烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48 L,通入足量的溴水,溴水质量增加2.8 g,此两种烃的组成为______________ (填分子式)。
(4)有机物的结构可用“键线式”表示,如: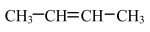 可简写为
可简写为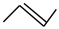 .
. 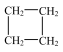 可简写为
可简写为  。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,
。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,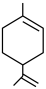 ,苧烯的分子式为
,苧烯的分子式为___________ 。
(1)在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)
 3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算
3C(g)+XD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。计算①5min末A的物质的量浓度为
②前5min内用B表示的化学反应速率v(B)为
③化学方程式中X值为
④此反应在四种不同情况下的反应速率分别为:①v(A)=5mol/(L·min);②v(B)=6mol/(L·min);③v(C)=4.5mol/(L·min);④v(D)=8mol/(L·min)。其中反应速率最快的是
(2)相对分子质量为72的烷烃,它的一氯代物只有一种,此烷烃的结构简式为
(3)某气态烷烃和一气态烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48 L,通入足量的溴水,溴水质量增加2.8 g,此两种烃的组成为
(4)有机物的结构可用“键线式”表示,如:
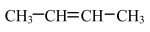 可简写为
可简写为 .
. 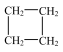 可简写为
可简写为  。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,
。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图, ,苧烯的分子式为
,苧烯的分子式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I.汽车行驶、某些化工厂生产过程,会向空气中排放出NOx、CO、SO2等有害气体,影响生态环境。
(1)汽油中含有某种烃A。已知A的相对分子质量为100,其中氢元素的质量分数为16%,A的分子式为____ 。
II.为防止氮的氧化物污染空气,可用氨或活性炭还原氮氧化物。回答下列问题:
(2)为了减少重型柴油车排放NOx,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为NH3,NH3再与NOx反应生成两种无污染的物质。
①写出其中NH3与NO在一定条件下反应的化学方程式:____ 。
②为提高此反应的速率,下列措施可行的是_____ (填字母代号)。
A.缩小容器体积 B.降低温度 C.使用适合催化剂 D.移出产物
(3)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g) N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
①温度为T1℃时,0~5min内,以CO2表示的该反应的平均速率v(CO2)=____ mol·L-1·min-1;反应达到最大限度(即平衡状态)时,混合气体中N2的物质的量分数为____ 。从反应开始到建立平衡的过程中,体系内气体的总压强____ (填“变大”“变小”或“不变”)。
②两容器中的温度关系为T1____ T2(填“>”“<”或“=”)。
③下列情况能说明该反应C(s)+2NO(g) N2(g)+CO2(g)达到平衡状态的是
N2(g)+CO2(g)达到平衡状态的是____ 。
A.2v正(NO)=v逆(CO2)
B.混合气体中N2的体积分数保持不变
C.单位时间内断裂1个N≡N同时生成1个C=O
D.恒温、恒容条件下,混合气体的密度保持不变
E.恒温、恒容条件下,混合气体的平均摩尔质量保持不变
(1)汽油中含有某种烃A。已知A的相对分子质量为100,其中氢元素的质量分数为16%,A的分子式为
II.为防止氮的氧化物污染空气,可用氨或活性炭还原氮氧化物。回答下列问题:
(2)为了减少重型柴油车排放NOx,向尾气处理装置内自动喷入的尿素溶液在一定条件下先转化为NH3,NH3再与NOx反应生成两种无污染的物质。
①写出其中NH3与NO在一定条件下反应的化学方程式:
②为提高此反应的速率,下列措施可行的是
A.缩小容器体积 B.降低温度 C.使用适合催化剂 D.移出产物
(3)向两个1L的密闭容器中各加入活性炭(足量)和1.0molNO,发生反应为:C(s)+2NO(g)
 N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:
N2(g)+CO2(g)。实验测得不同温度下NO和N2的物质的量变化如表所示:| 温度/℃ | 物质的量/mol | 时间 | ||||
| 0 | 5min | 9min | 10min | 12min | ||
| T1 | NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 |
| N2 | 0 | 0.21 | 0.29 | x | x | |
| T2 | NO | 1.0 | 0.50 | 0.34 | 0.34 | |
| N2 | 0 | 0.25 | 0.33 | 0.33 | ||
②两容器中的温度关系为T1
③下列情况能说明该反应C(s)+2NO(g)
 N2(g)+CO2(g)达到平衡状态的是
N2(g)+CO2(g)达到平衡状态的是A.2v正(NO)=v逆(CO2)
B.混合气体中N2的体积分数保持不变
C.单位时间内断裂1个N≡N同时生成1个C=O
D.恒温、恒容条件下,混合气体的密度保持不变
E.恒温、恒容条件下,混合气体的平均摩尔质量保持不变
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g) N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
(1)上述反应的熵变ΔS_________ (填“>”“<”或“=”,下同)0,该反应能够自发进行,则反应的ΔH_______ 0。
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是____________ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
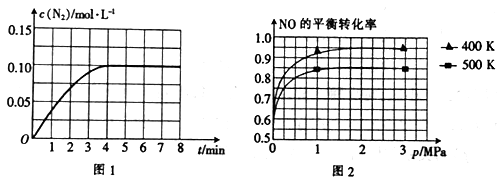
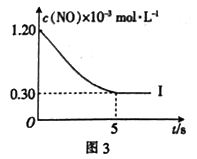
(3)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=_________ ,4 min末CO的浓度为_________________ 。
(4)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是____________________ 。
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
请在图3中分别画出上表中实验Ⅱ、Ⅲ条件下混合气体中NO的浓度随时间变化的曲线,并标明各条曲线的实验编号__________ 。
 N2(g)+2CO2(g)。
N2(g)+2CO2(g)。(1)上述反应的熵变ΔS
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=
(4)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是

(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了以下三组实验:
| 实验编号 | T(K) | NO的初始浓度 (mol·L-1) | CO的初始浓度 (mol·L-1) | 催化剂的比表面积 (m2·g-1) |
| I | 400 | 1.20×10-3 | 3.80×10-3 | 75 |
| Ⅱ | 400 | 1.20×10-3 | 3.80×10-3 | 100 |
| Ⅲ | 450 | 1.20×10-3 | 3.80×10-3 | 100 |
请在图3中分别画出上表中实验Ⅱ、Ⅲ条件下混合气体中NO的浓度随时间变化的曲线,并标明各条曲线的实验编号

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气方法,氨热分解法制氢气。
相关化学键的键能数据
一定温度下,利用催化剂将 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:
(1)反应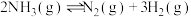

_______  ;
;
(2)已知该反应的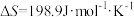 ,在下列哪些温度下反应能自发进行?_______(填标号)
,在下列哪些温度下反应能自发进行?_______(填标号)
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol 通入3L的密闭容器中进行反应(此时容器内总压为2kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为2kPa),各物质的分压随时间的变化曲线如图所示。
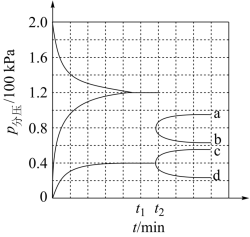
①若保持容器体积不变, 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示0~
的浓度变化表示0~ 时间内的反应速率
时间内的反应速率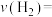
_______  (用含
(用含 的代数式表示)
的代数式表示)
②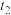 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是_______ (用图中a、b、c、d表示),理由是_______ ;
③在该温度下,反应的平衡常数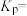
_______ 。
相关化学键的键能数据
| 化学键 | N≡N | H−H | N−H |
键能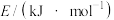 | 946 | 436.0 | 390.8 |
一定温度下,利用催化剂将
 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:(1)反应
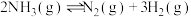

 ;
;(2)已知该反应的
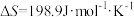 ,在下列哪些温度下反应能自发进行?_______(填标号)
,在下列哪些温度下反应能自发进行?_______(填标号)| A.25℃ | B.125℃ | C.225℃ | D.325℃ |
 通入3L的密闭容器中进行反应(此时容器内总压为2kPa),各物质的分压随时间的变化曲线如图所示。
通入3L的密闭容器中进行反应(此时容器内总压为2kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变,
 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示0~
的浓度变化表示0~ 时间内的反应速率
时间内的反应速率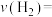
 (用含
(用含 的代数式表示)
的代数式表示)②
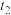 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是③在该温度下,反应的平衡常数
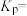
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知2NO2(g)=N2O4(g) △H=﹣52.7kJ•mol﹣1,常温下N2O4为无色气体。某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体(NH4NO3固体溶解吸收大量的热)。请回答:
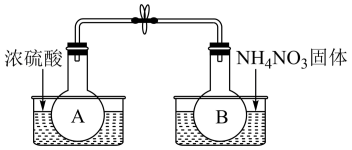
(1)A中的现象___________ ,B中的现象___________ ;
(2)由此可知,降低温度,该化学平衡向___________ (填“正”或“逆”)反应方向移动;
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3相同浓度的NO2与N2O4的混合气体,将针筒前端封闭。
(3)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后气体颜色变深的原因是___________ ;
②一段时间后气体颜色又变浅的原因是___________ ;
(4)将第三支针筒活塞拉至20cm3处,此时气体的颜色___________ ,一段时间后气体颜色___________ ,但仍比第一支针筒气体的颜色___________ 。
①在此过程中,该反应的化学平衡常数___________ (填“增大”、“减小”或“不变”)。
②NO2的转化率___________ (填“增大”、“减小”或“不变”)。
Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体(NH4NO3固体溶解吸收大量的热)。请回答:

(1)A中的现象
(2)由此可知,降低温度,该化学平衡向
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3相同浓度的NO2与N2O4的混合气体,将针筒前端封闭。
(3)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后气体颜色变深的原因是
②一段时间后气体颜色又变浅的原因是
(4)将第三支针筒活塞拉至20cm3处,此时气体的颜色
①在此过程中,该反应的化学平衡常数
②NO2的转化率
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氨在国防、工农业等领域发挥着重要作用。
(1)工业以甲烷为原料生产氨气的过程如下:甲烷 氢气
氢气 氨气
氨气
①过程Ⅰ中,有关化学反应的能量变化如下图所示

反应①为______ 反应(填吸热或放热),CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是___________________ 。
②CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:
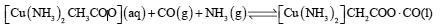 ,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是
,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是_______________ 。(选填字母)。
a.高温、高压b.高温、低压
c.低温、低压d.低温、高压
③下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数
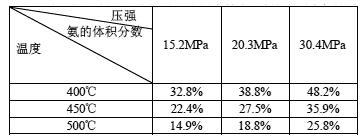
Ⅰ.根据表中数据,得出的结论是____________________ 。
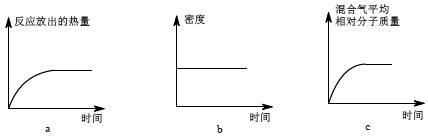
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n(N2)= 0.1mol,
n(H2)= 0.3mol。下列图象能正确表示该过程中相关量的变化的是_________ 。(选填字母)。
(2)直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:

①负极的电极反应式是______ 。
②用该电池电解300ml的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是_____ L。(标准状况)
(1)工业以甲烷为原料生产氨气的过程如下:甲烷
 氢气
氢气 氨气
氨气①过程Ⅰ中,有关化学反应的能量变化如下图所示

反应①为
②CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:
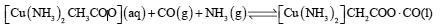 ,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是
,所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是a.高温、高压b.高温、低压
c.低温、低压d.低温、高压
③下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数

Ⅰ.根据表中数据,得出的结论是
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n(N2)= 0.1mol,
n(H2)= 0.3mol。下列图象能正确表示该过程中相关量的变化的是

(2)直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:

①负极的电极反应式是
②用该电池电解300ml的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】研究高效催化剂是解决汽车尾气中的NO和CO对大气污染的重要途径。
(1)已知: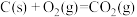


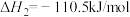
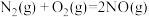

则汽车尾气的催化转化反应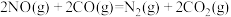 属于反应
属于反应______ (放热或吸热)。
(2)400℃时,在分别装有催化剂A和B的两个容积为2L的刚性密闭容器中,各充入物质的量均为 的
的 和
和 发生上述反应。通过测定容器内总压强随时间变化来探究催化剂对反应速率的影响,数据如下表;
发生上述反应。通过测定容器内总压强随时间变化来探究催化剂对反应速率的影响,数据如下表;
①由上表可以判断催化剂______ (填“A”或“B”)的效果更好。
②容器中 的平衡转化率为
的平衡转化率为______ 。
③汽车尾气排气管中使用催化剂可以提高污染物转化率,其原因是______ 。
(3)为研究气缸中 的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为
的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为 的氮气和氧气,发生反应
的氮气和氧气,发生反应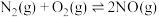 。
。
①下列说法能表明该反应已经达到平衡状态的是______ (填序号)。
A.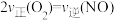 B.混合气体的平均相对分子质量不变
B.混合气体的平均相对分子质量不变
C. D.容器内气体的密度不再发生变化
D.容器内气体的密度不再发生变化
②为减小平衡混合气中NO体积分数,可采取的措施是_____ 。(填升高温度或降低温度)
(4)对于气缸中 的生成,化学家提出了如下反应历程:
的生成,化学家提出了如下反应历程:
第一步 慢反应
慢反应
第二步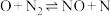 较快平衡
较快平衡
第三步 快速平衡
快速平衡
下列说法正确的是______(填标号)。
(1)已知:
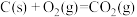


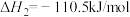
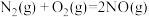

则汽车尾气的催化转化反应
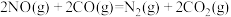 属于反应
属于反应(2)400℃时,在分别装有催化剂A和B的两个容积为2L的刚性密闭容器中,各充入物质的量均为
 的
的 和
和 发生上述反应。通过测定容器内总压强随时间变化来探究催化剂对反应速率的影响,数据如下表;
发生上述反应。通过测定容器内总压强随时间变化来探究催化剂对反应速率的影响,数据如下表;| 时间/min | 0 | 10 | 20 | 30 |
|
| A容器内压强/kPa | 100.0 | 90.0 | 85.0 | 80.0 | 80.0 |
| B容器内压强/kPa | 100.0 | 95.0 | 90.0 | 85.0 | 80.0 |
①由上表可以判断催化剂
②容器中
 的平衡转化率为
的平衡转化率为③汽车尾气排气管中使用催化剂可以提高污染物转化率,其原因是
(3)为研究气缸中
 的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为
的生成,在体积可变的恒压密闭容器中,高温下充入物质的量均为 的氮气和氧气,发生反应
的氮气和氧气,发生反应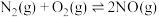 。
。①下列说法能表明该反应已经达到平衡状态的是
A.
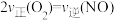 B.混合气体的平均相对分子质量不变
B.混合气体的平均相对分子质量不变C.
 D.容器内气体的密度不再发生变化
D.容器内气体的密度不再发生变化②为减小平衡混合气中NO体积分数,可采取的措施是
(4)对于气缸中
 的生成,化学家提出了如下反应历程:
的生成,化学家提出了如下反应历程:第一步
 慢反应
慢反应第二步
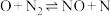 较快平衡
较快平衡第三步
 快速平衡
快速平衡下列说法正确的是______(填标号)。
| A.N、O原子均为该反应的催化剂 |
B.第一步反应不从 分解开始,是因为 分解开始,是因为 比 比 稳定 稳定 |
| C.三步反应中第一步反应活化能最小 |
| D.三步反应的速率都随温度升高而增大 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
I、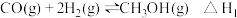
II、
(1)则 的
的
_____ (用 、
、 表示)
表示)
(2)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为______ 反应(填“吸热”或“放热”)。
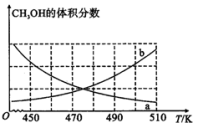
(3)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是___________ (填“a”或“b”)。
②下列说法能表明反应已达平衡状态的是___________ (填标号)。
A、容器中气体的压强不再变化
B、混合气体的密度不再变化
C、混合气体的平均相对分子质量不再变化
D、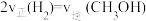
(4)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且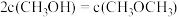 ,则:
,则:
①0~4min,反应I的v(H2)=___________ ,反应I的平衡常数K=___________ 。
②反应II中CH3OH的转化率α=___________ 。
I、
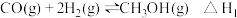
II、

(1)则
 的
的
 、
、 表示)
表示)(2)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为
(3)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是

②下列说法能表明反应已达平衡状态的是
A、容器中气体的压强不再变化
B、混合气体的密度不再变化
C、混合气体的平均相对分子质量不再变化
D、
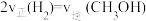
(4)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且
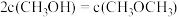 ,则:
,则:①0~4min,反应I的v(H2)=
②反应II中CH3OH的转化率α=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】捕集二氧化碳是实现温室气体减排的重要途径之一
(1)目前,NH3和(NH4)2CO3,可与CO2可发生如下可逆反应:
2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) K1
(NH4)2CO3(aq) K1
NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) K2
NH4HCO3(aq) K2
(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) K3
2NH4HCO3(aq) K3
则K3=_______ (用含K1、K2的代数式表示)。
(2)对于可逆反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH=a kJ·mol-1,起始时按n(CO2):n(H2)=1:3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图所示:
C2H4(g)+4H2O(g) ΔH=a kJ·mol-1,起始时按n(CO2):n(H2)=1:3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图所示:
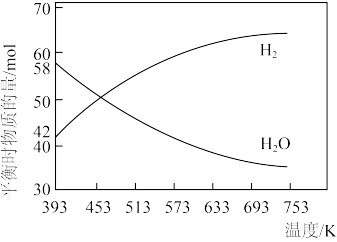
①a_______ 0(填“>”或“<”)。
②下列说法正确的是_______ (填序号)。
A.使用催化剂,可降低反应的活化能,加快反应速率
B.其他条件不变时,若扩大容器容积,则v正减小,v逆增大
C.测得容器内混合气体的密度不再随时间改变时,说明反应已达到平衡
③393 K时,H2的平衡转化率为_______ 。
④393 K时,该反应达到平衡后,再向容器中再向容器中按n(CO2):n(H2)=1:3的投料比投入CO2和H2,反应再次达到平衡时,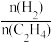 将
将_______ (填“变大”“不变”或“变小”)。
(3)相同温度下,根据三种酸的电离常数如下:
①请排列三种酸的强弱关系_______ ;
② 反应HZ+Y-=HY+Z-________ 填“能”或“不能)”发生;
③ 电离常数只与_______ 有关。
(1)目前,NH3和(NH4)2CO3,可与CO2可发生如下可逆反应:
2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) K1
(NH4)2CO3(aq) K1NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) K2
NH4HCO3(aq) K2(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) K3
2NH4HCO3(aq) K3则K3=
(2)对于可逆反应2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ΔH=a kJ·mol-1,起始时按n(CO2):n(H2)=1:3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图所示:
C2H4(g)+4H2O(g) ΔH=a kJ·mol-1,起始时按n(CO2):n(H2)=1:3的投料比充入20 L的恒容密闭容器中,不同温度下平衡时H2和H2O的物质的量如图所示:
①a
②下列说法正确的是
A.使用催化剂,可降低反应的活化能,加快反应速率
B.其他条件不变时,若扩大容器容积,则v正减小,v逆增大
C.测得容器内混合气体的密度不再随时间改变时,说明反应已达到平衡
③393 K时,H2的平衡转化率为
④393 K时,该反应达到平衡后,再向容器中再向容器中按n(CO2):n(H2)=1:3的投料比投入CO2和H2,反应再次达到平衡时,
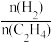 将
将(3)相同温度下,根据三种酸的电离常数如下:
| 酸 | HX | HY | HZ |
| 电离常数K | 9×10-7 | 9×10-6 | 10-2 |
①请排列三种酸的强弱关系
② 反应HZ+Y-=HY+Z-
③ 电离常数只与
您最近半年使用:0次




