CO2是主要的温室气体,以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上常用CO2和H2为原料合成甲醇( ),过程中发生如下两个反应:
),过程中发生如下两个反应:
反应I:
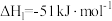
反应II:
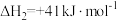
①则

_______  ;
;
②若反应II逆反应活化能Ea(逆)为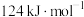 ,则该反应的Ea (正)活化能为
,则该反应的Ea (正)活化能为_______  。
。
(2)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应: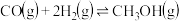 ,下列事实能说明此反应已达到平衡状态的是_______。
,下列事实能说明此反应已达到平衡状态的是_______。
(3)向2L容器中充入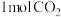 和
和 ,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中
,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图1所示,测得反应时逆反应速率与容器中
体积分数如图1所示,测得反应时逆反应速率与容器中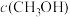 关系如图II所示:
关系如图II所示:
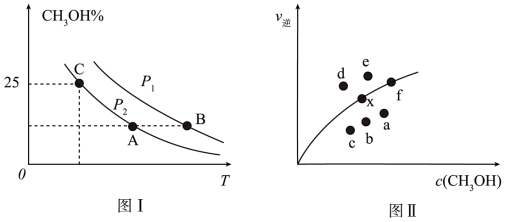
①图I中P1_______ P2(填“>”、“<”或“=”)。
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是_______ 。
③利用图I中C点对应的数据,计算求出对应温度下反应Ⅰ的平衡常数K=_______ 。
(1)工业上常用CO2和H2为原料合成甲醇(
 ),过程中发生如下两个反应:
),过程中发生如下两个反应:反应I:

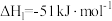
反应II:

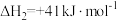
①则


 ;
;②若反应II逆反应活化能Ea(逆)为
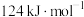 ,则该反应的Ea (正)活化能为
,则该反应的Ea (正)活化能为 。
。(2)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应:
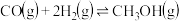 ,下列事实能说明此反应已达到平衡状态的是_______。
,下列事实能说明此反应已达到平衡状态的是_______。| A.容器内气体密度保持不变 |
| B.混合气体的平均相对分子质量不变 |
C.生成 的速率与生成H2的速率相等 的速率与生成H2的速率相等 |
| D.CO的体积分数保持不变 |
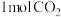 和
和 ,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中
,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中 体积分数如图1所示,测得反应时逆反应速率与容器中
体积分数如图1所示,测得反应时逆反应速率与容器中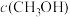 关系如图II所示:
关系如图II所示:
①图I中P1
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
③利用图I中C点对应的数据,计算求出对应温度下反应Ⅰ的平衡常数K=
更新时间:2022-07-02 20:31:45
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】习近平总书记十分重视生态环境保护,多次对生态文明建设作出重要指示。试回答下列与环境有关的问题:
(1)煤燃烧产生的烟气中含有氮的氧化物,用催化还原 可消除氮氧化物的污染。
可消除氮氧化物的污染。
已知:①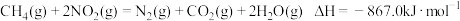
②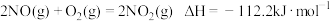
③适量的 和
和 完全反应,每生成
完全反应,每生成 (标准状况下)
(标准状况下) 时,吸收
时,吸收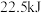 的热量。
的热量。
则

___________  ;反应①在高温下
;反应①在高温下___________ (填“能”或“不能”)自发进行。
(2)在汽车排气系统中安装三元催化转化器,可发生下列反应: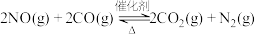 。在某恒容密闭容器中通入等物质的量的
。在某恒容密闭容器中通入等物质的量的 和
和 ,在不同温度
,在不同温度 下发生上述反应时,
下发生上述反应时,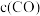 随时间
随时间 的变化曲线如图所示:
的变化曲线如图所示:
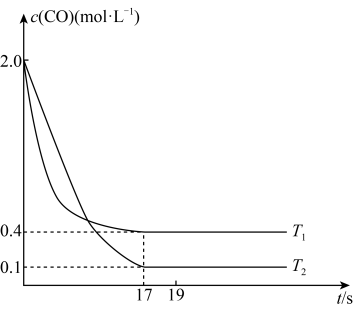
①该反应的正反为___________ (填“放热”或“吸热”)反应。
②温度为 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为___________ 。
③温度为 时,该反应的平衡常数
时,该反应的平衡常数
___________ 。
(1)煤燃烧产生的烟气中含有氮的氧化物,用催化还原
 可消除氮氧化物的污染。
可消除氮氧化物的污染。已知:①
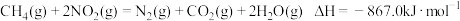
②
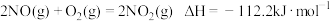
③适量的
 和
和 完全反应,每生成
完全反应,每生成 (标准状况下)
(标准状况下) 时,吸收
时,吸收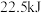 的热量。
的热量。则


 ;反应①在高温下
;反应①在高温下(2)在汽车排气系统中安装三元催化转化器,可发生下列反应:
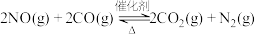 。在某恒容密闭容器中通入等物质的量的
。在某恒容密闭容器中通入等物质的量的 和
和 ,在不同温度
,在不同温度 下发生上述反应时,
下发生上述反应时,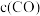 随时间
随时间 的变化曲线如图所示:
的变化曲线如图所示:
①该反应的正反为
②温度为
 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为③温度为
 时,该反应的平衡常数
时,该反应的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.在0.1 mol·L-1的重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O72-+H2O 2HCrO4
2HCrO4 2CrO42-+2H+
2CrO42-+2H+
(1)重铬酸钾溶液呈______ 性,在强碱溶液中,铬元素的主要存在形式为________ (填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中c(Cr2O72-)/c(CrO42-)将______ (填“增大”、“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)若溶液中只溶解了一种溶质,则该溶质是________ ,上述四种离子浓度的大小顺序为________ (选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________ ;
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______ c(NH3·H2O) (填“大于”“小于”或“等于”)。
III.重金属离子对河流海洋造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含有Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1。排放前拟用沉淀法除去这两种
离子,查找有关数据如下:
(1)你认为往废水中投入________________ (填字母序号),沉淀效果最好。
A. NaOH B.Na2S C.KI D. Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=_______ 。
Cr2O72-+H2O
 2HCrO4
2HCrO4 2CrO42-+2H+
2CrO42-+2H+(1)重铬酸钾溶液呈
Ⅱ.已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:并按要求填写下列空白:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若上述关系中③是正确的,则溶液中的溶质为
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
III.重金属离子对河流海洋造成严重污染。某化工厂废水(pH=2.0,d≈1 g·mL-1)中含有Ag+,Pb 2+等重金属离子,其浓度各约为0.0lmol·L-1。排放前拟用沉淀法除去这两种
离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
(1)你认为往废水中投入
A. NaOH B.Na2S C.KI D. Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品。
(1)CO与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g) COCl2(g)ΔH=a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g)ΔH=a kJ/mol反应过程中测定的部分数据如下表:

①反应0~2min末的平均速率v(COCl2)=__________ mol/(L·min)。
②在2min~4min间,v正(Cl2)______ v逆(Cl2)(填“>”、“=”或“<”),该温度下K=______ 。
③已知X、L可分别代表温度或压强,下图表示L一定时,CO的转化率随X的变化关系。
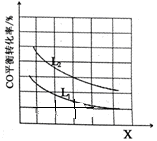
X代表的物理量是__________ ;a_________ 0(填“>”,“=”,“<”)。
(2)在催化剂作用下NO和CO转化为无毒气体:2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是____________________ 。
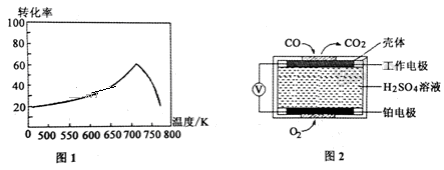
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为______________________ ;方法2:氧化还原滴定法。用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度。写出NO与H2O2溶液反应的离子方程式_______________ 。
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g) CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是
CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是_______________ 。
(1)CO与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)
 COCl2(g)ΔH=a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g)ΔH=a kJ/mol反应过程中测定的部分数据如下表:
①反应0~2min末的平均速率v(COCl2)=
②在2min~4min间,v正(Cl2)
③已知X、L可分别代表温度或压强,下图表示L一定时,CO的转化率随X的变化关系。

X代表的物理量是
(2)在催化剂作用下NO和CO转化为无毒气体:2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH=-748 kJ·mol-1
2CO2(g)+N2(g) ΔH=-748 kJ·mol-1①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是

②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法。其中CO传感器的工作原理如图2所示,则工作电极的反应式为
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g)
 CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是
CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中KOH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】二氧化锰和高锰酸钾是重要的化学用品
文献资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
Ⅰ.用软锰矿吸收含SO2的废气,制备高纯度的硫酸锰晶体
已知:①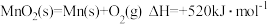
②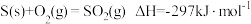
③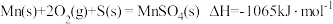
(1)固体MnO2和SO2(g)反应生成MnSO4固体的热化学方程式为___________ 。
Ⅱ.工业上常用软锰矿(主要成分MnO2)为原料制备高锰酸钾。其方法为:将软锰矿(主要成分MnO2)充分粉碎后与KOH固体混合,通入空气充分焙烧,生成暗绿色熔融态物质。冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液(主要成分为K2MnO4)。再将K2MnO4溶液采用惰性电极隔膜法电解,制得KMnO4。
(2)软锰矿与KOH固体混合焙烧前充分粉碎的原因是___________ 。
(3)焙烧时发生反应的化学方程式为___________ 。
(4)固体研细后用稀KOH溶液浸取的原因是___________ 。
(5)用惰性电极隔膜法电解K2MnO4溶液的装置为如下:
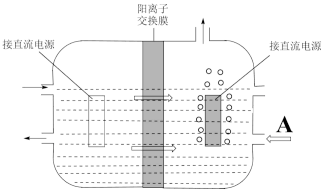
①a极的电极反应为___________ 。
②研究发现,用无膜法电解时,锰元素利用较低,其原因是___________ 。
Ⅲ.测定KMnO4产品的纯度
(6)测定KMnO4产品的纯度可用标准Na2SO3溶液滴定。
①取某KMnO4产品0.5000g溶于水,并加入___________ (填字母)进行酸化。
A.稀盐酸 B.稀硫酸 C.硝酸 D.次氯酸
②所得溶液用0.2000 mol/L标准Na2SO3溶液进行滴定,滴定至终点记录实验消耗Na2SO3溶液的体积。
重复步骤①②,三次平行实验数据如表:
(有关离子方程式为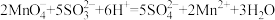 )
)
计算该KMnO4 (式量为:158)产品的纯度为___________ (结果保留三位有效数字)。
文献资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
Ⅰ.用软锰矿吸收含SO2的废气,制备高纯度的硫酸锰晶体
已知:①
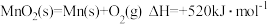
②
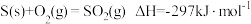
③
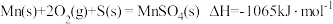
(1)固体MnO2和SO2(g)反应生成MnSO4固体的热化学方程式为
Ⅱ.工业上常用软锰矿(主要成分MnO2)为原料制备高锰酸钾。其方法为:将软锰矿(主要成分MnO2)充分粉碎后与KOH固体混合,通入空气充分焙烧,生成暗绿色熔融态物质。冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液(主要成分为K2MnO4)。再将K2MnO4溶液采用惰性电极隔膜法电解,制得KMnO4。
(2)软锰矿与KOH固体混合焙烧前充分粉碎的原因是
(3)焙烧时发生反应的化学方程式为
(4)固体研细后用稀KOH溶液浸取的原因是
(5)用惰性电极隔膜法电解K2MnO4溶液的装置为如下:

①a极的电极反应为
②研究发现,用无膜法电解时,锰元素利用较低,其原因是
Ⅲ.测定KMnO4产品的纯度
(6)测定KMnO4产品的纯度可用标准Na2SO3溶液滴定。
①取某KMnO4产品0.5000g溶于水,并加入
A.稀盐酸 B.稀硫酸 C.硝酸 D.次氯酸
②所得溶液用0.2000 mol/L标准Na2SO3溶液进行滴定,滴定至终点记录实验消耗Na2SO3溶液的体积。
重复步骤①②,三次平行实验数据如表:
| 实验次数 | 1 | 2 | 3 |
消耗 溶液体积/mL 溶液体积/mL | 19.30 | 20.98 | 21.02 |
(有关离子方程式为
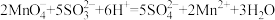 )
)计算该KMnO4 (式量为:158)产品的纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】尿素[CO(NH2)2][]是首个由无机物人工合成的有机物。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)⇌NH2COONH4(l) △H1=-119.2 ;NH2COONH4(l)⇌CO(NH2)2(s)+H2O(g) △H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) △H3=
;NH2COONH4(l)⇌CO(NH2)2(s)+H2O(g) △H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) △H3=___________  ,下列图象能表示尿素合成塔中发生反应的能量变化历程的是
,下列图象能表示尿素合成塔中发生反应的能量变化历程的是___________ (填标号)。
A.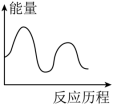 B.
B.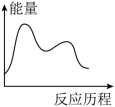 C.
C.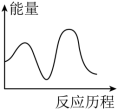 D.
D.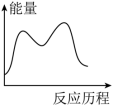
(2)T℃,在2L的密闭容器中,通入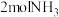 和
和 ,保持体积不变,发生反应,2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
,保持体积不变,发生反应,2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
① 的平衡转化率为
的平衡转化率为___________ 。
②能说明上述反应达到平衡状态的是___________ (填标号)。
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C. 的体积分数在混合气体中保持不变
的体积分数在混合气体中保持不变
D.单位时间内消耗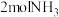 ,同时生成
,同时生成
③若10min时保持温度和容器的容积不变,再向容器中同时充入1molNH3(g)、0.5molCO2(g)和0.5molH2O(g),则此时平衡___________ (填“正向移动”、“逆向移动”或“不移动”)。
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),若原料气中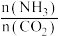 =m,测得m与
=m,测得m与 的平衡转化率(α)的关系如图所示:
的平衡转化率(α)的关系如图所示:
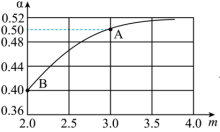
①若平衡时A点容器内总压强为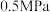 ,则上述反应的平衡常数
,则上述反应的平衡常数
___________  。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②若平衡时A、B对应容器的压强相等,则A、B对应的容器中,起始时投入氨气的物质的量之比nA(NH3):nB(NH3)=___________ 。
(4)合成氨催化剂前驱体(主要成分为 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数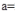 287nm,密度为
287nm,密度为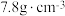 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为___________ (列出计算式,阿伏加德罗常数的值为 )。
)。
(1)在尿素合成塔中发生的反应可表示为2NH3(g)+CO2(g)⇌NH2COONH4(l) △H1=-119.2
 ;NH2COONH4(l)⇌CO(NH2)2(s)+H2O(g) △H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) △H3=
;NH2COONH4(l)⇌CO(NH2)2(s)+H2O(g) △H2=+15.5kJ∙mol-1,已知第一步反应为快速反应,第二步反应为慢速反应,则2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) △H3= ,下列图象能表示尿素合成塔中发生反应的能量变化历程的是
,下列图象能表示尿素合成塔中发生反应的能量变化历程的是A.
 B.
B. C.
C. D.
D.
(2)T℃,在2L的密闭容器中,通入
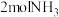 和
和 ,保持体积不变,发生反应,2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:
,保持体积不变,发生反应,2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),10min时反应刚好达到平衡。测得起始压强为平衡时压强的1.5倍,则:①
 的平衡转化率为
的平衡转化率为②能说明上述反应达到平衡状态的是
A.n(CO2):n(NH3)=1:2
B.混合气体的密度不再发生变化
C.
 的体积分数在混合气体中保持不变
的体积分数在混合气体中保持不变D.单位时间内消耗
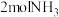 ,同时生成
,同时生成
③若10min时保持温度和容器的容积不变,再向容器中同时充入1molNH3(g)、0.5molCO2(g)和0.5molH2O(g),则此时平衡
(3)一定温度下,某恒容密闭容器中发生反应2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),若原料气中
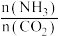 =m,测得m与
=m,测得m与 的平衡转化率(α)的关系如图所示:
的平衡转化率(α)的关系如图所示:
①若平衡时A点容器内总压强为
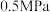 ,则上述反应的平衡常数
,则上述反应的平衡常数
 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)②若平衡时A、B对应容器的压强相等,则A、B对应的容器中,起始时投入氨气的物质的量之比nA(NH3):nB(NH3)=
(4)合成氨催化剂前驱体(主要成分为
 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数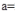 287nm,密度为
287nm,密度为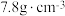 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】利用太阳能分解H2O获得氢气,再通过CO2加氢制甲醇(CH3OH)等燃料,从而实现可再生能源和 CO2的资源化利用。
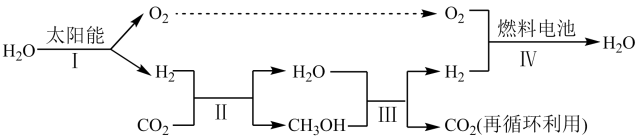
(1)过程Ⅰ的能量转化形式为,由___________ 能转化为___________ 能。
(2)活化CO2需从外界输入电子,CO2中易于获得电子的原子是___________ 。
(3)过程Ⅱ中CO2催化加氢制取甲醇,反应如下:
主反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H1=-49.0kJ·mol-1
CH3OH(g)+H2O(g) ∆H1=-49.0kJ·mol-1
副反应:CO2(g)+H2(g) CO(g)+H2O(g) ∆H2 = + 41.2 kJ·mol-1
CO(g)+H2O(g) ∆H2 = + 41.2 kJ·mol-1
①CO、H2生成CH3OH的热化学方程式是___________ 。
②提高CH3OH在平衡体系中的含量,可采取如下措施:___________ (写出两条即可)。
(4)过程Ⅲ中制得的H2中混有CO,去除CO的反应如下: CO(g)+H2O(g) CO2(g)+H2(g)。在容积不变的密闭容器中,将0.1 mol CO、0.1 mol H2O混合加热到830℃,平衡时 CO的转化率为50%,反应的平衡常数K=
CO2(g)+H2(g)。在容积不变的密闭容器中,将0.1 mol CO、0.1 mol H2O混合加热到830℃,平衡时 CO的转化率为50%,反应的平衡常数K=___________ 。

(1)过程Ⅰ的能量转化形式为,由
(2)活化CO2需从外界输入电子,CO2中易于获得电子的原子是
(3)过程Ⅱ中CO2催化加氢制取甲醇,反应如下:
主反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H1=-49.0kJ·mol-1
CH3OH(g)+H2O(g) ∆H1=-49.0kJ·mol-1副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2 = + 41.2 kJ·mol-1
CO(g)+H2O(g) ∆H2 = + 41.2 kJ·mol-1①CO、H2生成CH3OH的热化学方程式是
②提高CH3OH在平衡体系中的含量,可采取如下措施:
(4)过程Ⅲ中制得的H2中混有CO,去除CO的反应如下: CO(g)+H2O(g)
 CO2(g)+H2(g)。在容积不变的密闭容器中,将0.1 mol CO、0.1 mol H2O混合加热到830℃,平衡时 CO的转化率为50%,反应的平衡常数K=
CO2(g)+H2(g)。在容积不变的密闭容器中,将0.1 mol CO、0.1 mol H2O混合加热到830℃,平衡时 CO的转化率为50%,反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义。
(1)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0
N2(g)+2CO2(g) △H<0
①一定条件下,将体积比为1:2的NO、CO气体置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_________ (填字母)。
A.体系压强保持不变 B.混合气体颜色保持不变
C. N2和CO2的体积比保持不变 D. v正(CO)=2v逆(N2)
②20min时,若改变反应条件,导致N2浓度发生如下图1所示的变化,则改变的条件可能是_____ (填字母)。
A.加入催化剂 B.降低温度 C.增加CO2量 D.缩小容器体积
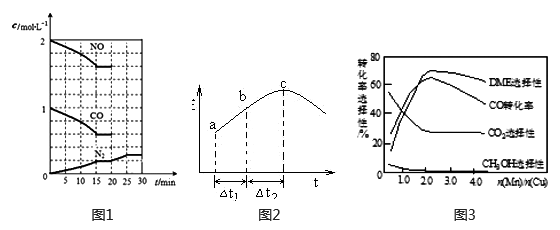
(2)在一定条件下,将SO2和NO2通入绝热恒容密闭容器中,发生反应:SO2(g)+NO2(g) SO3(g)+NO(g),正反应速率随时间变化如图2所示。由图可得出的正确结论是
SO3(g)+NO(g),正反应速率随时间变化如图2所示。由图可得出的正确结论是_____________ (填字母)。
A.反应在c点达到平衡状态
B.反应物浓度:b点小于c点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2 时,SO2的转化率:a~b段小于b~c段
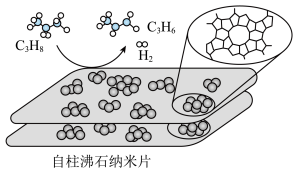
(3)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2可制备二甲醚(DME)。观察图3回答问题。催化剂中n(Mn)/n(Cu)约为__________ 时最有利于二甲醚的合成。
(4)工业上可以用CO和H2生产燃料甲醇:CO(g)+2H2(g) CH3OH(g) △H=-92.9kJ/mol, 300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
CH3OH(g) △H=-92.9kJ/mol, 300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
下列说法中正确的是______
A.2c1>c3 B. a+b=92.9 C.2p23 D.a1+a3<1
(1)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0
N2(g)+2CO2(g) △H<0①一定条件下,将体积比为1:2的NO、CO气体置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变 B.混合气体颜色保持不变
C. N2和CO2的体积比保持不变 D. v正(CO)=2v逆(N2)
②20min时,若改变反应条件,导致N2浓度发生如下图1所示的变化,则改变的条件可能是
A.加入催化剂 B.降低温度 C.增加CO2量 D.缩小容器体积

(2)在一定条件下,将SO2和NO2通入绝热恒容密闭容器中,发生反应:SO2(g)+NO2(g)
 SO3(g)+NO(g),正反应速率随时间变化如图2所示。由图可得出的正确结论是
SO3(g)+NO(g),正反应速率随时间变化如图2所示。由图可得出的正确结论是A.反应在c点达到平衡状态
B.反应物浓度:b点小于c点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2 时,SO2的转化率:a~b段小于b~c段
(3)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2可制备二甲醚(DME)。观察图3回答问题。催化剂中n(Mn)/n(Cu)约为
(4)工业上可以用CO和H2生产燃料甲醇:CO(g)+2H2(g)
 CH3OH(g) △H=-92.9kJ/mol, 300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
CH3OH(g) △H=-92.9kJ/mol, 300℃,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 | lmolCH3OH | 2molCH3OH | |
| 平衡 时的 数据 | CH3OH/mol·L-1 | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ | |
| 体系压强/Pa | p1 | p2 | p3 | |
| 反应物转化率 | a1 | a2 | a3 | |
下列说法中正确的是
A.2c1>c3 B. a+b=92.9 C.2p23 D.a1+a3<1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】丙烯是合成聚丙烯的原料。近日,科学家开发自柱沸石纳米片上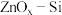 稳定的高分散Pt用于高效催化丙烷脱氢制备丙烯。
稳定的高分散Pt用于高效催化丙烷脱氢制备丙烯。
(1)Zn是位于第四周期的元素,基态Zn原子核外电子占据能量最高的能级符号是_______ 。
(2)丙烷脱氢制备丙烯的反应为 。已知几种共价键的键能数据如下:
。已知几种共价键的键能数据如下:
丙烷、丙烯、氢气的燃烧热(△H)依次为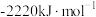 、
、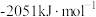 、
、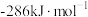 。丙烯中π键键能为
。丙烯中π键键能为_______  。
。
(3)在恒温恒容密闭容器中充入1mol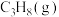 和3molAr(不参与反应),发生上述反应,下列叙述正确的是_______(填标号)。
和3molAr(不参与反应),发生上述反应,下列叙述正确的是_______(填标号)。
(4)丙烷脱氢反应中,丙烷的平衡转化率与温度、压强的关系如图1所示。
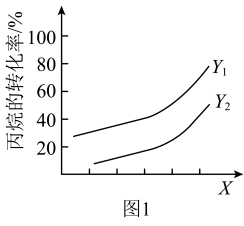
①X代表_______ (填“温度”或“压强”),判断依据是_______ 。
②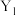
_______  (填“>”或“<”)。
(填“>”或“<”)。
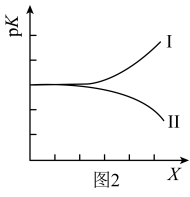
(5)丙烷脱氢反应的平衡常数为K, ,pK与X的关系如图2所示。符合题意的曲线是
,pK与X的关系如图2所示。符合题意的曲线是_______ (填“Ⅰ”或“Ⅱ”)。
(6)在t℃、压强恒定为58kPa下,向密闭容器中充入 和Ar在催化剂作用下,发生脱氢反应和副反应:
和Ar在催化剂作用下,发生脱氢反应和副反应: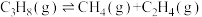 。丙烷的平衡转化率与投料比
。丙烷的平衡转化率与投料比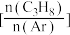 的关系如图所示。
的关系如图所示。
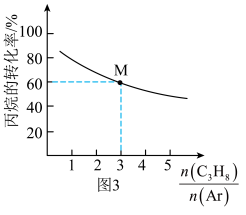
①随着 增大,丙烷的转化率降低的原因是
增大,丙烷的转化率降低的原因是_______ 。
②已知M点中丙烯的选择性为66.67%,该温度下,丙烷脱氢反应的压强平衡常数( )为
)为_______ (要求带单位)。[注明:用分压计算的平衡常数叫压强平衡常数( ),分压=总压×物质的量分数。]
),分压=总压×物质的量分数。]
 稳定的高分散Pt用于高效催化丙烷脱氢制备丙烯。
稳定的高分散Pt用于高效催化丙烷脱氢制备丙烯。
(1)Zn是位于第四周期的元素,基态Zn原子核外电子占据能量最高的能级符号是
(2)丙烷脱氢制备丙烯的反应为
 。已知几种共价键的键能数据如下:
。已知几种共价键的键能数据如下:| 化学键 | H—H | C—H | C=C | C—C |
键能(E)/( ) ) | 436 | 413 | a | b |
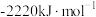 、
、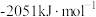 、
、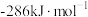 。丙烯中π键键能为
。丙烯中π键键能为 。
。(3)在恒温恒容密闭容器中充入1mol
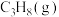 和3molAr(不参与反应),发生上述反应,下列叙述正确的是_______(填标号)。
和3molAr(不参与反应),发生上述反应,下列叙述正确的是_______(填标号)。| A.气体平均摩尔质量不变时达到平衡状态 |
B.平衡时 体积分数小于20% 体积分数小于20% |
| C.加入催化剂能提高丙烯的平衡产率 |
D.平衡后,充入少量 ,丙烷平衡转化率增大 ,丙烷平衡转化率增大 |

①X代表
②
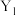
 (填“>”或“<”)。
(填“>”或“<”)。(5)丙烷脱氢反应的平衡常数为K,
 ,pK与X的关系如图2所示。符合题意的曲线是
,pK与X的关系如图2所示。符合题意的曲线是
(6)在t℃、压强恒定为58kPa下,向密闭容器中充入
 和Ar在催化剂作用下,发生脱氢反应和副反应:
和Ar在催化剂作用下,发生脱氢反应和副反应: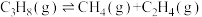 。丙烷的平衡转化率与投料比
。丙烷的平衡转化率与投料比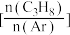 的关系如图所示。
的关系如图所示。
①随着
 增大,丙烷的转化率降低的原因是
增大,丙烷的转化率降低的原因是②已知M点中丙烯的选择性为66.67%,该温度下,丙烷脱氢反应的压强平衡常数(
 )为
)为 ),分压=总压×物质的量分数。]
),分压=总压×物质的量分数。]
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】合成气(主要成分为CO、H2及少量CO、H2O)在工业上有广泛用途。合成甲醇的主要反应为:CO(g)+2H2(g) CH3OH(g) ΔH<0。将CO与H2混合气体充入密闭容器中,投料比
CH3OH(g) ΔH<0。将CO与H2混合气体充入密闭容器中,投料比 =
= ,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OHK)]与温度(T)、压强(p)之间的关系如图所示。
,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OHK)]与温度(T)、压强(p)之间的关系如图所示。
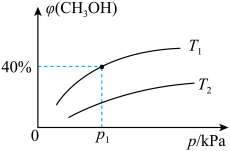
(1)T1、p1时,CO的转化率为_______ (保留3位有效数字)﹔压强平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用含p1的代数式表示)。在该条件下,若CO、H2、CH3OH气体的起始物质的量之比为2∶1∶2,则反应开始时v(CO)正______ v(CO)逆。
(2)恒温恒容条件下,下列叙述不能说明反应达到化学平衡状态的是_______ 。
 CH3OH(g) ΔH<0。将CO与H2混合气体充入密闭容器中,投料比
CH3OH(g) ΔH<0。将CO与H2混合气体充入密闭容器中,投料比 =
= ,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OHK)]与温度(T)、压强(p)之间的关系如图所示。
,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OHK)]与温度(T)、压强(p)之间的关系如图所示。
(1)T1、p1时,CO的转化率为
(2)恒温恒容条件下,下列叙述不能说明反应达到化学平衡状态的是
| A.CO、H2的物质的量浓度不再随时间的变化而变化 |
| B.混合气体的平均摩尔质量不再随时间的变化而变化 |
| C.混合气体的密度不再随时间的变化而变化 |
| D.若将容器改为绝热恒容容器时,平衡常数K不随时间变化而变化 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
真题
名校
【推荐1】在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应应:
A(g) B(g)+C(g) △H=+85.1kJ·mol-1
B(g)+C(g) △H=+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为_____________ 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为___________________ 。
平衡时A的转化率为_________ ,列式并计算反应的平衡常数K __________________ 。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________ mol,n(A)= ______ mol。
②下表为反应物A浓度与反应时间的数据,计算a=_________
分析该反应中反应反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是______ ,
由此规律推出反应在12h时反应物的浓度c(A)为_______ mol·L-1。
A(g)
 B(g)+C(g) △H=+85.1kJ·mol-1
B(g)+C(g) △H=+85.1kJ·mol-1反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为
平衡时A的转化率为
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=
②下表为反应物A浓度与反应时间的数据,计算a=
| 反应时间t/h | 0 | 4 | 8 | 16 |
| C(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.0065 |
分析该反应中反应反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是
由此规律推出反应在12h时反应物的浓度c(A)为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.已知在448℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为____________ ;反应1/2H2(g)+ I2(g)
I2(g) HI(g)的平衡常数K3为
HI(g)的平衡常数K3为____________ 。
II.在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的逆反应为____________ (填“吸热”或“放热”)反应。
(2)能判断该反应达到化学平衡状态的依据是____________ 。
A.混合气体中c(CO)不变
B.c(CO2)=c(CO)
C.v正(H2)=v逆(H2O)
D.容器中压强不变
(3)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为____________ ℃,在此温度下,加入2mol的CO和3mol的H2,达到平衡时,CO的转化率为____________ 。
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol•L-1,c(H2)为1.5mol•L-1,c(CO)为1mol•L-1,c(H2O)为3mol•L-1,则下一时刻,反应将____________ (填“正向”或“逆向”)进行。
 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为 I2(g)
I2(g) HI(g)的平衡常数K3为
HI(g)的平衡常数K3为II.在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的逆反应为
(2)能判断该反应达到化学平衡状态的依据是
A.混合气体中c(CO)不变
B.c(CO2)=c(CO)
C.v正(H2)=v逆(H2O)
D.容器中压强不变
(3)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol•L-1,c(H2)为1.5mol•L-1,c(CO)为1mol•L-1,c(H2O)为3mol•L-1,则下一时刻,反应将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】向某密闭容器中加入0.6molA、0.2molC和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示(其中t0-t1阶段c(B)未画出)。乙图为反应体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件(催化剂、温度、浓度、压强,每次改变条件均不同),已知t3~t4阶段为使用催化剂。

(1)若t1=5s,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L•s)。
(2)若t2~t3阶段,C的体积分数变小,此阶段v(正)___v(逆)(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为_______,B的起始物质的量为_______。
(4)t5~t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式:__________________________________。
(5)该反应的化学平衡常数K可表示为_______________。[用含c(A) 、c(B) 、c(C)的式子表示]
并在下图中补画出t1~t6各阶段K的变化趋势图像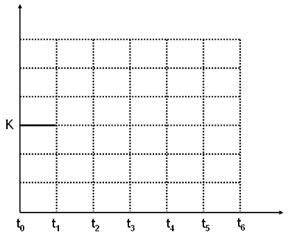

(1)若t1=5s,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L•s)。
(2)若t2~t3阶段,C的体积分数变小,此阶段v(正)___v(逆)(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为_______,B的起始物质的量为_______。
(4)t5~t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式:__________________________________。
(5)该反应的化学平衡常数K可表示为_______________。[用含c(A) 、c(B) 、c(C)的式子表示]
并在下图中补画出t1~t6各阶段K的变化趋势图像

您最近一年使用:0次



