在绝热恒容的密闭容器中,进行反应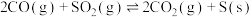
 ,对此反应下列说法正确的是
,对此反应下列说法正确的是
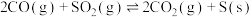
 ,对此反应下列说法正确的是
,对此反应下列说法正确的是| A.分离出S,正、逆反应速率均减小 |
| B.若混合气体的密度保持不变,则已达平衡 |
C.达平衡后,再充入一定量的 ,平衡常数保持不变 ,平衡常数保持不变 |
| D.从反应开始至平衡,容器内气体的压强保持不变 |
21-22高二上·福建龙岩·阶段练习 查看更多[7]
福建省武平县第一中学2021-2022学年高二上学期10月月考化学试题天津市第一中学2021-2022学年高一下学期期末质量调查化学试题山西省晋中市平遥县第二中学校2022-2023学年高二上学期8月质检化学试题河南省周口市周口恒大中学2023-2024学年高二上学期1月期末化学试题陕西省西安市西安区县联考2023-2024学年高二上学期1月期末化学试题陕西省西安市蓝田县乡镇学校联考2023-2024学年高二上学期1月期末化学试题(已下线)重难点04 化学反应速率及平衡图表问题的分析 平衡状态的判断-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
更新时间:2022-07-20 10:47:40
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业合成氨是人类科学技术的一项重大突破。其合成原理为: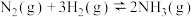
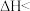
 ,下列说法错误的是
,下列说法错误的是
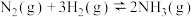
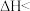
 ,下列说法错误的是
,下列说法错误的是| A.增大压强,单位体积内活化分子增多,反应速率加快 |
| B.该反应在低温下能自发进行 |
| C.为了防止混有的杂质使催化剂“中毒”,原料气必须经过净化 |
| D.用勒夏特列原理解释通常采用500℃有利于氨的合成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作和现象与结论均正确的是
选项 | 实验操作和现象 | 结论 |
A | 取两支试管,分别加入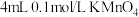 酸性溶液,然后向第一支试管加入 酸性溶液,然后向第一支试管加入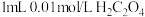 溶液,向第二支试管加入 溶液,向第二支试管加入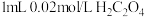 溶液,第二支试管先褪色 溶液,第二支试管先褪色 | 证明草酸浓度越大,反应速率越快 |
B | 向 溶液中加入 溶液中加入 溶液,充分反应后,滴入KSCN溶液,溶液变红 溶液,充分反应后,滴入KSCN溶液,溶液变红 |  与 与 发生的反应为可逆反应 发生的反应为可逆反应 |
C | 用pH计分别测定饱和 溶液和饱和 溶液和饱和 溶液的pH,前者的pH较小 溶液的pH,前者的pH较小 | 酸性: |
D | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,有白色沉淀生成,溶液红色变浅 固体,有白色沉淀生成,溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,向圆底烧瓶中加入1molC2H5OH和含1molHBr的氢溴酸,溶液中发生反应:C2H5OH+HBr C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃,下列有关叙述错误的是
C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃,下列有关叙述错误的是
 C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃,下列有关叙述错误的是
C2H5Br+H2O,充分反应后达到平衡。已知常压下,C2H5Br和C2H5OH的沸点分别为38.4℃和78.5℃,下列有关叙述错误的是| A.增大C2H5OH浓度,有利于生成C2H5Br |
| B.若反应物均增大至3mol,则两种反应物平衡转化率之比不变 |
| C.为缩短反应达到平衡的时间,将起始温度提高至50℃ |
| D.加入NaOH,可增大乙醇的物质的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某种葍二价铜微粒 的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
 的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是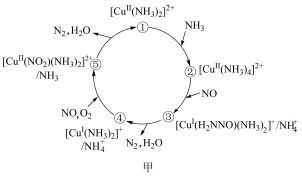

A.微粒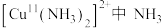 的键角小于氨气中 的键角小于氨气中 分子的键角 分子的键角 |
B.该催化过程的总反应方程式为  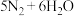 |
C. 可加快脱硝速率,提高脱硝的平衡转化率 可加快脱硝速率,提高脱硝的平衡转化率 |
| D.升高温度,脱硝反应的正反应速率的增大程度小于逆反应速率的增大程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验“操作和现象”与对应“结论”不正确 的是
| 选项 | 操作和现象 | 结论 |
| A | 用pH计测定同温度同浓度NaF溶液和CH3COONa溶液:pH(NaF)<pH(CH3COONa) | 酸性:HF>CH3COOH |
| B | 在相同条件下,向两份4mL0.01mol·L-1酸性KMnO4溶液中分别滴加2mL0.1mol·L-1和0.2mol·L-1草酸溶液,滴加0.2mol·L-1草酸溶液的先褪色 | 反应物浓度越大,反应速率越大 |
| C | 将两个相同的NO2球分别放入热水和冰水里,热水中的NO2球红棕色加深,冰水中的变浅 | 升温平衡向着吸热方向移动;降温平衡向着放热方向移动 |
| D | 将NaI溶液加入AgCl悬浊液中,产生黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】利用低温技术可处理废气中的氮氧化物。在恒容密闭容器中发生下列化学反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
 5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是
5N2(g)+6H2O(l) ΔH=Q kJ/mol(Q<0)。下列有关说法正确的是| A.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
| B.平衡时,其他条件不变,增加NH3的浓度,废气中NO的转化率减小 |
| C.单位时间内生成NH3和H2O的物质的量之比为2∶3时,反应达到平衡 |
| D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将一定量的氨基甲酸铵置于恒温恒容容器中,发生反应: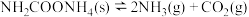 。下列说法不正确的是
。下列说法不正确的是
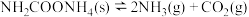 。下列说法不正确的是
。下列说法不正确的是A.该反应的 |
B.平衡时通入少量 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
| C.氨气的体积分数不变,则说明反应已经达到平衡状态 |
| D.容器中总压强不变,则说明反应已经达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
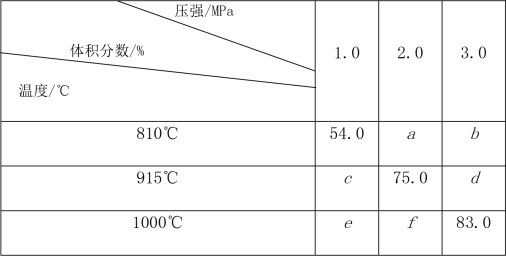
【推荐3】钼及其合金在冶金、电器等方面有广泛应用。在1L恒容密闭容器中充入足量的Na2CO3、MoS2和H2,发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)⇌Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H,测得在不同温度下H2的物质的量与时间关系数据如表所示:下列说法错误的是( )
| min mol K | 0 | 10 | 20 | 30 | 40 |
| T1 | 2 | 1.6 | 1.3 | 1.0 | 1.0 |
| T2 | 2 | 1.2 | 1.0 | n | 0.6 |
| A.T2>T1,△H<0 |
| B.表格中n=0.6 |
| C.T2K下20min时,v正>v逆 |
| D.T1K下平衡常数K=0.25(mol•L-1)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在反应2NO(g)+2H2(g) N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k∙cm(NO)∙cn(H2)(k、m、n 待测),其反应包含两步:
N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k∙cm(NO)∙cn(H2)(k、m、n 待测),其反应包含两步:
①2NO+H2=N2+H2O2(慢);②H2O2+H2=2H2O(快),T ℃时测得有关实验数据如下表:
下列说法中不正确的是
 N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k∙cm(NO)∙cn(H2)(k、m、n 待测),其反应包含两步:
N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k∙cm(NO)∙cn(H2)(k、m、n 待测),其反应包含两步:①2NO+H2=N2+H2O2(慢);②H2O2+H2=2H2O(快),T ℃时测得有关实验数据如下表:
实验数据 | 初始浓度 | 生成N2的初始速率/mol∙L-1∙s-1 | |
c(NO)/mol∙L-1 | c(H2)/mol∙L-1 | ||
1 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
2 | 1.00×10-3 | 6.00×10-3 | 4.80×10-4 |
3 | 2.00×10-3 | 3.00×10-3 | 9.60×10-4 |
下列说法中不正确的是
| A.关系式中m=1,n=2 |
| B.整个反应的反应速率由第①步反应决定 |
| C.当其他条件不变时,升高温度,速率常数将增大 |
D.该反应的热化学方程式为2NO(g)+2H2(g) N2(g)+2H2O(g) ΔH=-664 kJ∙mol-1 N2(g)+2H2O(g) ΔH=-664 kJ∙mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应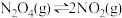
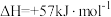 ,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
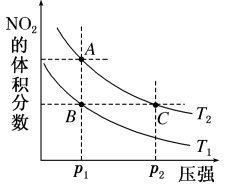
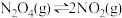
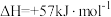 ,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
A.A、C两点的化学平衡常数: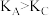 |
| B.A、C两点气体的颜色:A深,C浅 |
| C.由状态B到状态A,可以用加热的方法 |
| D.A、C两点气体的平均相对分子质量:A>C |
您最近一年使用:0次

 。下列分析
。下列分析 键能大,断开该化学键需要较多能量
键能大,断开该化学键需要较多能量 和
和 的共价键所需能量小于断裂
的共价键所需能量小于断裂 的共价键所需能量
的共价键所需能量