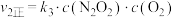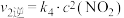已知在一容积恒定的密闭容器中发生反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,该反应达到平衡后,测得相关数据如下:
CO2(g)+H2(g) ΔH<0,该反应达到平衡后,测得相关数据如下:
(1)实验1中,10h后达到平衡,H2的平均反应速率为_______ mol·L-1h-1,该反应的平衡常数为_______ ,在此平衡体系中再加入0.5mol CO(g)和0.5mol H2(g),平衡_______ 移动(填“正向”、“逆向”或“不”)。
(2)实验2中X的值_______(填序号)。
(3)实验3中Y的值为_______ 。
 CO2(g)+H2(g) ΔH<0,该反应达到平衡后,测得相关数据如下:
CO2(g)+H2(g) ΔH<0,该反应达到平衡后,测得相关数据如下:| 实验序号 | 温度/℃ | 初始CO浓度/(mol·L-1) | 初始H2O浓度/(mol·L-1) | CO的平衡转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | X |
| 3 | 110 | 0.8 | Y | 60% |
(1)实验1中,10h后达到平衡,H2的平均反应速率为
(2)实验2中X的值_______(填序号)。
| A.等于50% | B.大于50% | C.小于50% | D.无法确定 |
更新时间:2022-09-13 10:49:07
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】已知断开1molAB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A-B的键能。如表列出了一些化学键的键能(E):
(1)反应H2(g)+ O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=______ 。
(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
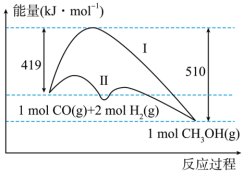
①计算当反应生成1.5molCH3OH(g)时,能量变化值是______ kJ。
②推测反应CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是______ (填“吸热”或“放热”)反应。
(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
①表中,a为______ mol。
②由表可知,3~6min内,v(CO2)=______ mol•L-1•min-1。
③对于上述反应,下列叙述正确的是______ 。
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
| 化学键 | H-H | O=O | O-H |
| E/(kJ•mol-1) | 436 | x | 463 |
 O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8kJ能量,则根据所给键能数据可得x=(2)工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。
①计算当反应生成1.5molCH3OH(g)时,能量变化值是
②推测反应CH3OH(g)
 CO(g)+2H2(g)是
CO(g)+2H2(g)是(3)为发展低碳经济,还有科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。
CH3OH(g)+H2O(g)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,一段时间内CO2和CH3OH的物质的量随时间的变化如表所示。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH) | 0mol | 0.50mol | 0.65mol | 0.75mol | 0.75mol |
| n(CO2) | 1mol | 0.50mol | 0.35mol | a | 0.25mol |
②由表可知,3~6min内,v(CO2)=
③对于上述反应,下列叙述正确的是
A.当各气体的浓度不再改变时,该反应一定已达平衡状态
B.当该反应达到平衡后,n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
C.由表可知,3min时CH3OH的生成速率大于12min时CH3OH的分解速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】无论是在环境保护领域还是在工农业生产领域,氮及其化合物一直是我国科研重点。回答下列问题:
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
(2)消除汽车尾气中的氮氧化合物的原理之一为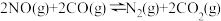 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
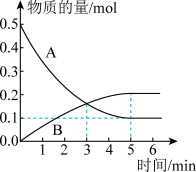
①其中B表示_______ (填“ ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。
②该温度下,反应开始至5min时该反应的平均反应速率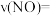
_______ 。
③3min时,反应_______ (填“达到”或“未达到”)化学平衡,6min时,正反应速率_______ (填“>”“<”或“=”)逆反应速率。
④下列情况能说明该反应达到平衡状态的是_______ (填选项字母)。
A.化学反应速率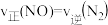
B.CO与 的物质的量之和不再发生变化
的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为_______ 。
(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。
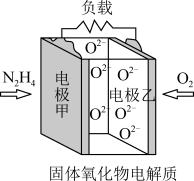
该电池的正极为_______ (填“电极甲”或“电极乙”,下同);电池工作时, 向
向_______ 移动。
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
| A.工业合成氨 |
| B.工业利用氨气合成硝酸 |
| C.雷雨天中氮气与氧气生成氮氧化合物 |
| D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 |
 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
①其中B表示
 ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。②该温度下,反应开始至5min时该反应的平均反应速率
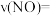
③3min时,反应
④下列情况能说明该反应达到平衡状态的是
A.化学反应速率
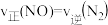
B.CO与
 的物质的量之和不再发生变化
的物质的量之和不再发生变化C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将
 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。

该电池的正极为
 向
向
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
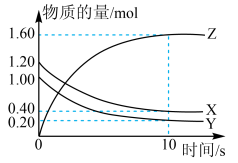
①此反应的化学方程式为________________ ;
②0~10s内,用Z表示的化学反应速率为_____________ ;
③X的转化率为________________ 。
(2)恒温恒容时,某密闭容器中发生反应:
C(s)+CO2(g) 2CO(g),下列描述中能说明该反应已达到化学平衡状态的是
2CO(g),下列描述中能说明该反应已达到化学平衡状态的是_____ 。
①C(s)的浓度不再改变
②CO2的体积分数不再改变
③气体的质量不再改变
④气体的密度不再改变
⑤单位时间内消耗1molCO2,同时生成2molCO
⑥n(CO2):n(CO)=1:2
⑦v正(CO2)=2v逆(CO)
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则

①此反应的化学方程式为
②0~10s内,用Z表示的化学反应速率为
③X的转化率为
(2)恒温恒容时,某密闭容器中发生反应:
C(s)+CO2(g)
 2CO(g),下列描述中能说明该反应已达到化学平衡状态的是
2CO(g),下列描述中能说明该反应已达到化学平衡状态的是①C(s)的浓度不再改变
②CO2的体积分数不再改变
③气体的质量不再改变
④气体的密度不再改变
⑤单位时间内消耗1molCO2,同时生成2molCO
⑥n(CO2):n(CO)=1:2
⑦v正(CO2)=2v逆(CO)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】当发动机工作时,反应产生的NO尾气是主要污染物之一,NO的脱除方法和转化机理是当前研究的热点。请回答下列问题:
(1)已知: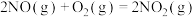
 kJ∙mol−1
kJ∙mol−1

 kJ∙mol−1
kJ∙mol−1
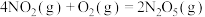
 kJ∙mol−1
kJ∙mol−1
则 是
是______ 反应(填“放热”或“吸热”),以上 氧化脱除氮氧化物的总反应是
氧化脱除氮氧化物的总反应是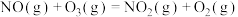

______ ,最后将 与
与______ 剂反应转化为无污染的气体而脱除。
(2)已知: 的反应历程分两步:
的反应历程分两步:
①表中 、
、 、
、 、
、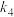 是只随温度变化的常数,温度升高将使其数值
是只随温度变化的常数,温度升高将使其数值______ (填“增大”或“减小”)。
②反应I瞬间建立平衡,因此决定 反应速率快慢的是
反应速率快慢的是______ ,则反应I与反应II的活化能的大小关系为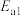
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③反应 的
的
______ (用 、
、 、
、 、
、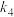 表示)。
表示)。
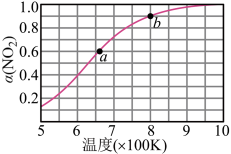
(3)将一定量的 放入恒容密闭容器中发生下列反应:
放入恒容密闭容器中发生下列反应: ,测得其平衡转化率
,测得其平衡转化率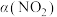 随温度变化如图所示,从b点到a点降温,平衡将向
随温度变化如图所示,从b点到a点降温,平衡将向______ 移动。图中a点对应温度下, 的起始压强为160kPa,该温度下反应的平衡常数
的起始压强为160kPa,该温度下反应的平衡常数
______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知:
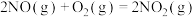
 kJ∙mol−1
kJ∙mol−1
 kJ∙mol−1
kJ∙mol−1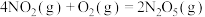
 kJ∙mol−1
kJ∙mol−1则
 是
是 氧化脱除氮氧化物的总反应是
氧化脱除氮氧化物的总反应是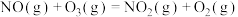

 与
与(2)已知:
 的反应历程分两步:
的反应历程分两步:步骤 | 反应 | 活化能 | 正反应速率方程 | 逆反应速率方程 |
I |
|
|
|
|
II |
|
|
|
|
 、
、 、
、 、
、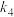 是只随温度变化的常数,温度升高将使其数值
是只随温度变化的常数,温度升高将使其数值②反应I瞬间建立平衡,因此决定
 反应速率快慢的是
反应速率快慢的是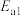
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③反应
 的
的
 、
、 、
、 、
、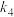 表示)。
表示)。(3)将一定量的
 放入恒容密闭容器中发生下列反应:
放入恒容密闭容器中发生下列反应: ,测得其平衡转化率
,测得其平衡转化率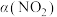 随温度变化如图所示,从b点到a点降温,平衡将向
随温度变化如图所示,从b点到a点降温,平衡将向 的起始压强为160kPa,该温度下反应的平衡常数
的起始压强为160kPa,该温度下反应的平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】I.
(1)羰基硫(COS)多产生于煤化工合成气中,能引起催化剂中毒,可通过水解反应除去,其热化学方程式为COS(g)+H2O(g) H2S(g)+CO2(g) △H,相关的化学键键能数据如下表所示:则该反应的△H为
H2S(g)+CO2(g) △H,相关的化学键键能数据如下表所示:则该反应的△H为___________ 。
Ⅱ.反应Fe(s)+CO2(g) FeO(s)+CO(g),ΔH1=−akJ∙mol−1,平衡常数为K;测得在不同温度下,K值如表:
FeO(s)+CO(g),ΔH1=−akJ∙mol−1,平衡常数为K;测得在不同温度下,K值如表:
(2)若500℃时进行反应,CO2起始浓度为2 mol∙L−1,则CO的平衡浓度为___________ 。
(3)反应中的a___________ 0(填大于、小于、等于)。
(4)700℃反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有___________。
(5)下列图像符合反应的是___________ (填序号)(图中φ是混合物中CO的含量,T为温度)。
A. B.
B. C.
C.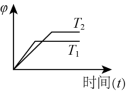
(1)羰基硫(COS)多产生于煤化工合成气中,能引起催化剂中毒,可通过水解反应除去,其热化学方程式为COS(g)+H2O(g)
 H2S(g)+CO2(g) △H,相关的化学键键能数据如下表所示:则该反应的△H为
H2S(g)+CO2(g) △H,相关的化学键键能数据如下表所示:则该反应的△H为| 化学键 | C=O(CO2) | C=O(COS) | C=S(COS) | H−S | H−O |
| E/( kJ∙mol−1) | 803 | 742 | 577 | 339 | 465 |
Ⅱ.反应Fe(s)+CO2(g)
 FeO(s)+CO(g),ΔH1=−akJ∙mol−1,平衡常数为K;测得在不同温度下,K值如表:
FeO(s)+CO(g),ΔH1=−akJ∙mol−1,平衡常数为K;测得在不同温度下,K值如表:| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(3)反应中的a
(4)700℃反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有___________。
| A.缩小反应器体积 | B.通入CO2 |
| C.升高温度到900℃ | D.使用合适的催化剂 |
A.
 B.
B. C.
C.
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)CO2催化加氢生成乙烯和水的反应中,反应物的物质的量之比n(CO2)∶n(H2)=___________ 。当反应达到平衡时,若增大压强,则n(C2H4)___________ (填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
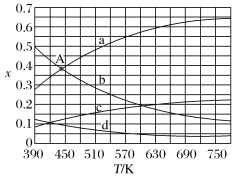
图中,表示H2、H2O变化的曲线分别是___________ 、___________ 。CO2催化加氢合成C2H4反应的ΔH___________ 0(填“大于”或“小于”)。
(3)根据图中点A(440 K,0.39),计算该温度时平衡分压p(H2O) =___________ ,p(C2H4)=___________ (分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________ 。
(1)CO2催化加氢生成乙烯和水的反应中,反应物的物质的量之比n(CO2)∶n(H2)=
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1 MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

图中,表示H2、H2O变化的曲线分别是
(3)根据图中点A(440 K,0.39),计算该温度时平衡分压p(H2O) =
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%,CO2可转化成有机物实现碳循环,有效降低碳排放。
(1)在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g)ΔH=-49.0kJ∙mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
①计算:从0min到3min,H2的平均反应速率v(H2)=_____ mol∙L-1∙min-1。
②能说明上述反应达到平衡状态的是_____ (填编号)。
A.c(CO2)∶c(CH3OH)=1∶1
B.混合气体的密度不再发生变化
C.单位时间内消耗3molH2,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
③反应达到平衡后,保持其他条件不变,能加快反应速率且使体系中气体的物质的量减少,可采取的措施有_____ (填编号)。
A.升高温度 B.缩小容器体积
C.再充入CO2气体 D.使用合适的催化剂
(2)将CO2通入适量氢氧化钠溶液中进行处理时,可生成Na2CO3溶液,在Na2CO3溶液中,下列关系式错误的是_____ 。
A.c( )>c(OH-)>c(
)>c(OH-)>c( )
)
B.c(Na+)=2c( )+2c(
)+2c( )+2c(H2CO3)
)+2c(H2CO3)
C.c(OH-)=c(H+)+c( )+2c(H2CO3)
)+2c(H2CO3)
D.c(Na+)+c(H+)=c( )+c(
)+c( )+c(OH-)
)+c(OH-)
(3)煤燃烧产生的烟气中含有氮的氧化物,用甲烷催化氧化可以还原NOx原理为:
①CH4(g)+2NO2(g)⇌ CO2(g)+N2(g)+H2O(g)ΔH=-867.0kJ/mol;
②N2(g)+2O2(g)⇌2NO2(g) ΔH=+67.8kJ/mol;
③适量的N2和O2完全反应,每生成标准状况下11.2LNO 时,则吸收45kJ的热量,则CH4催化还原NO的热化学反应方程式为_____ 。
(4)已知A(g)+B(g)⇌C(g)+D(g)ΔH,反应的平衡常数和温度的关系如下:
回答下列问题:
830℃时,向一个2L的密闭容器中充入0.20mol的A和0.80mol的B,反应至10s时达到平衡,测得A的转化率为80%,计算830℃时,反应的平衡常数x=_____ 。

(1)在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g)ΔH=-49.0kJ∙mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
①计算:从0min到3min,H2的平均反应速率v(H2)=
②能说明上述反应达到平衡状态的是
A.c(CO2)∶c(CH3OH)=1∶1
B.混合气体的密度不再发生变化
C.单位时间内消耗3molH2,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
③反应达到平衡后,保持其他条件不变,能加快反应速率且使体系中气体的物质的量减少,可采取的措施有
A.升高温度 B.缩小容器体积
C.再充入CO2气体 D.使用合适的催化剂
(2)将CO2通入适量氢氧化钠溶液中进行处理时,可生成Na2CO3溶液,在Na2CO3溶液中,下列关系式错误的是
A.c(
 )>c(OH-)>c(
)>c(OH-)>c( )
)B.c(Na+)=2c(
 )+2c(
)+2c( )+2c(H2CO3)
)+2c(H2CO3)C.c(OH-)=c(H+)+c(
 )+2c(H2CO3)
)+2c(H2CO3)D.c(Na+)+c(H+)=c(
 )+c(
)+c( )+c(OH-)
)+c(OH-)(3)煤燃烧产生的烟气中含有氮的氧化物,用甲烷催化氧化可以还原NOx原理为:
①CH4(g)+2NO2(g)⇌ CO2(g)+N2(g)+H2O(g)ΔH=-867.0kJ/mol;
②N2(g)+2O2(g)⇌2NO2(g) ΔH=+67.8kJ/mol;
③适量的N2和O2完全反应,每生成标准状况下11.2LNO 时,则吸收45kJ的热量,则CH4催化还原NO的热化学反应方程式为
(4)已知A(g)+B(g)⇌C(g)+D(g)ΔH,反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | x | 0.6 | 0.4 |
回答下列问题:
830℃时,向一个2L的密闭容器中充入0.20mol的A和0.80mol的B,反应至10s时达到平衡,测得A的转化率为80%,计算830℃时,反应的平衡常数x=

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】 是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是
是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是 和
和 ,还含有少量
,还含有少量 、
、 、
、 )为原料制取
)为原料制取 的过程如下:
的过程如下:

已知不同金属离子生成氢氧化物沉淀所需的pH如下表。
(1)“氧化”时,主要发生反应的离子方程式为___________ 。
(2)加入NiO能除去Fe、Cu的原因为___________ ,应调节溶液pH的范围为___________ 。
(3)向“除Fe、Cu”后的滤液中加入NaF溶液,使 转化为
转化为 沉淀除去。
沉淀除去。
①若溶液pH偏低,将会导致 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
②用NaF除镁而不用 ,与反应
,与反应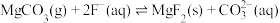 有关,该反应的平衡常数为
有关,该反应的平衡常数为___________ (结果保留两位有效数字)。[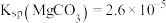 ,
,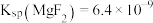 ]
]
(4) 的萃取率随溶液pH变化关系如题图所示。萃取
的萃取率随溶液pH变化关系如题图所示。萃取 时应调节溶液pH的范围为
时应调节溶液pH的范围为___________ 。
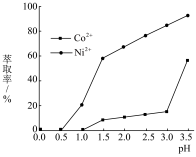
(5)通过氧化、除杂(铁、铜、镁)、萃取、反萃取、沉淀等过程,可制备 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (水层)
(水层) (有机层)
(有机层)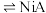 (有机层)
(有机层) (水层),则反萃取最好加入的试剂是
(水层),则反萃取最好加入的试剂是___________ 。
A. B.
B. C.
C.
 是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是
是一种蓝色易溶于水的细粒结晶,主要用于电镀、医药、以及印染工业等。以一种含镍废液(主要成分是 和
和 ,还含有少量
,还含有少量 、
、 、
、 )为原料制取
)为原料制取 的过程如下:
的过程如下:
已知不同金属离子生成氢氧化物沉淀所需的pH如下表。
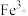 |  | 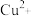 | 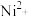 | 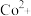 | 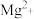 | |
| 开始沉淀的pH | 2.7 | 7.0 | 4.4 | 7.1 | 7.6 | 9.3 |
| 完全沉淀的pH | 3.7 | 9.6 | 6.4 | 9.2 | 9.2 | 10.8 |
(2)加入NiO能除去Fe、Cu的原因为
(3)向“除Fe、Cu”后的滤液中加入NaF溶液,使
 转化为
转化为 沉淀除去。
沉淀除去。①若溶液pH偏低,将会导致
 沉淀不完全,其原因是
沉淀不完全,其原因是②用NaF除镁而不用
 ,与反应
,与反应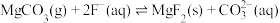 有关,该反应的平衡常数为
有关,该反应的平衡常数为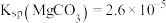 ,
,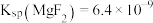 ]
](4)
 的萃取率随溶液pH变化关系如题图所示。萃取
的萃取率随溶液pH变化关系如题图所示。萃取 时应调节溶液pH的范围为
时应调节溶液pH的范围为
(5)通过氧化、除杂(铁、铜、镁)、萃取、反萃取、沉淀等过程,可制备
 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (水层)
(水层) (有机层)
(有机层)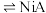 (有机层)
(有机层) (水层),则反萃取最好加入的试剂是
(水层),则反萃取最好加入的试剂是A.
 B.
B. C.
C.
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.恒温下,在容积为2L的恒容密闭容器A中通入1mol 与1mol
与1mol 的混合气体,发生如下反应:
的混合气体,发生如下反应:
 ,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
(1)平衡时 的速率为
的速率为_______ 。
(2)此温度时该反应的平衡常数为_______ 。
(3)平衡时与起始时压强之比_______ 。
(4)该反应在什么温度下_______ (填“高温”“低温”“任何温度”)自发进行。
Ⅱ.在一定容积的密闭容器中,进行如下化学反应 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:
(5)800℃在恒容密闭容器中放入混合物,各物质的浓度为 ,
, ,
, ,
, ,此时
,此时
_______  (填“=”“>”“<”或“不能确定”),该反应正反应为
(填“=”“>”“<”或“不能确定”),该反应正反应为_______ 热。
 与1mol
与1mol 的混合气体,发生如下反应:
的混合气体,发生如下反应:
 ,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol
,5min时,达到平衡,若平衡时氢气的物质的量为0.4mol(1)平衡时
 的速率为
的速率为(2)此温度时该反应的平衡常数为
(3)平衡时与起始时压强之比
(4)该反应在什么温度下
Ⅱ.在一定容积的密闭容器中,进行如下化学反应
 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 ,
, ,
, ,
, ,此时
,此时
 (填“=”“>”“<”或“不能确定”),该反应正反应为
(填“=”“>”“<”或“不能确定”),该反应正反应为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】氮及其化合物与人们的生活生产密切相关。回答下列问题:
(1)微生物作用下,废水中的NH 可转化为NO
可转化为NO ,该反应分两步反应:
,该反应分两步反应:
Ⅰ步:2 NH (aq)+3O2(g)=2NO
(aq)+3O2(g)=2NO (aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
(aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
Ⅱ步:2NO (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH=-146 kJ/mol。
(aq) ΔH=-146 kJ/mol。
则低浓度氨氮废水中的NH (aq)氧化生成NO
(aq)氧化生成NO (aq)的热化学方程式为:NH
(aq)的热化学方程式为:NH (aq)+2O2(g)=2H+(aq)+H2 O(l)+NO
(aq)+2O2(g)=2H+(aq)+H2 O(l)+NO (aq) ΔH=
(aq) ΔH=___________ kJ/mol。
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g) 2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
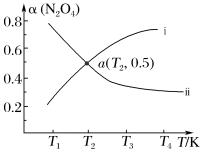
α(N2O4)随温度的变化的正确曲线是___________ (填“i”或“ii”)。若该容器中通入N2O4的起始浓度为2mol/L,则a点温度下的平衡常数K=___________ 。若加入催化剂,图中的曲线会___________ (填“上移”、“下移”或“不移”)。
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
则反应温度高的容器是___________ (填“甲”或“乙”);甲容器中,0~120 min的速率v(N2)=___________ mol/(L·min),达到化学平衡后,乙容器中各物质均加倍,则平衡向___________ (“正反应”或“逆反应”)方向移动。
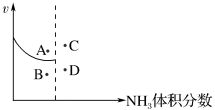
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为___________ (从点“A、B、C、D”中选择)。
(1)微生物作用下,废水中的NH
 可转化为NO
可转化为NO ,该反应分两步反应:
,该反应分两步反应:Ⅰ步:2 NH
 (aq)+3O2(g)=2NO
(aq)+3O2(g)=2NO (aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
(aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/molⅡ步:2NO
 (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH=-146 kJ/mol。
(aq) ΔH=-146 kJ/mol。则低浓度氨氮废水中的NH
 (aq)氧化生成NO
(aq)氧化生成NO (aq)的热化学方程式为:NH
(aq)的热化学方程式为:NH (aq)+2O2(g)=2H+(aq)+H2 O(l)+NO
(aq)+2O2(g)=2H+(aq)+H2 O(l)+NO (aq) ΔH=
(aq) ΔH=(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g)
 2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
α(N2O4)随温度的变化的正确曲线是
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:| t/min | 0 | 40 | 80 | 120 | 160 |
| n甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】二甲醚( )具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(
)具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(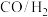 )为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
①
②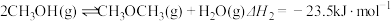
③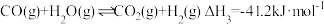
(1)一种新合成二甲醚的方法为一定条件下:
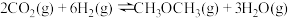 ,该反应的
,该反应的
___________  ;
;
判断该反应在一定温度下、体积恒定的密闭容器中,下列不能作为达到化学平衡状态的依据是___________ 。
A.平均摩尔质量保持不变
B.容器的密度不变
C.容器内压强保持不变
D.单位时间内消耗 ,同时消耗
,同时消耗 二甲醚
二甲醚
(2)可采用 和二甲醚催化合成乙醇。
和二甲醚催化合成乙醇。
反应①: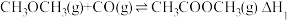
反应②: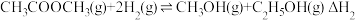
a.压强为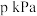 时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则
时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则
___________ (填“>”或“<”)0。
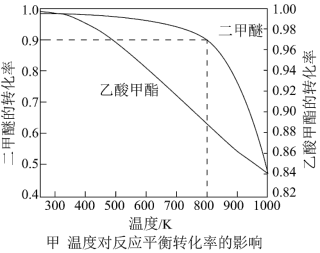
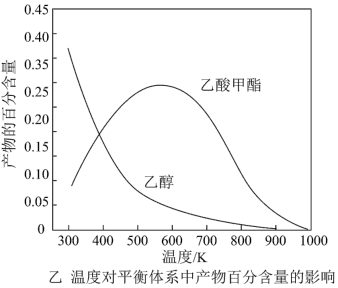
b.温度对平衡体系中乙酸甲酯的含量和乙醇的影响如图乙所示,在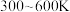 范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:
范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:___________ 。
c.若压强为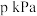 、温度为
、温度为 时,向
时,向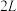 恒容密闭容器中充入
恒容密闭容器中充入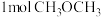 和
和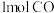 发生反应①,
发生反应①, 时达到平衡,则前
时达到平衡,则前 内
内 的平均生成速率为
的平均生成速率为___________ ,该条件下反应①的平衡常数
___________ 。
 )具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(
)具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(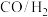 )为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:①

②
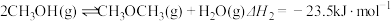
③
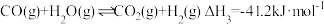
(1)一种新合成二甲醚的方法为一定条件下:
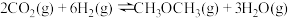 ,该反应的
,该反应的
 ;
;判断该反应在一定温度下、体积恒定的密闭容器中,下列不能作为达到化学平衡状态的依据是
A.平均摩尔质量保持不变
B.容器的密度不变
C.容器内压强保持不变
D.单位时间内消耗
 ,同时消耗
,同时消耗 二甲醚
二甲醚(2)可采用
 和二甲醚催化合成乙醇。
和二甲醚催化合成乙醇。反应①:
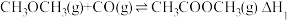
反应②:
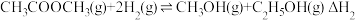
a.压强为
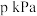 时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则
时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图甲所示,则


b.温度对平衡体系中乙酸甲酯的含量和乙醇的影响如图乙所示,在
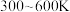 范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:
范围内,乙酸甲酯的含量逐渐增大,而乙醇的百分含量逐渐减小的原因是:c.若压强为
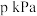 、温度为
、温度为 时,向
时,向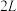 恒容密闭容器中充入
恒容密闭容器中充入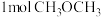 和
和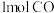 发生反应①,
发生反应①, 时达到平衡,则前
时达到平衡,则前 内
内 的平均生成速率为
的平均生成速率为
您最近一年使用:0次
【推荐3】(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+CO(g) ΔH1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;
FeO(s)+H2(g) ΔH2,平衡常数为K2;
在不同温度时K1、K2的值如下表:
①由表中数据可知:ΔH1_____ 0(填“>”、“=”、“ < ”)
②反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH
CO(g)+H2O(g) ΔH
平衡常数为K,则ΔH=________ (用ΔH1和ΔH2表示),K=________ (用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g) CO(g)+H2O(g)是
CO(g)+H2O(g)是 ______ 反应(填“吸热”或“放热”)。
(2)采用(1)中两反应产生的CO与H2合成再生能源甲醇,反应如下:CO(g)+ 2H2(g) CH3OH(g),据此回答下列问题:
CH3OH(g),据此回答下列问题:
①写出该化学反应平衡常数的表达式为:K=_____________
②该反应达平衡后升温,混合气中H2的体积百分含量增大,则合成甲醇的反应为_______ (填 “放热”或“吸热”)反应。
③若将一定量CO和H2置于容器中,保持容积不变,能说明该化学反应达到化学平衡状态的是( )
A.容器内的密度保持不变 B.2v(CO)正 = v(H2)逆
C.容器内的压强保持不变 D.消耗CO和 H2的速率比为1:2
④在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是________ ℃;若曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为____________________ 。在a点时,若达平衡后,再将CO、H2、CH3OH各充入1.0mol,平衡向____________ (填“正反应方向”、“逆反应方向”或“不”)移动。

 FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
 FeO(s)+H2(g) ΔH2,平衡常数为K2;
FeO(s)+H2(g) ΔH2,平衡常数为K2;| 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
①由表中数据可知:ΔH1
②反应CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH
CO(g)+H2O(g) ΔH 平衡常数为K,则ΔH=
 CO(g)+H2O(g)是
CO(g)+H2O(g)是 (2)采用(1)中两反应产生的CO与H2合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)
 CH3OH(g),据此回答下列问题:
CH3OH(g),据此回答下列问题:①写出该化学反应平衡常数的表达式为:K=
②该反应达平衡后升温,混合气中H2的体积百分含量增大,则合成甲醇的反应为
③若将一定量CO和H2置于容器中,保持容积不变,能说明该化学反应达到化学平衡状态的是
A.容器内的密度保持不变 B.2v(CO)正 = v(H2)逆
C.容器内的压强保持不变 D.消耗CO和 H2的速率比为1:2
④在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线z对应的温度是

您最近一年使用:0次

 (快)
(快)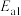
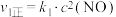
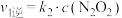
 (慢)
(慢)