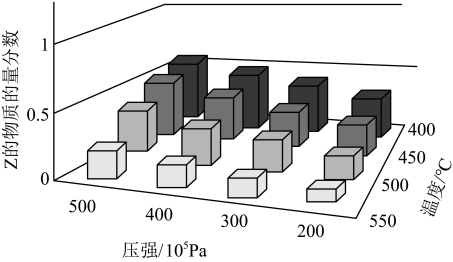
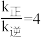恒容密闭容器中充入3 mol CH4和6 mol H2S,发生反应:CH4(g)+2H2S(g) CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是

 CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
CS2(g)+4H2(g),温度变化对平衡时各组分的物质的量分数的影响如图所示。下列说法错误的是
| A.当满足v逆(H2S)=2v正(H2)时,反应达到平衡状态 |
| B.高温、低压条件有利于提高CH4的平衡转化率 |
| C.M点时,保持温度不变,继续充入3 mol CH4和6 mol H2S,达到新平衡时,CH4的物质的量分数小于H2 |
D.图中N点对应温度下,以物质的量分数表示的化学平衡常数Kx= |
更新时间:2022-09-20 10:55:51
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,在密闭容器中进行反应:3SiCl4(g)+2N2(g)+6H2(g)  Si3N4(s)+12HCl(g)能表示上述反应达到化学平衡状态的是
Si3N4(s)+12HCl(g)能表示上述反应达到化学平衡状态的是
 Si3N4(s)+12HCl(g)能表示上述反应达到化学平衡状态的是
Si3N4(s)+12HCl(g)能表示上述反应达到化学平衡状态的是| A.3v逆(N2)=v正(H2) | B.v正(HCl)=4v正(SiCl4) |
| C.混合气体密度保持不变 | D.c(N2)∶c(H2)∶c(HCl)=1∶3∶6 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】在恒容绝热的容器中投入1molA和1molB进行反应:2A(g)+B(g) 3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
 3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是
3C(g)+D(s) △H=-akJ·mol-1(a>0),下列说法不正确的是| A.容器中压强不变,表明反应达到平衡状态 |
| B.B的体积分数不变,不能表明反应达到平衡状态 |
| C.增加A的浓度,平衡时B的体积分数减少 |
| D.反应达到平衡状态后增加D的量,容器内的温度会降低 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列有关相应图的说法正确的是
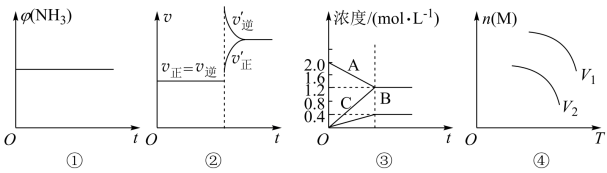

A.NH2COONH4(s) 2NH3(g)+CO2(g),将一定量纯净的氨基甲酸铵固体置于密闭容器中,图①表示NH3的体积分数随时间的变化时,表示该反应已经达到平衡状态 2NH3(g)+CO2(g),将一定量纯净的氨基甲酸铵固体置于密闭容器中,图①表示NH3的体积分数随时间的变化时,表示该反应已经达到平衡状态 |
B.对于达到平衡状态的反应:N2(g)+3H2(g) 2NH3(g),图②中表示在t0时刻充入了一定量的NH3,平衡逆向移动 2NH3(g),图②中表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
C.图③表示的化学方程式为2A(g) B(g)+3C(g) B(g)+3C(g) |
D.取amolA(g)和bmolB(g)在恒容密闭容器中发生反应:aA(g)+bB(g) mM(g)+nN(g) △H=QkJ/mol,达到平衡时,M的物质的量与容器体积、温度的关系如图④所示,若V1>V2,则a+b<m+n mM(g)+nN(g) △H=QkJ/mol,达到平衡时,M的物质的量与容器体积、温度的关系如图④所示,若V1>V2,则a+b<m+n |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用传感技术可以探究压强对2NO2(g)⇌N2O4(g)化学平衡移动的影响。在室温、100 kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞至一定位置,并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是
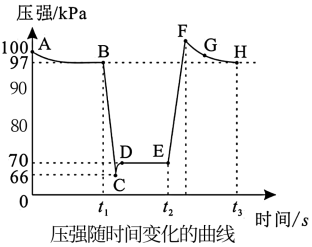

| A.t1时刻的操作是向内推活塞 |
| B.E点到H点的过程中,NO2的物质的量先增大后减小 |
| C.E、H两点对应的正反应速率大小为v(H)>v(E) |
| D.B、E两点气体的平均相对分子质量大小为M(B)>M(E) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】一定温度下向体积为2L的恒容密闭容器中充入6 molCO2和8molH2,发生反应:CO2(g)+3 H2(g)=CH3OH(g)+H2O(g) △H=-49kJ·mol-1。测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是
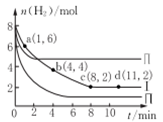
| A.该反应在O~8min内的v(CO2)=0.125mol·L-1·min-1 |
| B.若起始时向容器中充入3molCO2和4molH2,则平衡时CH3OH的体积分数大于20% |
| C.若起始时向容器中充入4molCO2和2molH2、2molCH3OH、1molH2O(g),则此时反应v(正)>v(逆) |
| D.曲线II、曲线III改变条件分别是升高温度、减小压强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】在恒容密闭容器中通入CH4与CO2,使其物质的量浓度均为1.0mol•L-1,在一定条件下发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是

 2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
2CO(g)+2H2(g)。测得平衡时CH4的体积分数与温度及压强的关系如图所示。下列说法一定正确的是
| A.a点时CH4的转化率为80% |
| B.压强力p1、p2、p3由小到大的顺序为p3<p2<p1 |
C.压强为p2时,b点处 正< 正< 逆 逆 |
| D.该反应的△H>0 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】在某温度下,向三个初始体积均为1L的密闭容器中按下表所示投料,发生反应:2SO2(g)+O2(g)  2SO3(g)△H<0。达到平衡状态,下列说法正确的是
2SO3(g)△H<0。达到平衡状态,下列说法正确的是
容器编号 | 容器类型 | 起始物质的量/mol | 平衡时SO3的 物质的量/mol | ||
SO2 | O2 | SO3 | |||
Ⅰ | 恒温恒容 | 2 | 1 | 0 | 1.2 |
Ⅱ | 绝热恒容 | 0 | 0 | 2 | a |
Ⅲ | 恒温恒压 | 2 | 1 | 0 | b |
| A.平衡时SO3的物质的量:a>1.2、b>1.2 |
| B.容器Ⅱ、Ⅲ中平衡常数相同 |
| C.容器I中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
| D.若起始时向容器Ⅰ中充入1.0molSO2(g)、0.40molO2(g)和1.40molSO3(g),则此时V正<V逆 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】控制某恒温条件,向2L密闭容器中充入1mol NO2和足量C发生下列反应:2NO2(g)+2C(s) N2(g)+2CO2(g)。10分钟达到平衡,测得平衡时NO2和CO2的物质的量浓度恰好相等,则下列说法中正确的是
N2(g)+2CO2(g)。10分钟达到平衡,测得平衡时NO2和CO2的物质的量浓度恰好相等,则下列说法中正确的是
 N2(g)+2CO2(g)。10分钟达到平衡,测得平衡时NO2和CO2的物质的量浓度恰好相等,则下列说法中正确的是
N2(g)+2CO2(g)。10分钟达到平衡,测得平衡时NO2和CO2的物质的量浓度恰好相等,则下列说法中正确的是| A.该温度下平衡常数为0.125 |
| B.若升温平衡常数减小,则△H>0 |
| C.平衡时,N2的体积分数为20% |
| D.选择适当的催化剂,可以增大反应的转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】在一定体积的密闭容器中,可逆反应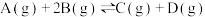 ,有如图所示的反应曲线,下列说法中错误的是
,有如图所示的反应曲线,下列说法中错误的是
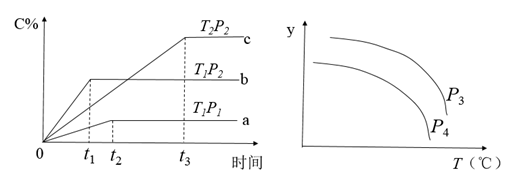
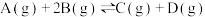 ,有如图所示的反应曲线,下列说法中错误的是
,有如图所示的反应曲线,下列说法中错误的是
| A.正反应是放热反应 | B. |
C.若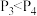 ,y轴可表示A的转化率 ,y轴可表示A的转化率 | D.若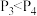 ,y轴可表示D的体积分数 ,y轴可表示D的体积分数 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
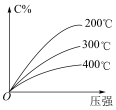
【推荐2】反应mA(g)+nB(g) eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
 eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
| A.达到平衡后,加入催化剂则C%增大 |
| B.化学方程式中n<e+f |
| C.达到平衡后,若升温,平衡左移 |
D.达到平衡后,增加 的量有利于平衡向右移动 的量有利于平衡向右移动 |
您最近一年使用:0次

 合成甲醇
合成甲醇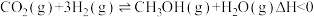 ,在
,在 密闭容器中按照不同氢碳比
密闭容器中按照不同氢碳比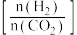 投料(曲线①~③),测得
投料(曲线①~③),测得 平衡转化率与温度的关系如图所示。已知该反应速率v=v正-v逆=k正
平衡转化率与温度的关系如图所示。已知该反应速率v=v正-v逆=k正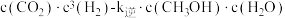 ,其中
,其中 正。
正。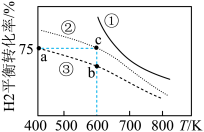
 、
、 处
处 正的大小:
正的大小:
 和
和 达到平衡,则
达到平衡,则